Clear Sky Science · pl
Szczepionka przeciw mutantowi KRAS z podwójną blokadą punktów kontrolnych w resekcyjnym raku trzustki: badanie fazy I
Nowe nadzieje przeciw zabójczemu rakowi
Rak trzustki należy do najbardziej śmiertelnych nowotworów, głównie dlatego, że rozprzestrzenia się wcześnie i często nawraca nawet po operacji i chemioterapii. W tym badaniu badacze analizują nowy rodzaj „programu szkoleniowego” dla układu odpornościowego: szczepionkę zaprojektowaną tak, by rozpoznawać powszechne mutacje w genie napędzającym nowotwór, KRAS, w połączeniu z dwoma współczesnymi lekami immunoterapeutycznymi. U osób, które przeszły usunięcie guza trzustki, podejście to ma na celu wykorzenienie niewidocznych „nasion” nowotworu, zanim odrosną.
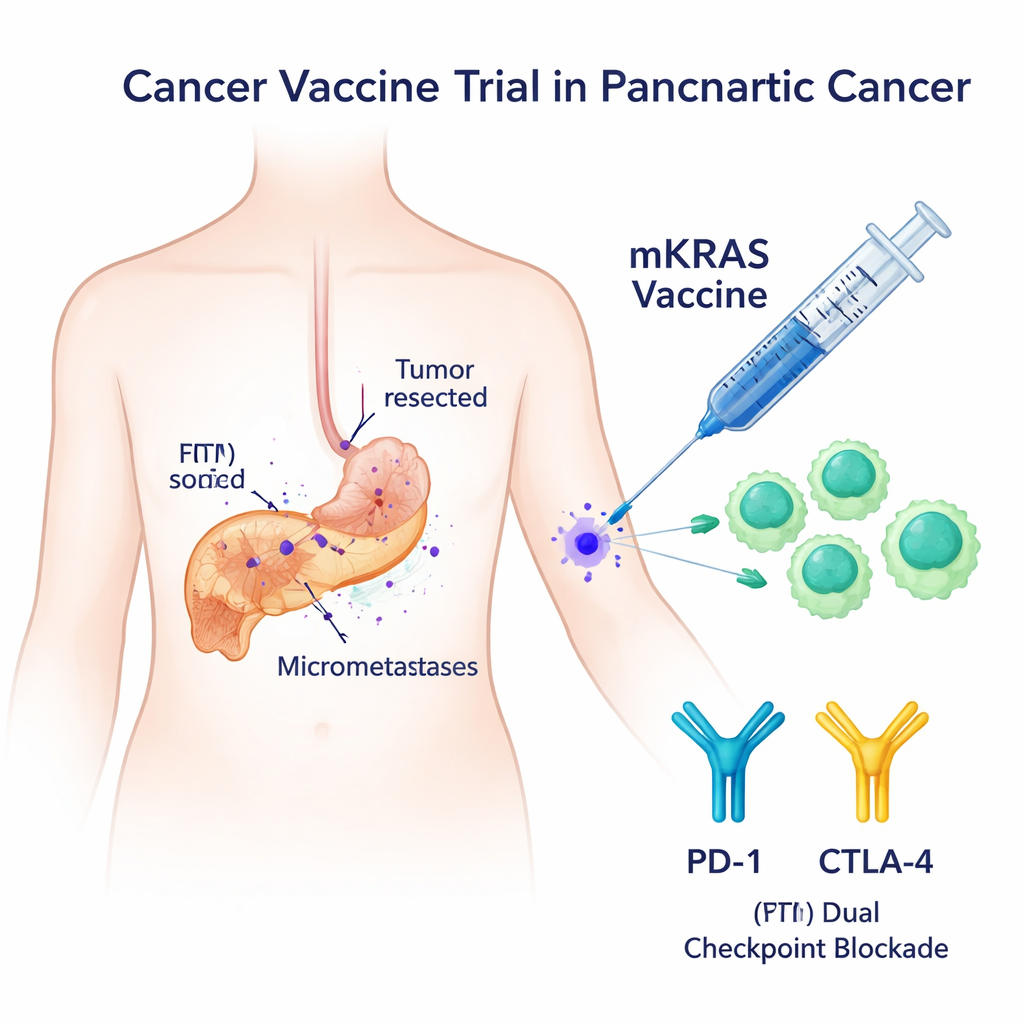
Precyzyjny cel: mutant KRAS
Większość guzów trzustki nosi zmiany w genie KRAS, które działają jak zablokowany pedał gazu dla wzrostu komórek. Te zmutowane wersje — takie jak G12V, G12D, G12R, G12C, G12A i G13D — niemal nigdy nie występują w tkankach zdrowych, co czyni je atrakcyjnym celem dla układu odpornościowego. Wcześniejsze próby szczepionek skierowanych przeciw KRAS dawały tylko umiarkowane odpowiedzi immunologiczne i koncentrowały się zwykle na jednej lub dwóch mutacjach. W tym badaniu fazy I badacze przetestowali szerszą szczepionkę, nazwaną mKRAS-VAX, która łączy sześć długich peptydów reprezentujących najczęstsze mutacje KRAS i stosuje je wraz z dwoma lekami blokującymi „punkty kontrolne” — nivolumabem i ipilimumabem — które pomagają uwolnić limfocyty T, gdyby w innym wypadku były hamowane.
Projektowanie i podawanie strategii szczepienia
Do badania włączono 12 osób, których guzy trzustki zostały usunięte chirurgicznie i które ukończyły standardową chemioterapię, lecz nadal miały wysoki ryzyko nawrotu. Guz każdego uczestnika nosił jedną z sześciu mutacji KRAS zawartych w szczepionce. W początkowej fazie „primingu” pacjenci otrzymywali cztery serie koktajlu peptydowego zmieszanego z adiuwantem stymulującym układ odpornościowy, równocześnie z dwoma lekami blokującymi punkty kontrolne. Potem podawano dawki przypominające, a niektórzy pacjenci, którzy po roku pozostawali wolni od choroby, kontynuowali jedynie przypomnienia szczepionkowe. Główne pytania dotyczyły tego, czy to połączenie jest bezpieczne i czy wyraźnie zwiększy liczbę limfocytów T ukierunkowanych na KRAS we krwi.
Szkolenie i śledzenie komórek odpornościowych
Pobierane próbki krwi przed i po szczepieniu poddawano ekspozycji na każdy peptyd KRAS, aby sprawdzić, ile komórek T wytwarza interferon gamma — kluczowy przekaźnik aktywności immunologicznej. Wyniki były uderzające jak na małe badanie: u 11 z 12 pacjentów zaobserwowano znaczący wzrost liczby komórek T rozpoznających peptydy zmutowanego KRAS ogólnie, a u 10 z 12 wystąpiła silna odpowiedź przeciw specyficznej mutacji KRAS występującej w ich guzie. Wielu pacjentów reagowało na kilka z sześciu wariantów KRAS, a niektóre komórki T potrafiły rozpoznawać więcej niż jedną mutację, co sugeruje pewien stopień korzystnej reaktywności krzyżowej. Szczegółowe profilowanie wykazało, że większość komórek wywołanych szczepionką to pomocnicze limfocyty CD4 o cechach pamięci, wspierane przez mniejszą, lecz istotną grupę cytotoksycznych limfocytów CD8 zdolnych do zabijania. Zespół zmapował i zklonował także setki receptorów komórek T specyficznych dla KRAS, w tym niektóre „publiczne” receptory współdzielone między różnymi pacjentami, co może mieć wartość dla przyszłych terapii opartych na komórkach.
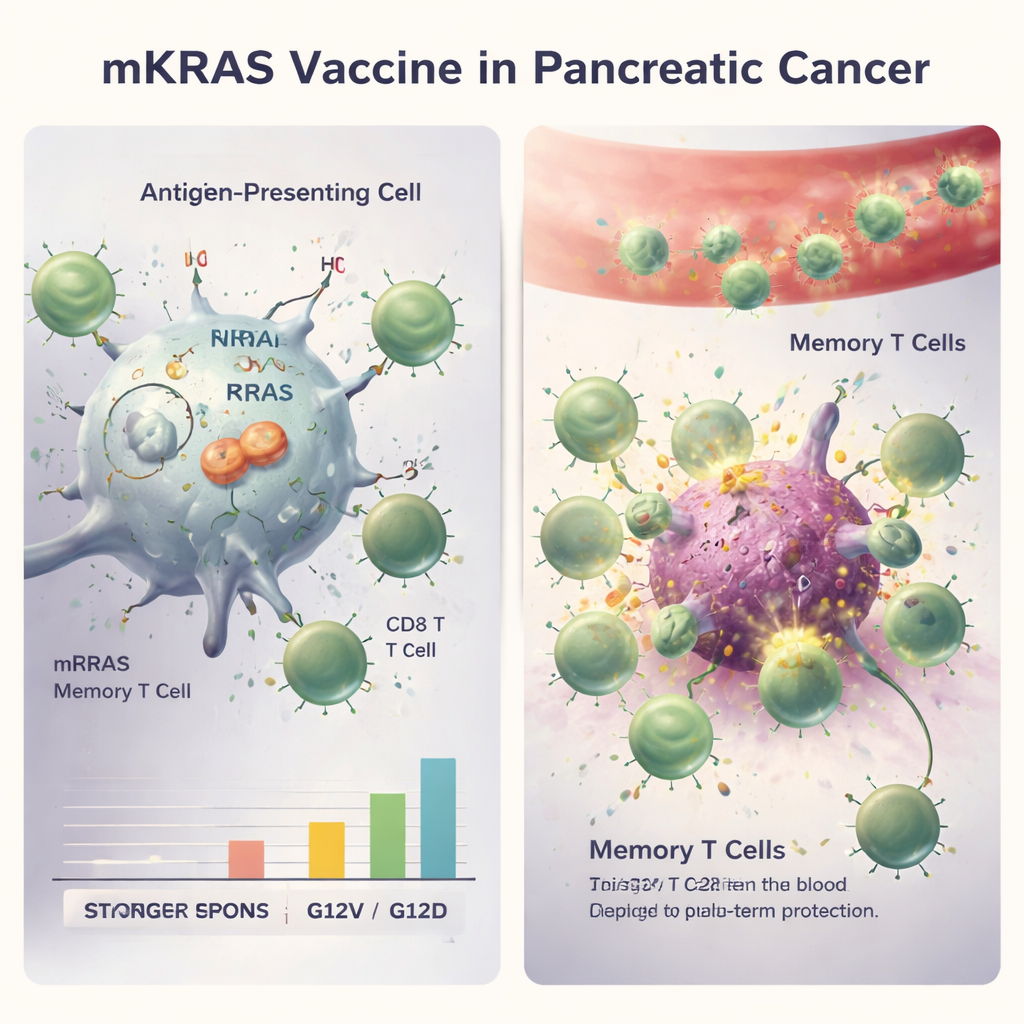
Wczesne sygnały kliniczne i różnice zależne od mutacji
Choć badanie nie było wystarczająco duże, by udowodnić korzyść w przeżyciu, pojawiły się zachęcające wskazówki. Pacjenci, których odpowiedzi komórek T ukierunkowanych na KRAS plasowały się w górnych trzech kwartylach, mieli tendencję do dłuższego pozostawania wolnymi od wykrywalnego nowotworu niż ci o słabszych odpowiedziach. Po około trzech latach obserwacji jedna trzecia uczestników nadal była wolna od choroby. Wszyscy czterej pacjenci, którzy pozostawali wolni od raka przy ostatnim badaniu kontrolnym, mieli guzy z KRAS G12V lub G12R, a ich komórki T specyficzne dla KRAS utrzymywały się ponad rok, szczególnie komórki pamięci CD4. Natomiast guzy z mutacją G12D nie tylko wykazywały słabsze odpowiedzi immunologiczne, lecz częściej nawracały, co potwierdza inne badania wiążące G12D z bardziej agresywnym przebiegiem choroby. Co ważne, działania niepożądane związane ze szczepionką były łagodne (głównie ból w miejscu podania, zmęczenie i gorączka), a poważniejsze powikłania immunologiczne wynikały głównie z leków blokujących punkty kontrolne, a nie ze szczepionki.
Co to może oznaczać dla przyszłych pacjentów
Mówiąc wprost, to badanie pokazuje, że „gotowa do użycia” szczepionka celująca w wiele mutantów KRAS, w połączeniu z nowoczesnymi lekami blokującymi punkty kontrolne, może bezpiecznie wywołać szeroką i trwałą odpowiedź limfocytów T u większości osób z wysokim ryzykiem nawrotu raka trzustki. Chociaż wielu pacjentów wciąż doświadczyło nawrotu choroby, ci ze silniejszymi odpowiedziami ukierunkowanymi na KRAS mieli tendencję do lepszych wyników, co sugeruje, że dalsze wzmocnienie tych odpowiedzi — albo wcześniejsze rozpoczęcie szczepień — może poprawić rokowania. Obszerna biblioteka receptorów komórek T specyficznych dla KRAS odkryta w tym badaniu otwiera również drzwi do terapii opartych na modyfikowanych komórkach T. Razem wyniki te sugerują, że zamiana KRAS z notorycznego promotora raka w rozpoznawalną przez układ odpornościowy „flagę” może stać się kluczową strategią zapobiegania nawrotom raka trzustki.
Cytowanie: Huff, A.L., Haldar, S.D., Gergis, A.A. et al. Mutant KRAS vaccine with dual checkpoint blockade in resected pancreatic cancer: a phase I trial. Nat Commun 17, 1538 (2026). https://doi.org/10.1038/s41467-026-68324-4
Słowa kluczowe: szczepionka na raka trzustki, mutant KRAS, immunoterapia, odpowiedź limfocytów T, blokada punktów kontrolnych