Clear Sky Science · pl
Struktura kompleksu SHOC2-KRAS-PP1C ujawnia izoformowe determinanty RAS i wgląd w celowanie w montaż kompleksu przez inhibitory RAS
Jak komórki decydują, kiedy rosnąć
Nasze komórki polegają na wewnętrznym systemie przewodów, który decyduje, kiedy rosnąć, dzielić się lub pozostawać w stanie spoczynku. W centrum tego systemu znajdują się białka RAS, drobne cząsteczkowe przełączniki, które często zawodzą w raku. To badanie zagląda głęboko w to, jak szczególna grupa białek — SHOC2, RAS i PP1C — łączy się, by przekręcić kluczowy przełącznik wzrostu, oraz jak współczesne leki przeciwnowotworowe można by dostroić, by skuteczniej blokować ten proces i zapobiegać przechytrzeniu terapii przez guzy.
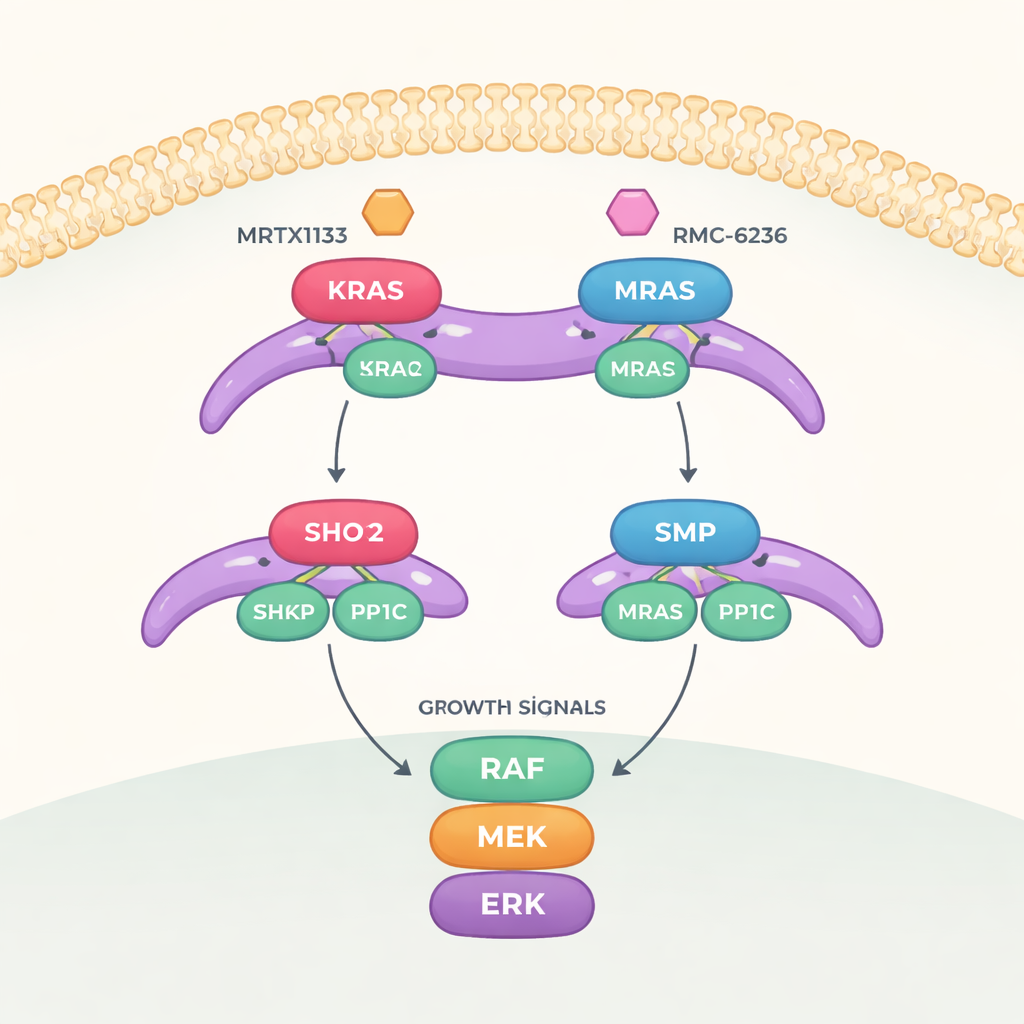
Przełącznik wzrostu z trzema kluczowymi elementami
Praca koncentruje się na szlaku sygnałowym zwanym ścieżką MAPK, która przekazuje sygnały wzrostu z powierzchni komórki do jądra. Aby ten szlak został w pełni włączony, białko RAF musi zostać przełączone ze stanu „wyłączonego” do „włączonego”. Ten przełącznik kontrolowany jest przez trójelementowy kompleks złożony z SHOC2 (rusztowania, które wszystko łączy), PP1C (enzym usuwający grupę fosforanową) oraz aktywnego białka RAS. Po złożeniu ten trio usuwa specyficzną resztę fosforanową z RAF, uwalniając go do aktywacji kaskady wzrostu położonej poniżej.
Dlaczego partner o niższym powinowactwie ma znaczenie w raku
Istnieje kilka rodzajów białek RAS. MRAS tworzy bardzo silny kompleks z SHOC2 i PP1C, podczas gdy lepiej znane napędzacze nowotworów — KRAS, HRAS i NRAS — tworzą słabsze wersje tego samego kompleksu. Co zaskakujące, komórki nowotworowe napędzane mutantami KRAS, HRAS lub NRAS okazują się silnie zależne od SHOC2, mimo że ich kompleksy są mniej stabilne. Duże zbiory danych z przesiewów genetycznych pokazują, że wiele guzów z określonymi mutacjami RAS — szczególnie wpływającymi na pozycje kluczowe, takie jak Q61 i G13 — jest wysoce wrażliwych na utratę SHOC2, co oznacza, że to złożenie jest istotne dla ich przetrwania.
Ujawnienie kształtu kompleksu KRAS
Dotychczas naukowcy widzieli jedynie strukturę o wysokiej rozdzielczości silnego kompleksu opartego na MRAS. Słabsza wersja z KRAS rozpadała się zbyt łatwo, by ją uchwycić. W tym badaniu autorzy użyli mutacji związanych z chorobą, które subtelnie wzmacniają kontakty między składnikami, aby ustabilizować kompleks SHOC2–KRAS–PP1C wystarczająco długo do zobrazowania go techniką krioelektronowej mikroskopii. Stwierdzili, że ogólna architektura jest bardzo zbliżona do kompleksu MRAS, ale KRAS pozbawiony jest kilku drobnych cech strukturalnych, których MRAS używa do mocniejszego chwytania SHOC2 i PP1C. W rezultacie kompleks z KRAS zakrywa mniejszą powierzchnię kontaktu i tworzy mniej wiązań, co wyjaśnia, dlaczego jest z natury mniej stabilny, mimo że pozostaje bardzo ważny w guzach z nadaktywnością KRAS.
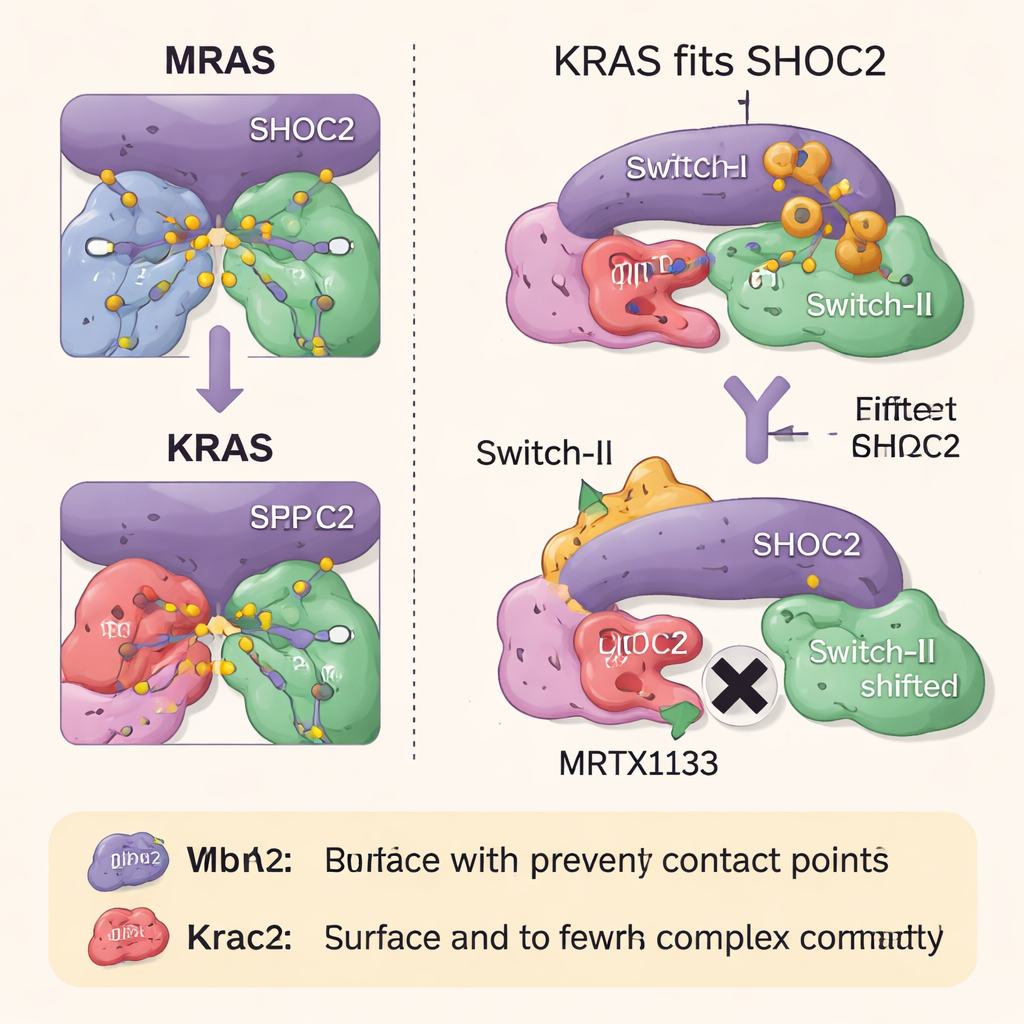
Jak leki na RAS blokują montaż kompleksu
Zespół następnie zbadał, jak dwie klasy leków celujących w RAS wpływają na ten trójelementowy kompleks. MRTX1133, zaprojektowany, by wiązać kieszeń w pobliżu elastycznego regionu KRAS znanego jako Switch‑II, blokuje ten region w kształcie, który koliduje z powierzchnią SHOC2. To silnie zapobiega formowaniu się nowych kompleksów SHOC2–KRAS–PP1C, chociaż mniej skutecznie rozbija już istniejące. Drugi lek, RMC‑6236, działa razem z białkiem pomocniczym (cyklofiliną A) i również blokuje te same powierzchnie KRAS potrzebne do wiązania SHOC2. Żaden z tych leków jednak naturalnie nie wiąże MRAS, więc wysokoprzepływowy kompleks MRAS pozostaje nienaruszony i może pomóc ponownie uruchomić szlak wzrostu, gdy KRAS jest inhibowany.
W kierunku podwójnego celowania, aby zapobiec oporności
Aby sprawdzić, czy możliwe jest podwójne celowanie, badacze skonstruowali wersję MRAS, której kieszeń Switch‑II została zmodyfikowana tak, by MRTX1133 mógł teraz wiązać. Ten mutant nadal tworzył silny kompleks z SHOC2 i PP1C, ale lek teraz blokował jego składanie i zmniejszał zdolność do włączania RAF w testach probówkowych. W połączeniu z danymi na temat związków wiążących SHOC2, wyniki te pokazują, że realistyczne jest zaprojektowanie leków, które wyłączą zarówno kompleks oparty na KRAS, jak i na MRAS. Dla osoby nietechnicznej kluczowy wniosek jest taki, że komórki nowotworowe używają wielu, blisko spokrewnionych przełączników, aby utrzymać przepływ sygnałów wzrostu, zwłaszcza gdy jeden przełącznik zostaje zahamowany przez lek. Poprzez zrozumienie precyzyjnych kształtów i kontaktów w tych zespołach białkowych, badacze mogą teraz planować terapie, które jednocześnie uderzą w obie drogi zapasowe, utrudniając komórkom napędzanym przez RAS adaptację i rozwój oporności na leczenie.
Cytowanie: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Słowa kluczowe: sygnalizacja RAS, inhibitory KRAS, szlak MAPK, kompleksy białkowe, oporność na leki