Clear Sky Science · pl
Odwracalne, lipidowo pośredniczone pH‑sterowanie koneksyną‑46/50 ujawnione metodą cryo‑EM
Dlaczego drobne kanały komórkowe mają znaczenie dla zdrowia i chorób
Każdej sekundy nasze komórki wymieniają sygnały elektryczne i małe cząsteczki przez mikroskopijne tunele zwane połączeniami szczelinowymi. Te kanały pomagają sercu bić synchronicznie, mózgowi usuwać toksyczne produkty przemiany materii, a soczewce oka zachować przejrzystość. Gdy wnętrze komórek staje się kwaśne, jak ma to miejsce podczas udaru, zawału serca czy powstawania zaćmy, wiele z tych kanałów się zamyka — lecz w jaki sposób wyczuwają i reagują na kwaśne środowisko, pozostawało długo tajemnicą. W tym badaniu zastosowano wysokorozdzielczą cryo‑elektronową mikroskopię, aby niemal atom po atomie ujawnić, jak konkretne kanały w soczewce oka zamykają się w odpowiedzi na kwasowość i jak ten proces może być całkowicie odwracalny.
Komórkowe tunele, które utrzymują tkanki w synchronii
Połączenia szczelinowe zbudowane są z białek zwanych koneksynami, które składają się w pierścieniowe kanały przechodzące przez błony dwóch sąsiednich komórek. Praca koncentruje się na parze blisko spokrewnionych koneksyn, koneksynie‑46 i koneksynie‑50, które tworzą kanały w soczewce oka. Te kanały umożliwiają przepływ jonów i małych cząsteczek bezpośrednio między komórkami, pomagając utrzymać przejrzystość soczewki i ogólne zdrowie tkanki. Jednak gdy komórki są poddane stresowi, te same kanały mogą stać się drogami dla szkodliwych sygnałów. Aby chronić tkanki, połączenia szczelinowe zamykają się, kiedy wnętrze komórki staje się bardziej kwaśne. Zrozumienie szczegółowego mechanizmu tego „pH‑sterowania” jest istotne dla wyjaśnienia, jak tkanki przetrwają stres i dlaczego niektóre mutacje prowadzą do chorób, takich jak zaćma.
Obserwowanie ruchu kanałów za pomocą cryo‑EM
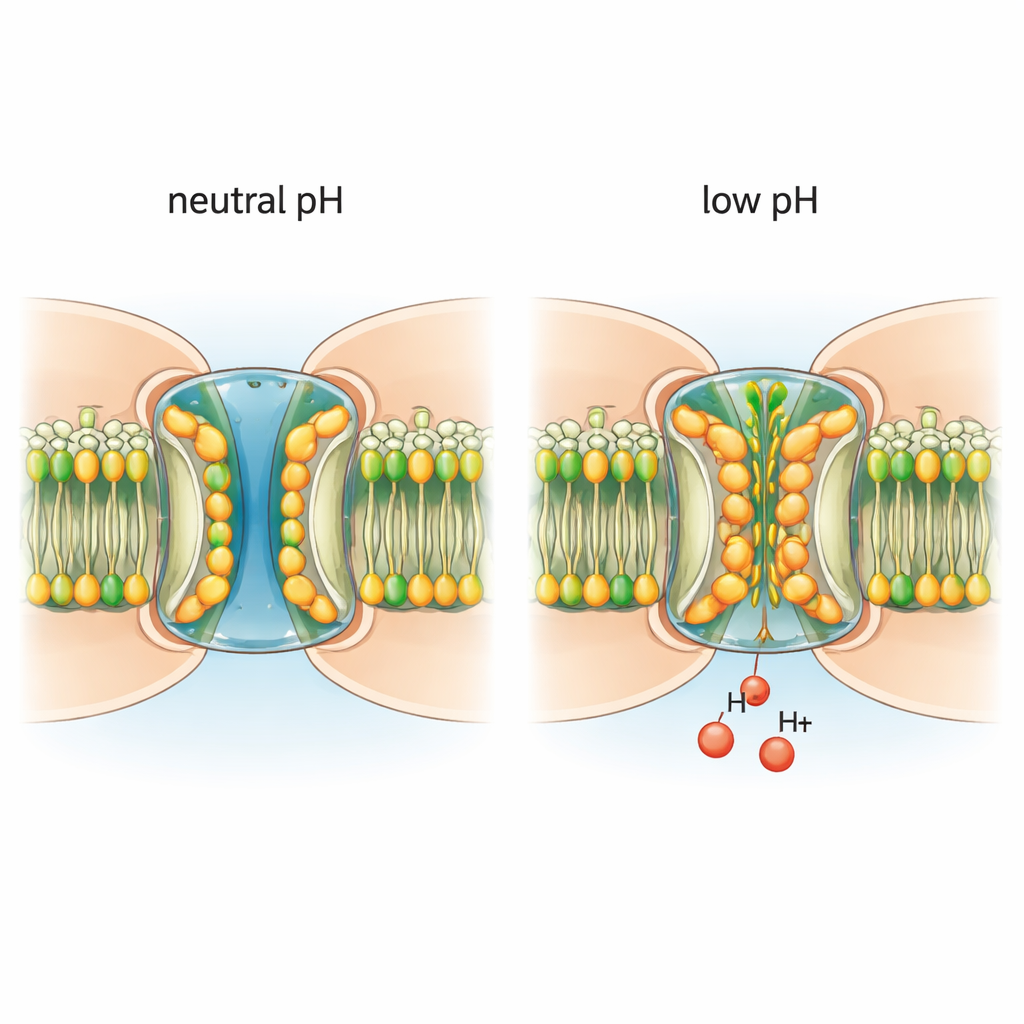
Naukowcy oczyścili natywne kanały koneksyny‑46/50 z soczewek starych owiec i osadzili je w modelowej błonie. Używając cryo‑elektronowej mikroskopii, obrazowali kanały w niemal atomowej rozdzielczości w warunkach neutralnych, sprzyjających otwartemu pory, oraz w warunkach łagodnie kwaśnych, które wywołują zamykanie. Przy neutralnym pH kanały w większości przyjmują stabilny stan otwarty, z centralnym tunelem na tyle szerokim, że mogą przechodzić jony i drobne cząsteczki, oraz z elastycznym odcinkiem – domeną N‑terminalną – wyściełającą wejście do poru. W tych warunkach por jest czysty: brak dodatkowych cząsteczek blokujących drogę, a otaczające lipidy błonowe pozostają ułożone w regularne warstwy.
Kwasowość przyciąga lipidy do poru
Gdy środowisko stało się łagodnie kwaśne, architektura kanału zmieniła się w uderzający sposób. Molekuły lipidowe z otaczającej błony zostały wciągnięte do poru, wsuwając się między i pod segmenty N‑terminalne. Najeżdżające lipidy tworzą dwuwarstwową hydrofobową „uszczelkę”, która popycha domeny N‑terminalne do środka, zawężając kanał i pomagając blokować przepływ. Dodatkowe lipidy klinują się między sąsiednimi podjednostkami białkowymi na ich powierzchniach styku, pełniąc najwyraźniej rolę ścieżek wejściowych z błony do poru. Co ważne, gdy kanały umieszczono w środowisku detergentowym, które nie zawiera prawdziwej błony lipidowej, niskie pH nie wywoływało już tych zmian strukturalnych. To dowodzi, że prawdziwe lipidy nie są tylko biernymi obserwatorami: są wymaganymi partnerami w procesie pH‑sterowania.
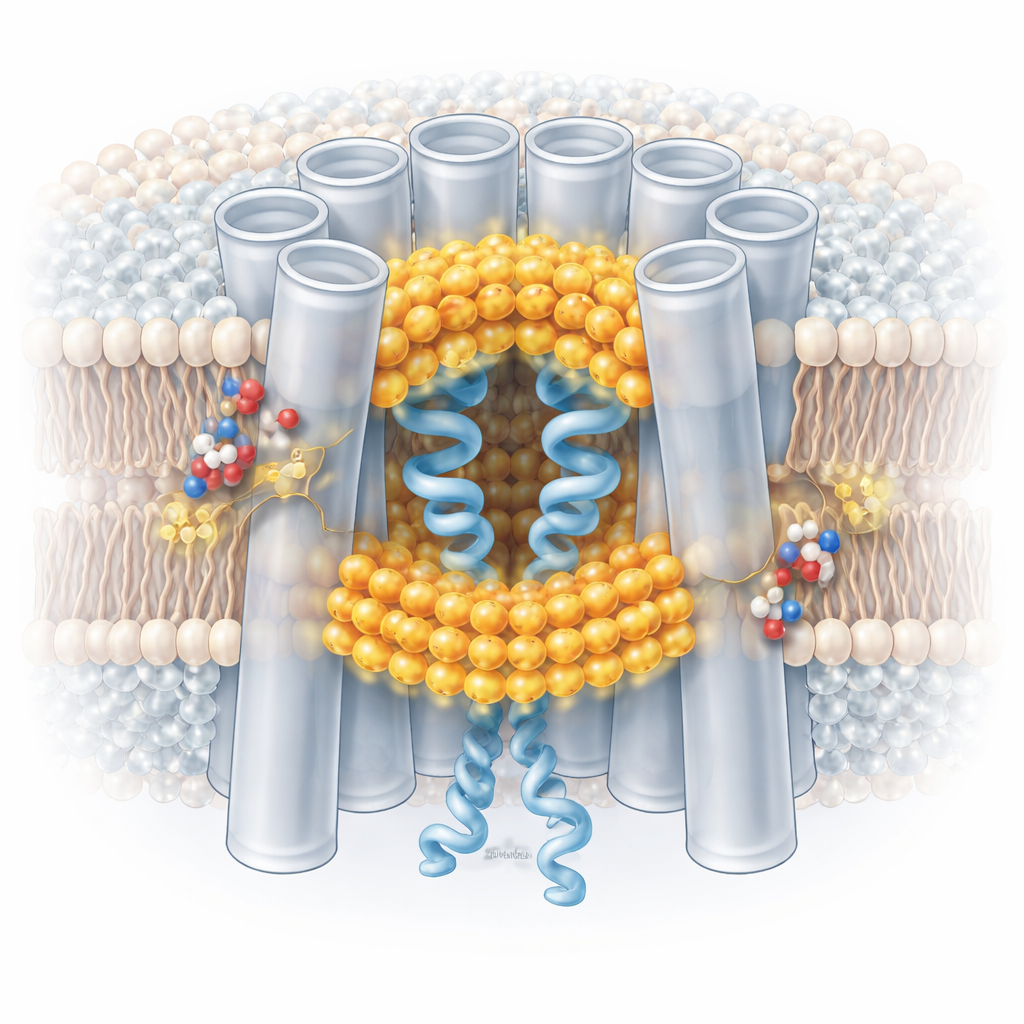
Odwracalny i precyzyjnie dostrojony wyłącznik bezpieczeństwa
Śledząc miliony pojedynczych cząstek kanału, autorzy odkryli, że niskie pH nie przełącza kanałów po prostu z całkowicie otwartego na całkowicie zamknięty. Zamiast tego przesuwa populację w kierunku mieszaniny stanów: niektóre podjednostki w kanale wykazują lipidowo‑stabilizowane, zamknięte konformacje, podczas gdy inne pozostają bardziej otwarte. Zachowanie zamykania jest w dużej mierze niekooperatywne — każdy element budulcowy kanału może reagować w pewnym stopniu niezależnie. Warunki kwaśne faworyzują te zamknięte konformacje, lecz gdy pH powraca do neutralnego, lipidy poru cofają się z powrotem do błony, a kanały wracają do stanu otwartego. Zachowane aminokwasy zwane histydynami, które zyskują dodatni ładunek przy niskim pH, wydają się pomagać rekrutować i stabilizować lipidy interfejsu inicjujące ten proces, oferując wiarygodny molekularny sensor pH.
Implikacje dla zaćmy i ochrony tkanek
Wyniki wspierają model, w którym lipidy działają jak ruchome zaślepki, które odwracalnie kontrolują przepływ przez połączenia szczelinowe w odpowiedzi na kwasowość. W soczewce oka taki mechanizm może pomagać izolować uszkodzone komórki i zapobiegać rozprzestrzenianiu się toksycznych sygnałów, ale przewlekłe lub niewłaściwie regulowane zamykanie może także przyczyniać się do rozwoju zaćmy związanej z wiekiem. Ponieważ podobne wtargnięcia lipidów zaobserwowano w pokrewnych rodzinach kanałów, praca sugeruje bardziej ogólną zasadę: pod wpływem stresu same błony komórkowe mogą dostarczać dynamicznych komponentów, które pomagają przełączać kluczowe kanały, co otwiera nowe pomysły na leki stabilizujące stan otwarty lub zamknięty w chorobie.
Cytowanie: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Słowa kluczowe: połączenia szczelinowe, koneksyna 46/50, pH‑sterowanie, zaćma, cryo‑EM