Clear Sky Science · pl
Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction
Dlaczego życie miłosne pasożyta ma znaczenie
Schistosomatoza to choroba pasożytnicza, która dotyka ponad 250 milionów ludzi, głównie w biedniejszych regionach o ograniczonym dostępie do opieki medycznej. Choroba nie wynika z ukąszeń czy toksyn robaków, lecz z ogromnej liczby jaj składanych przez samice wewnątrz ciała gospodarza. Co zaskakujące, samice potrzebują kopulacji z samcem, by dojrzeć i rozpocząć składanie jaj. W badaniu postawiono proste, lecz kluczowe pytanie: co dokładnie robi samiec, by włączyć płodność samicy — i czy można wyłączyć ten przełącznik, aby zatrzymać chorobę?
Mapowanie ukrytego świata komórka po komórce
Aby to sprawdzić, badacze stworzyli szczegółowy „atlas komórek” przywrzęba krwi Schistosoma japonicum w kluczowym oknie, gdy samce i samice się parują i osiągają dojrzałość płciową. Wykorzystując transkryptomikę pojedynczych komórek (single-cell RNA sequencing), technikę odczytującą aktywność genów w pojedynczych komórkach, przeanalizowali ponad 100 000 komórek pochodzących z robaków zebranych w czterech punktach czasowych po zakażeniu myszy. Zidentyfikowali 76 odrębnych typów komórek, w tym liczne rodzaje komórek nerwowych, komórek macierzystych i komórek rozrodczych. Pozwoliło to śledzić, jak poszczególne populacje komórek się rozrastają, kurczą lub zmieniają tożsamość w miarę wzrostu robaków i rozpoczęcia rozmnażania.
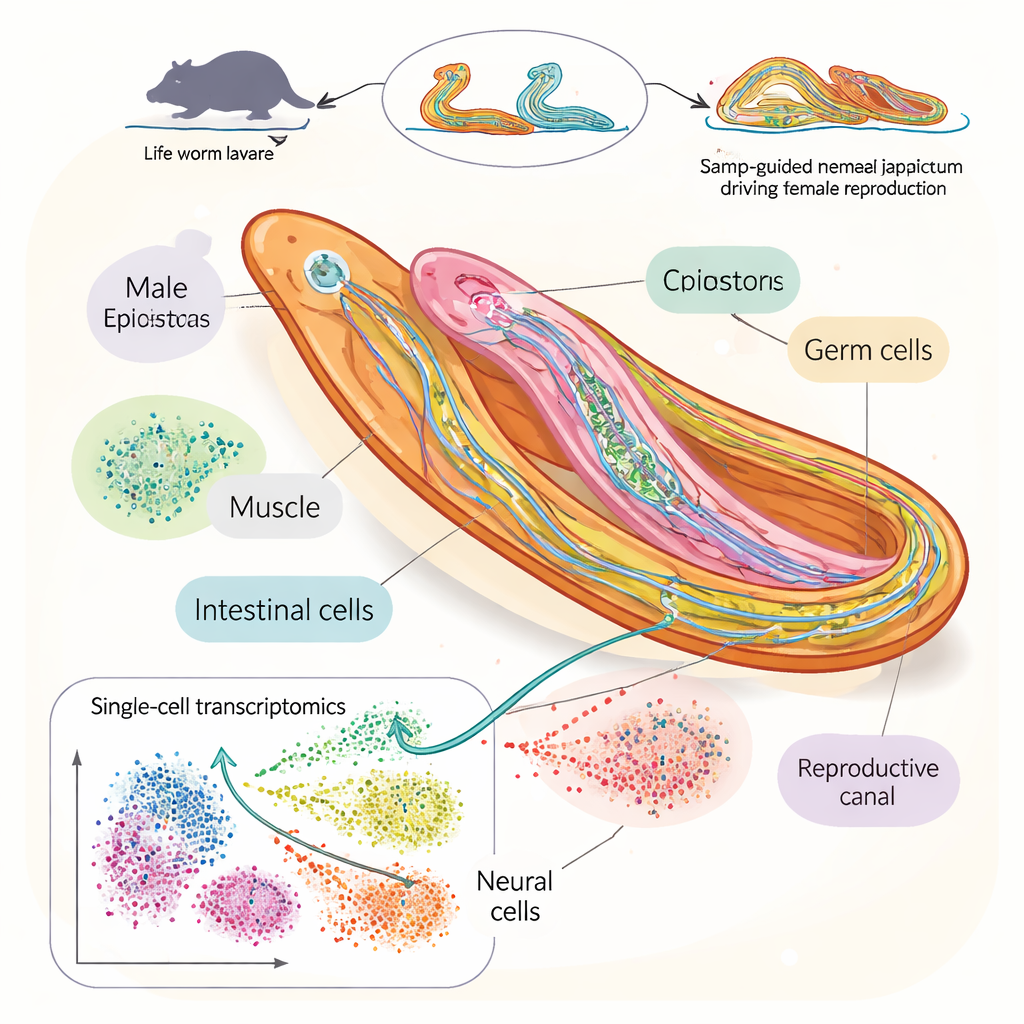
Śledzenie pojawienia się jaj i plemników
Skupiając się na komórkach z jąder, jajników i powiązanych tkanek, zespół odtworzył etapowy rozwój plemników i komórek jajowych. Pokazali, jak komórki macierzyste linii germinalnej dają początek dojrzałym stadiów plemników i jaj poprzez odrębne programy aktywności genów u samców i samic. U samic geny wspierające rozwój jaj kładą nacisk na produkcję i pakowanie białek, natomiast u samców dominują geny związane ze strukturami takimi jak rzęski i mikrotubule, które pomagają plemnikom w ruchu. Badanie zmapowało również rozwój masywnego narządu wspierającego jaja u samic — witellarii — przez stadia pośrednie i zidentyfikowało nowe markery genetyczne wskazujące na stopień dojrzałości poszczególnych tkanek rozrodczych.
Obwód nerwowy tylko u samca w kanale obejmowania
Jedno z najbardziej uderzających odkryć dotyczyło układu nerwowego. Zamiast luźnej zbieraniny neuronów atlas ujawnił pięć wyraźnych linii neuronalnych, w tym kilka różniących się między samcami i samicami. Trzy typy neuronów — oznaczone jako N2.2, N3.2 i N4.3 — były silnie wzbogacone u samców i skupione w kanale gynekoforycznym, specjalnym rowku, którym samiec obejmuje samicę. Wśród nich neurony N4.3 wyróżniały się ekspresją genu nrps, kodującego enzym produkujący BATT — drobny peptyd-feromon wykazany wcześniej jako stymulator rozwoju płciowego samic. Innymi słowy, komórki N4.3 działają jako „stacje sygnałowe” samca uruchamiające płodność samicy.
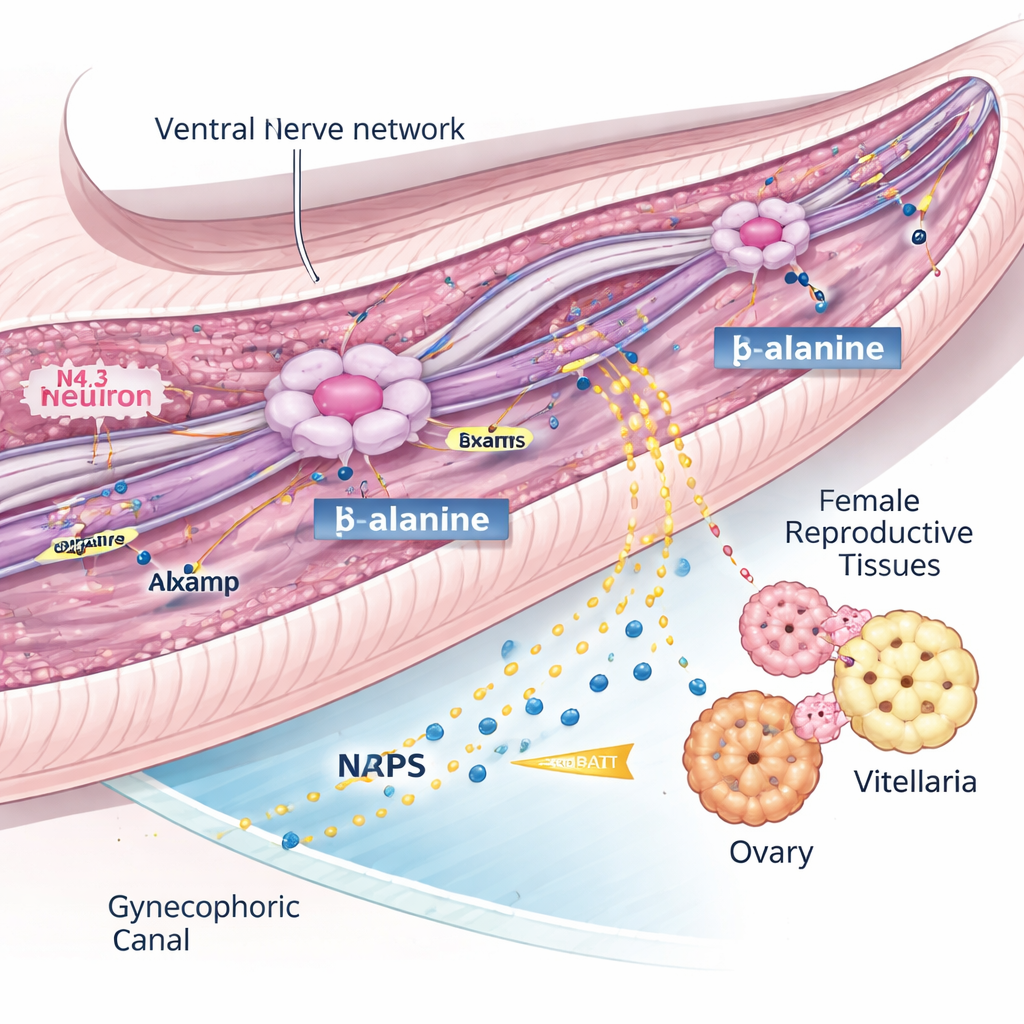
Cząsteczka przewodnia, która utrzymuje przepływ sygnału
Aby zrozumieć działanie neuronów N4.3, badacze szukali genów kierujących ich rozwojem i funkcją. Skoncentrowali się na lsamp — genie znanym u innych zwierząt z udziału w łączeniu komórek nerwowych i utrzymaniu aksonów. U samców lsamp był włączony w tych samych neuronach N4.3 produkujących enzym BATT, a jego aktywność gwałtownie wzrastała w miarę dojrzewania robaków. Przy użyciu interferencji RNA do zmniejszenia ekspresji lsamp u samców zespół zaobserwował, że sparowane samice nie rozwijały w pełni jajników i witellarii i składały niemalże brak jaj. Mimo to neurony N4.3 były nadal obecne, gen nrps był aktywny, a surowe chemiczne składniki do syntezy BATT pozostały niezmienione. Zamiast tego samce z ograniczonym lsamp wykazywały uszkodzone włókna nerwowe i zaburzenia transportu pęcherzyków wzdłuż ustabilizowanych mikrotubuli oraz wytwarzały znacznie mniej BATT wewnątrz ciała i do otaczającego środowiska. To sugeruje, że lsamp jest niezbędny do utrzymania brzusznego układu nerwowego dostarczającego kluczowy prekursor, prawdopodobnie β-alaninę, do neuronów N4.3, aby mogły syntetyzować wystarczającą ilość feromonu aktywującego samicę.
Wyłączenie przełącznika rozrodczego
Dla osób niezwiązanych z dziedziną główne przesłanie jest takie: zdolność tego pasożyta do wywoływania choroby zależy od intymnej „rozmowy” między samcem i samicą, prowadzonej przez wyspecjalizowaną sieć nerwową i niewielki feromon. Badanie pokazuje, że pojedyncza cząsteczka przewodnia, lsamp, pomaga zbudować i utrzymać brzuszne okablowanie nerwowe samca; gdy to okablowanie zawodzi, samiec nie jest w stanie dostarczyć wystarczająco silnego sygnału chemicznego, by w pełni dojrzały narządy rozrodcze samicy, a produkcja jaj drastycznie spada. Dzięki szczegółowemu zmapowaniu komórek pasożyta i odkryciu tego męskiego, specyficznego obwodu nerwowego praca ta wskazuje nowe sposoby blokowania składania jaj — oferując potencjalną strategię ograniczenia schistosomatozy w sytuacjach, gdy obecne leczenie opiera się na jednym, postarzałym leku.
Cytowanie: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Słowa kluczowe: schistosomiasis, single-cell transcriptomics, parasite reproduction, neural circuits, pheromone signaling