Clear Sky Science · pl
Mechanizm oporności SARS-CoV-2 na leki przeciwwirusowe oparte na analogach nukleotydów
Jak wirus przechytrza kluczowe leki przeciwwirusowe
Wirus wywołujący COVID-19 należy do rzadkiej grupy wirusów RNA, które potrafią korygować swój materiał genetyczny, dzięki czemu są wyjątkowo skuteczne w opieraniu się niektórym z naszych najlepszych leków przeciwwirusowych. W tym badaniu przeanalizowano szczegóły na poziomie atomowym, jak SARS‑CoV‑2 wykrywa i usuwa szeroko stosowaną klasę leków nazywanych analogami nukleotydów, wyjaśniając, dlaczego leki skuteczne przeciw innym wirusom często zawodzą w infekcjach koronawirusowych.
Walka o RNA wirusa
SARS‑CoV‑2 kopiuje swój genom RNA o długości ~30 000 zasad za pomocą dużego kompleksu molekularnego zwanego kompleksem replikacyjno‑transkrypcyjnym. W jego centrum znajduje się polimeraza zależna od RNA (RdRp), która buduje nowe nici RNA, oraz oddzielna jednostka — egzonukleaza (ExoN), która sprawdza poprawność i przycina błędy. Wiele doustnych leków przeciwwirusowych, w tym związki opracowane pierwotnie przeciw wirusowi zapalenia wątroby typu C, naśladuje naturalne składniki budulcowe RNA na tyle wiernie, że RdRp potrafi je włączyć, ale z subtelnymi modyfikacjami, które zatrzymują kopiowanie lub wprowadzają błędy. Niestety koronawirusy mają ExoN, który potrafi rozpoznać tych „oszustów” raz już włączonych do łańcucha RNA i wyciąć je, ratując replikację wirusa.
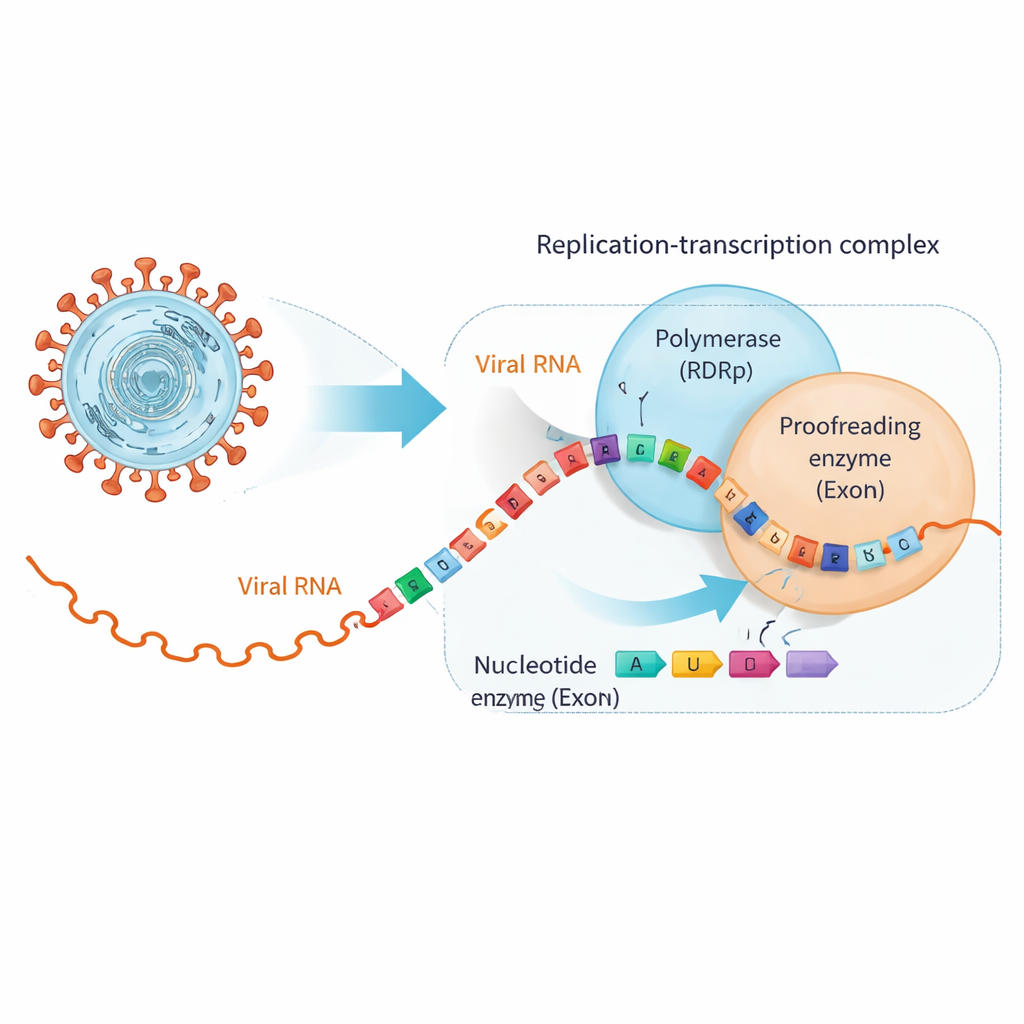
Kiedy pomocne leki zmieniają partnera RNA
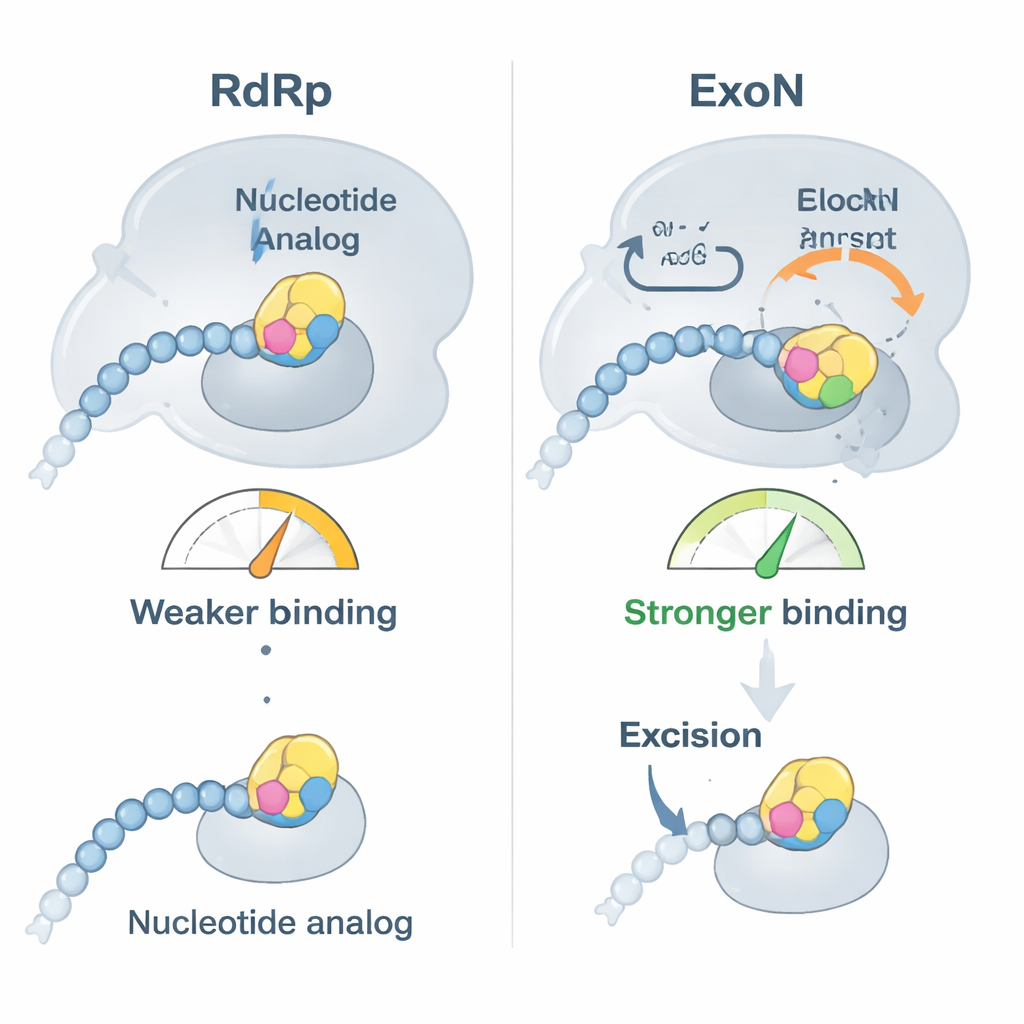
Naukowcy skoncentrowali się na dwóch klinicznie istotnych lekach przeciwwirusowych, bemnifosbuwirze i sofosbuwirze, zaprojektowanych jako wadliwe jednostki budulcowe RNA. Najpierw pokazali, że polimeraza SARS‑CoV‑2 chętnie włącza te analogi na końcu nici RNA i w dużej mierze przestaje dalej wydłużać łańcuch, zgodnie z zamierzeniem. Testy wiązania ujawniły jednak zaskakujący efekt: gdy analog znajduje się na końcu RNA, nić nie przyłącza się już tak mocno do polimerazy, lecz wiąże się silniej z ExoN. W praktyce zmodyfikowane lekiem RNA jest odsuwane od „maszyny kopiującej” i przekazywane do korektora, który następnie ma szansę odciąć problematyczny nukleotyd i umożliwić kontynuację replikacji.
Korekta, która jest spowolniona, lecz nie zatrzymana
Biochemiczne eksperymenty śledzące przebieg reakcji wykazały, że ExoN rzeczywiście usuwa bemnifosbuwir i sofosbuwir z RNA, ale wolniej niż normalne nukleotydy. W reakcjach pozakomórkowych oba analogi silnie blokowały dalszą syntezę RNA — jednak po dodaniu aktywnego ExoN znaczna część zatrzymanych łańcuchów RNA została ocalona i wydłużona. Mutant ExoN pozbawiony aktywności nie potrafił tego zrobić, co potwierdza, że aktywność korekcyjna odpowiada za cofnięcie dużej części efektu leków. Obecność polimerazy razem z ExoN faktycznie przyspieszała usuwanie analogów, co sugeruje, że oba wirusowe enzymy współpracują, aby usuwać przeszkody i utrzymywać replikację.
Obserwowanie korektora w rozdzielczości atomowej
Aby zrozumieć, jak ExoN rozpoznaje i reaguje na te leki, zespół wykorzystał krioelektronową mikroskopię o wysokiej rozdzielczości do rozwiązania struktur kompleksu ExoN związanych z nićmi RNA zakończonymi bemnifosbuwirem lub sofosbuwirem. Struktury — na tyle szczegółowe, że widać pojedyncze grupy chemiczne — ujawniły, że zmodyfikowane pierścienie cukrowe każdego leku mieszczą się w hydrofobowym kieszonkowym utworzonym przez krótką pętlę białka ExoN. To dodatkowe dopasowanie wyjaśnia mocniejsze wiązanie RNA zawierającego leki do ExoN. Ma to jednak nieoczekiwany skutek uboczny: pociągając tę pętlę, leki zaburzają precyzyjne ułożenie pobliskiej pętli katalitycznej, w której znajduje się kluczowe reszta histydyny. Kiedy ta histydyna odsuwa się od miejsca cięcia, centrum aktywne ExoN staje się częściowo zdezaktywowane, spowalniając, ale nie całkowicie uniemożliwiając usuwanie analogu.
Wbudowany przełącznik, który reguluje korektę wirusa
Mutacje pojedynczych aminokwasów w tej wrażliwej pętli potwierdziły jej znaczenie. Zmiany czterech zachowanych reszt znacząco zmniejszały zdolność ExoN do cięcia zarówno standardowych końców RNA, jak i końców zakończonych lekiem, a także zmieniały preferencję, który końcowy nukleotyd ExoN usuwa w pierwszej kolejności. Identyfikuje to pętlę jako regulator allosteryczny — wbudowany mechaniczny przełącznik, który wyczuwa, jaki nukleotyd znajduje się na końcu RNA, i dostosowuje aktywność enzymu. Struktury pokazują także, że ExoN rozpoznaje różne zasady (A, U, C lub G) przez elastyczne wiązania wodorowe, ale ma największe trudności z przyjęciem zasad podobnych do guaniny, co jest istotne, ponieważ bemnifosbuwir naśladuje guanozynę.
Co to oznacza dla przyszłych leków przeciw COVID‑19
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że SARS‑CoV‑2 ma zaawansowany „korektor błędów”, który potrafi wyciągnąć niektóre leki ze swojego genomu po tym, jak te leki zatrzymały replikację. Bemnifosbuwir i sofosbuwir osłabiają maszynerię kopiującą wirusa, ale jednocześnie kierują RNA ku korektorowi, który potrafi w znacznym stopniu cofnąć ich działanie. Poprzez ujawnienie, w jaki sposób wirusowy korektor chwyta te leki i jak niewielka pętelka regulacyjna przełącza enzym między stanem aktywnym a mniej aktywnym, praca ta dostarcza mapy drogowej do projektowania nowych nukleotydów przeciwwirusowych, które albo słabo wiążą się z ExoN, albo blokują go w nieaktywnej konformacji, albo wykorzystują jego trudności z obsługą struktur podobnych do guaniny. Takie kolejne generacje cząsteczek mogłyby być znacznie trudniejsze dla wirusa do „wymazania”, poprawiając nasze możliwości leczenia COVID‑19 i przyszłych epidemii koronawirusów.
Cytowanie: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Słowa kluczowe: SARS-CoV-2, oporność na leki przeciwwirusowe, analogi nukleotydów, korekta RNA, replikacja koronawirusa