Clear Sky Science · pl
Centralnie umieszczony skup wielokrotnych centrioli w komórkach prezentujących antygen sprzyja aktywacji limfocytów T
Jak komórki odpornościowe ustawiają swoją wewnętrzną kompas
Nasz układ odpornościowy opiera się na bliskiej „rozmowie” między dwoma kluczowymi graczami: komórkami dendrytycznymi, które prezentują fragmenty mikroorganizmów, oraz limfocytami T, które decydują, czy rozpocząć odpowiedź. Badanie to pokazuje, że drobny wewnętrzny „kompas” komórek dendrytycznych — struktura zbudowana z centrioli w centrum komórki — nie jest jedynie biernym elementem. Gdy ten kompas jest wzmocniony i precyzyjnie umieszczony, pomaga komórkom dendrytycznym skuteczniej aktywować limfocyty T, co ma znaczenie dla szczepionek, immunoterapii i leczenia nowotworów.
Maleńkie centrum organizujące komórki
Każda komórka zwierzęca zawiera centrum organizujące mikrotubule, zakotwiczone przez centriole — krótkie cylindry pełniące rolę zaczepów, z których wyrastają włókna strukturalne (mikrotubule). Te włókna kształtują wnętrze komórki i transportują ładunki, takie jak cząsteczki sygnałowe i pęcherzyki. Limfocyty T zwykle mają tylko jeden taki centrosom z dwiema centriolami. W przeciwieństwie do nich komórki dendrytyczne mogą tworzyć dodatkowe centrioli w miarę dojrzewania i kontaktu z materiałem obcym. Autorzy chcieli sprawdzić, czy te dodatkowe centrioli mają znaczenie dla jakości „rozmowy” komórek dendrytycznych z limfocytami T przez synapsę immunologiczną — strefę kontaktu, w której wymieniane są informacje i cząsteczki.
Rozbijanie i osłabianie wewnętrznego rusztowania
Aby zbadali rolę tego wewnętrznego rdzenia, zespół najpierw zakłócił funkcję centrioli lub mikrotubul w komórkach dendrytycznych myszy. Stosując lek blokujący tworzenie nowych centrioli, uzyskali komórki z niewielką liczbą lub bez centrioli, choć z pewnym pozostałym materiałem otaczającym wciąż zdolnym do nukleacji mikrotubul. Zmodyfikowane komórki potrafiły nadal formować włókna mikrotubularne, ale po zmieszaniu z naiwnymi limfocytami T powodowały znacznie mniejszą proliferację i aktywację tych komórek. 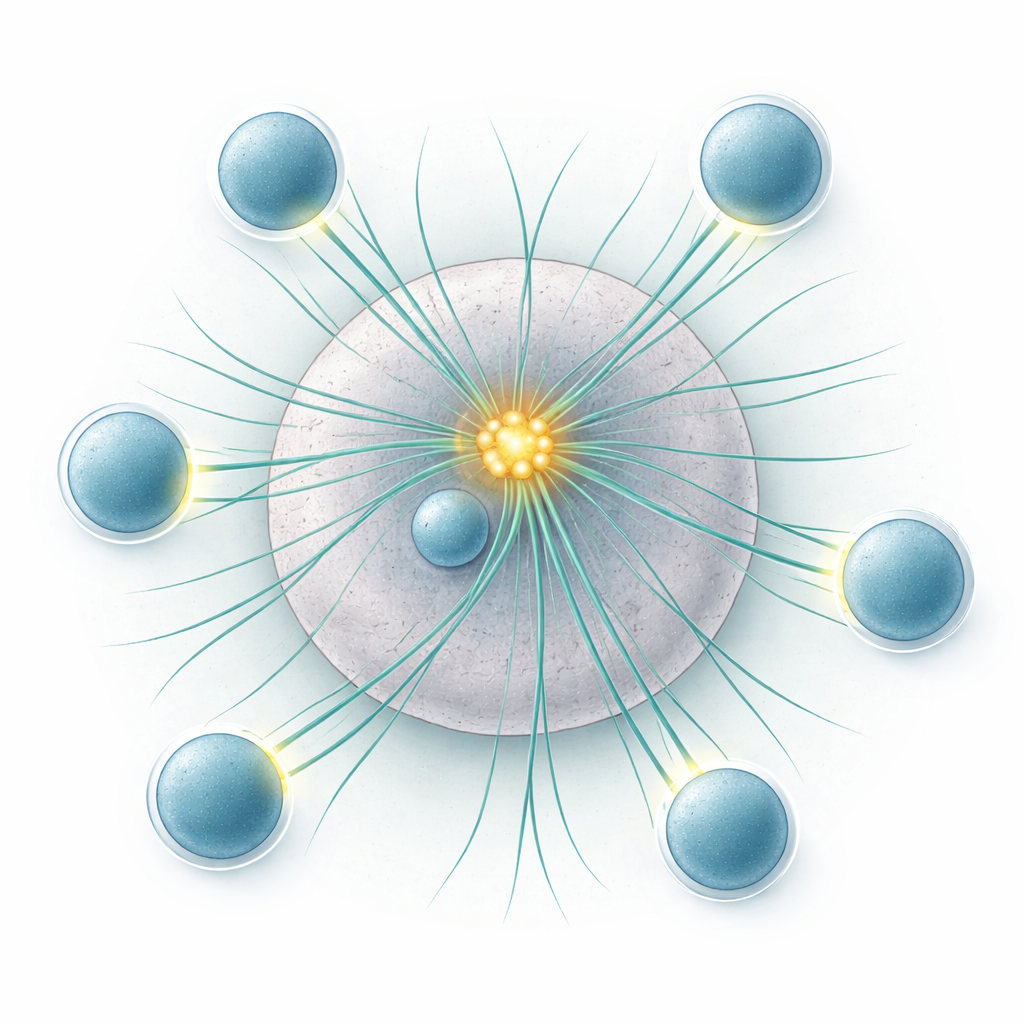
Dodatkowe centrioli jako wzmacniacz mocy
Autorzy zwrócili się następnie do komórek dendrytycznych, które naturalnie zawierają wiele centrioli. Stwierdzili, że dodatkowe centrioli rekrutują więcej białek inicjujących powstawanie mikrotubul, przekształcając pojedyncze centrum organizujące komórki w potężniejsze źródło włókien, bez zwiększania liczby oddzielnych centrów. Podczas kontaktów z limfocytami T komórki dendrytyczne z dodatkowymi centriolami wytwarzały gęstsze sieci mikrotubul, przy czym ich liczne centrioli pozostawały mocno skupione blisko geometrycznego środka komórki. Używając specjalnie zaprojektowanych limfocytów T, których fluorescencja raportuje siłę sygnalizacji receptora, zespół pokazał, że komórki dendrytyczne wzbogacone o wiele centrioli aktywowały więcej limfocytów T i robiły to szybciej niż komórki mające tylko dwie centrioli. Co ważne, te komórki dendrytyczne mogły jednocześnie angażować kilka limfocytów T, a zdolność wielokontaktowa nie zależała od liczby centrioli.
Dlaczego skupienie przewyższa rozproszenie
Zaskakująco, liczne centrioli w komórkach dendrytycznych nie rozchodziły się w kierunku każdego punktu styku z limfocytem T. Zamiast tego w hodowli i w węzłach chłonnych żywych myszy pozostawały zwarte w pobliżu jądra i środka komórki. Aby sprawdzić, czy to skupienie ma znaczenie, badacze użyli leku rozluźniającego kohezję centrioli bez zmiany kluczowych markerów powierzchniowych czy wydzielania cytokin. W tych warunkach centrioli rozchodziły się, tworząc wiele słabszych centrów organizujących i więcej miejsc powstawania mikrotubul rozrzuconych po komórce. Limfocyty T stykające się z takimi „odklastrowanymi” komórkami dendrytycznymi były aktywowane mniej efektywnie. To sugeruje, że istotne nie jest jedynie posiadanie większej liczby centrioli, lecz utrzymanie ich razem w odpowiednim miejscu.
Fizyka wyjaśnia optymalny punkt
Aby zrozumieć, dlaczego scentralizowany skup centrioli jest tak efektywny, zespół opracował modele matematyczne i komputerowe komórek dendrytycznych. Zadał pytanie: gdzie wewnątrz mniej więcej sferycznej komórki powinno się znaleźć centrum organizujące mikrotubule, aby zminimalizować średnią odległość do dowolnej potencjalnej synapsy na powierzchni? Ich obliczenia wykazały, że, biorąc pod uwagę obecność jądra, najlepsze miejsce to tuż nad powierzchnią jądra lub blisko geometrycznego środka komórki, w zależności od położenia jądra. Dynamiczne mikrotubule, które rosną i kurczą się z tego centralnego ośrodka, mogą wtedy szybciej osiągnąć dowolny punkt na powierzchni — przewaga „wyszukiwania i schwytania”. Gdy modelowali wiele niezależnych centrów organizujących rozproszonych po komórce, czas potrzebny mikrotubulom na znalezienie celu wzrastał. W przeciwieństwie do tego, skupienie kilku centrioli w jedno silne centrum i zwiększenie liczby mikrotubul konsekwentnie przyspieszało wychwytywanie celów.
Implikacje dla odporności i terapii
Mówiąc prosto, praca ta pokazuje, że komórki dendrytyczne działają bardziej jak efektywni kontrolerzy ruchu lotniczego, gdy ich liczne centrioli są zgrupowane w jasne, centralne centrum. To centrum uruchamia wiele „torów” mikrotubularnych, które szybko dostarczają sygnały stymulujące do limfocytów T wokół powierzchni komórki. Zakłócenie integralności tego centrum lub rozproszenie jego składników spowalnia to dostarczanie i osłabia aktywację limfocytów T. Poza wyjaśnieniem subtelnej warstwy organizacji komórek odpornościowych, wyniki te przecinają się z badaniami nad rakiem, gdzie testuje się leki rozbijające skupienie centrioli w celu zabicia komórek nowotworowych. Badanie ostrzega, że takie strategie mogą także osłabić odpowiedź immunologiczną, jeśli przypadkowo wpłyną na komórki prezentujące antygen, i wskazuje na amplifikację oraz pozycjonowanie centrioli jako potencjalne dźwignie do precyzyjnego dostrajania szczepionek i immunoterapii. 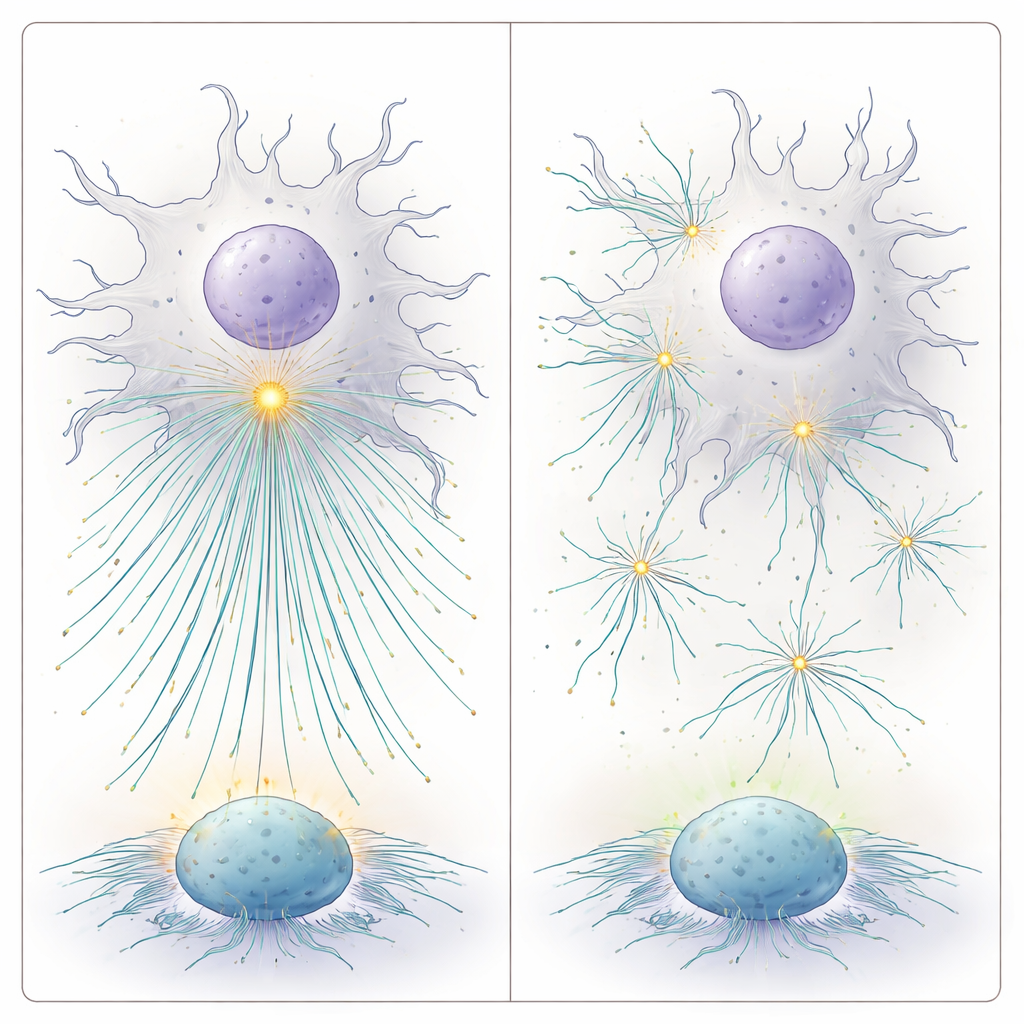
Cytowanie: Stötzel, I., Weier, AK., Sarkar, A. et al. A centrally positioned cluster of multiple centrioles in antigen-presenting cells fosters T cell activation. Nat Commun 17, 536 (2026). https://doi.org/10.1038/s41467-026-68286-7
Słowa kluczowe: komórki dendrytyczne, aktywacja limfocytów T, centrosomy, mikrotubule, synapsa immunologiczna