Clear Sky Science · pl
Warianty de novo w genie czynniku splicingowym SF3B1 są związane z zaburzeniami neurorozwojowymi
Kiedy jeden gen zaburza wczesny plan mózgu
Dlaczego niektóre dzieci rozwijają trudności w nauce, napady padaczkowe czy problemy z karmieniem, mimo że ciąża i poród przebiegały prawidłowo? Badanie to przygląda się jednemu genowi, SF3B1, który pomaga komórkom przetwarzać genetyczne informacje. Autorzy pokazują, że nowe, spontaniczne zmiany w tym genie mogą subtelnie zaburzać sposób odczytywania instrukcji DNA przez komórki mózgu, prowadząc do wcześniej niepoznanego zespołu neurorozwojowego.
Mistrzowski redaktor wiadomości genetycznych
Każda komórka w naszym ciele musi przekształcić surowy zapis genetyczny w zrozumiałe instrukcje, zanim będzie mogła wytworzyć białka. Ten etap edycji, zwany składaniem RNA (RNA splicing), usuwa niekodujące odcinki i łączy użyte fragmenty. SF3B1 jest centralnym elementem komórkowej „maszyny splicingowej”. Dotychczas zmiany w SF3B1 były głównie rozpoznawane w kontekście nowotworów, gdzie komórki nowotworowe nabywają mutacje w tym genie w trakcie życia. Nowe badanie stawia inne pytanie: co się dzieje, gdy uszkadzająca zmiana w SF3B1 obecna jest od poczęcia we wszystkich komórkach organizmu?
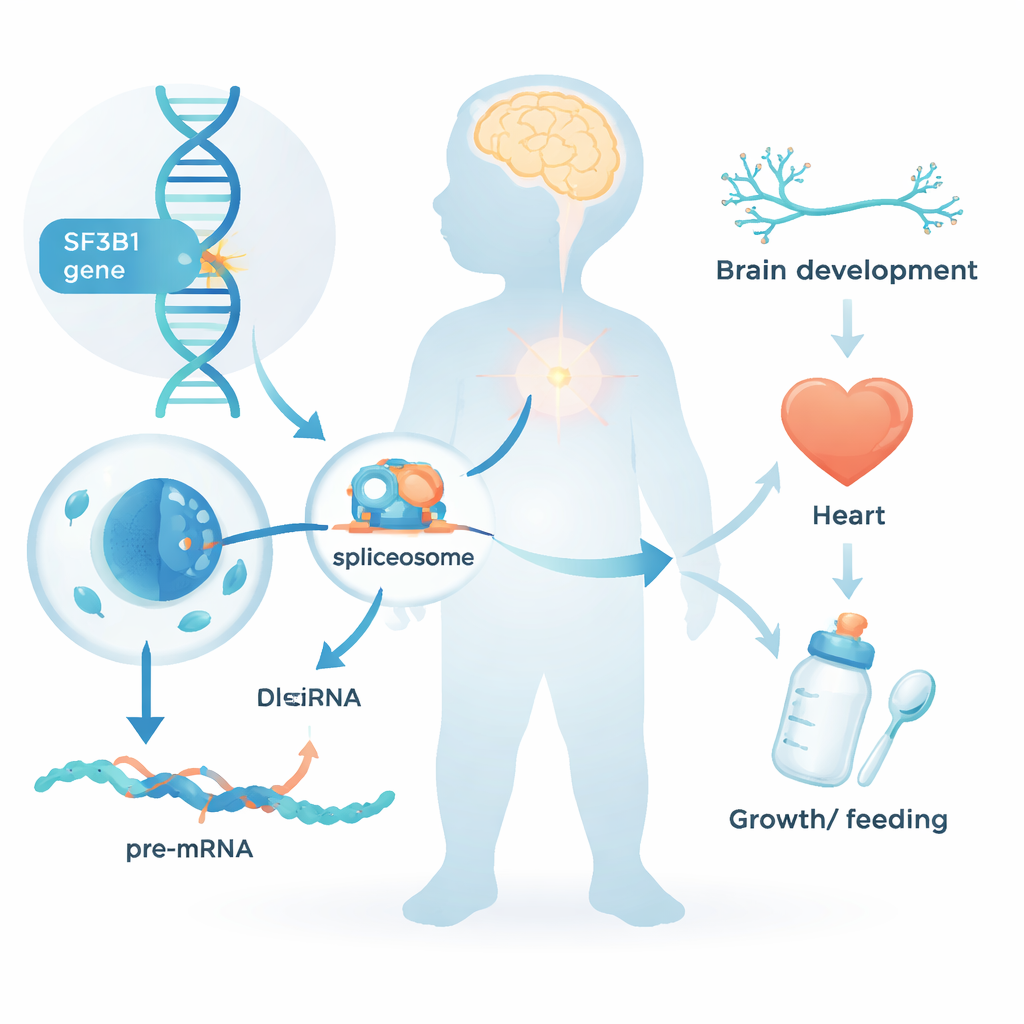
Nowo rozpoznany zespół dziecięcy
Zespół zebrał dane od 26 dzieci i młodych dorosłych, którzy wszyscy mieli rzadkie warianty SF3B1, w większości powstające de novo — to znaczy nie odziedziczone od żadnego z rodziców. Niemal wszyscy mieli problemy neurorozwojowe: opóźnienia w nauce siadania, chodzenia czy mówienia; niepełnosprawność intelektualną przeważnie łagodną do umiarkowanej; a u około połowy przypadków występowały napady padaczkowe. Wiele osób miało obniżone napięcie mięśniowe i wymagało dodatkowej pomocy przy karmieniu, czasem przez sondę żołądkową. Cechy twarzy były subtelnie nietypowe, choć nie identyczne u poszczególnych dzieci; wyraźnie częstym znakiem był wysoki lub rozszczepiony podniebienie. Kilku uczestników miało także wady serca, zahamowanie wzrostu lub małą głowę, co pokazuje, że skutki zmian w SF3B1 wykraczają poza mózg.
Dwie klasy zmian genetycznych, dwa wzorce kliniczne
Naukowcy rozróżnili dwie szerokie kategorie wariantów SF3B1. Do jednej grupy zaliczono zmiany prowadzące do „utraty funkcji”, takie jak przedwczesne sygnały stop, które prawdopodobnie zmniejszają ilość funkcjonalnego białka SF3B1. Druga grupa obejmowała warianty missensowne, w których pojedynczy aminokwas w białku jest zmieniony. Poprzez grupowanie cech klinicznych dzieci zespół zaobserwował, że pacjenci z wariantami missensownymi mieli tendencję do cięższych i bardziej złożonych problemów, w tym wyższej częstości wad serca i przewodu pokarmowego, niskiego wzrostu i mikrocefalii. Wariantu utraty funkcji natomiast czasem dziedziczyły osoby z łagodnymi objawami lub nawet pozornie zdrowi rodzice, co sugeruje, że po prostu mniejsza ilość SF3B1 może u niektórych osób wiązać się z relatywnie łagodnymi objawami.
Błędy w dopracowaniu zamiast całkowitej awarii
Aby zrozumieć, co warianty missensowne robią w komórkach, naukowcy odtworzyli je w liniach komórkowych w laboratorium. Ku zaskoczeniu, zmienione białka SF3B1 wciąż potrafiły wykonać podstawowe zadanie splicingu wystarczająco dobrze, by uratować komórki, w których normalne SF3B1 zostało wyciszone. Wykluczyło to proste wyjaśnienie typu utraty funkcji. Przy użyciu głębokiego sekwencjonowania RNA zespół przeanalizował całe spektrum komunikatów komórkowych. Stwierdzili, że warianty missensowne subtelnie przesuwają splicing setek genów, zwłaszcza przez zmianę wyboru miejsc splicingu na końcach eksonów i przez sporadyczne pomijanie eksonów. Skala zaburzeń była mniejsza niż w przypadku klasycznej mutacji SF3B1 związanej z rakiem (K700E), ale wciąż istotna: wiele dotkniętych genów bierze udział w rozwoju mózgu, łączeniu nerwów oraz w podstawowych procesach, takich jak obróbka RNA i synteza białek.
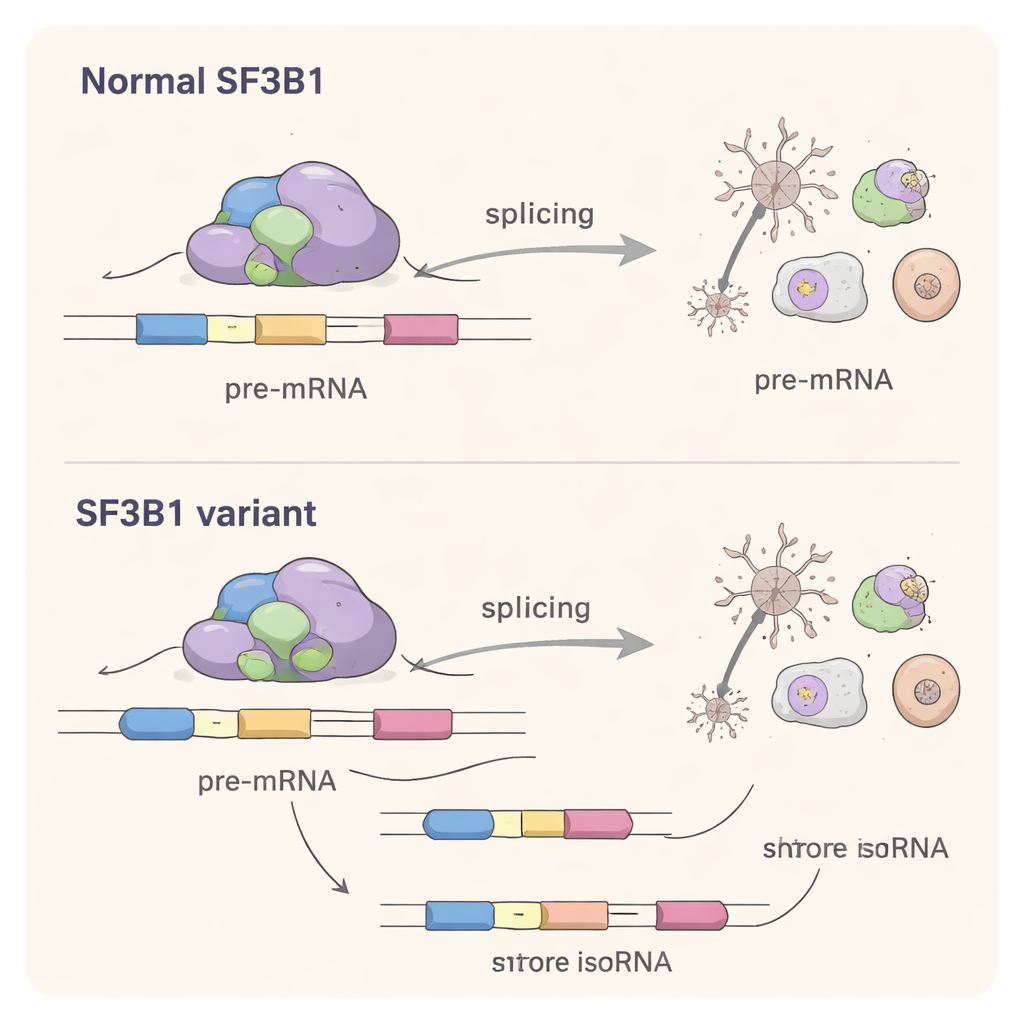
Wspólny mechanizm między rakiem a zaburzeniami mózgu
Chociaż większość wariantów SF3B1 związanych z zaburzeniami neurorozwojowymi występuje w innych miejscach niż dobrze znane mutacje rakowe, zakłócają one ten sam zasadniczy proces: precyzyjne rozpoznawanie miejsc splicingu w RNA. Badanie pokazuje, że te rozwojowe warianty mają własny „podpis splicingu”, wybierając alternatywne miejsca splicingu, które często są bliżej normalnych miejsc niż te preferowane w raku. Sugeruje to mechanizm zmiany funkcji, w którym zmutowane białko konkuruje z kopią normalną i skłania maszynerię splicingową do wielokrotnie nieco błędnych wyborów w wielu genach jednocześnie.
Co to oznacza dla rodzin i przyszłych badań
Dla dotkniętych rodzin praca ta identyfikuje SF3B1 jako nową przyczynę zaburzeń neurorozwojowych, którą można teraz badać w poradniach genetycznych, potencjalnie kończąc długie poszukiwania diagnozy. Szerzej rzecz biorąc, dodaje SF3B1 do niewielkiej, lecz rosnącej listy genów splicingowych, których zmiany mogą powodować zarówno nowotwory, jak i dziecięce zaburzenia mózgu, w zależności od tego, kiedy i jak gen ulega zmianie. Mapując, jak konkretne warianty SF3B1 przekształcają splicing RNA, badanie tworzy podstawy pod przyszłe terapie ukierunkowane na korygowanie nieprawidłowego splicingu.
Cytowanie: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Słowa kluczowe: splicing RNA, SF3B1, zaburzenia neurorozwojowe, warianty de novo, spliceosomopatie