Clear Sky Science · pl
Wiskozelastyczny hydrożel aktywujący makrofagi z CAR do leczenia włóknienia płuc
Przekształcanie „sprzątaczy” ciała w precyzyjne zespoły naprawcze
Włóknienie płuc to wyniszczająca choroba, w której normalna, elastyczna tkanka płucna stopniowo zostaje zastąpiona sztywną blizną. Ludzie mają trudności z oddychaniem, a dostępne dziś leki przeważnie jedynie hamują postęp. W tym badaniu badacze proponują nowe podejście: przekształcenie własnych komórek sprzątających organizmu, makrofagów, w zaprojektowane „inteligentne sprzątaczki” i wzmocnienie ich działania za pomocą specjalnie zaprojektowanego miękkiego hydrożelu. W połączeniu te zabiegi pomagają komórkom tropić sprawców tworzących blizny, a nawet rozluźniać usztywnioną tkankę w uszkodzonych płucach.
Kiedy gojenie szkodzi
W zdrowych płucach fibroblasty pomagają utrzymać delikatną sieć kolagenu podtrzymującą pęcherzyki płucne. W włóknieniu płuc te komórki stają się nadaktywne i odkładają grube włókna kolagenu, które zatykają przestrzenie powietrzne. Istniejące leki mogą tłumić te procesy, ale rzadko je odwracają. Autorzy skupiają się na markerze powierzchniowym zwanym białkiem aktywacji fibroblastów (FAP), które jest obficie obecne na nadaktywnych fibroblastach, ale rzadkie w tkance normalnej. Gdyby komórki odpornościowe można było wyszkolić do rozpoznawania FAP, mogłyby selektywnie usuwać „uciekające” fibroblasty napędzające bliznowacenie, oszczędzając zdrowe sąsiedztwo.
Reprogramowanie makrofagów do ataku na budowniczych blizn
Makrofagi to patrolujące komórki odpornościowe, które normalnie pochłaniają martwe komórki, mikroby i szczątki komórkowe. Zespół wyposażył je w chimeryczny receptor antygenowy (CAR) rozpoznający FAP, tworząc makrofagi CAR (CAR‑M). W hodowlach laboratoryjnych te CAR‑M skutecznie połykały fibroblasty bogate w FAP i je zabijały, podczas gdy w dużej mierze ignorowały komórki o obniżonej ekspresji FAP. Również intensywniej degradowały żelowe matryce bogate w kolagen niż niemodyfikowane makrofagi, co sugeruje podwójną korzyść: eliminację komórek tworzących blizny i bezpośrednie rozkładanie matrycy bliznowatej. Efekty te obserwowano zarówno w liniach komórkowych, jak i w pierwotnych makrofagach mysich, które lepiej odzwierciedlają sytuację tkankową. 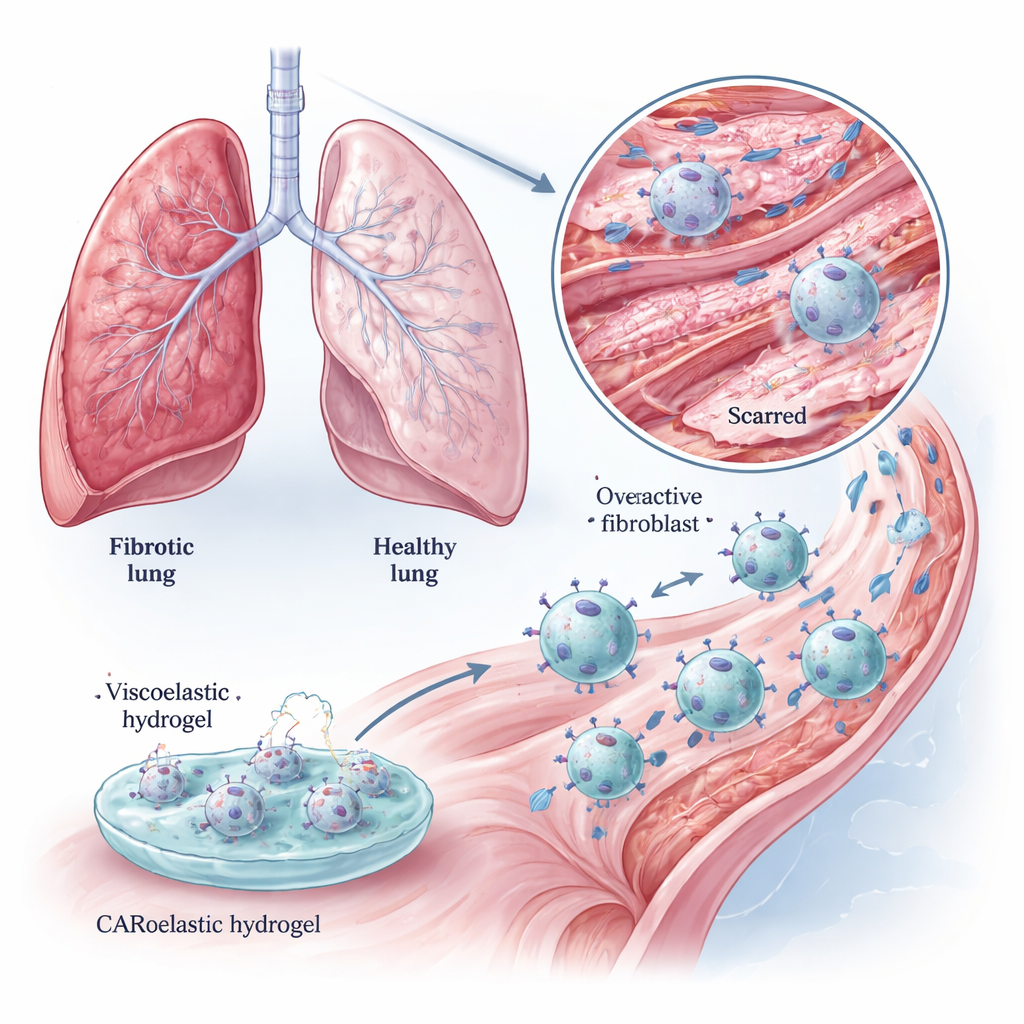
Aktywacja komórek odpornościowych miękkim, wiskozelastycznym żelem
Genetyczne modyfikowanie komórek jest potężne, ale złożone. Naukowcy zastanowili się więc, czy czysto fizyczny sygnał — miękki, wiskozelastyczny hydrożel — może dodatkowo stuningować zachowanie CAR‑M. Zbudowali hydrożel z żelatyny i alginianu, którego „moduł utraty”, miara tego, jak żel relaksuje się pod obciążeniem z upływem czasu, można było precyzyjnie regulować bez zmiany ogólnej sztywności. Gdy CAR‑M krótko inkubowano na żelach o odpowiedniej wiskozelastyczności, ich zdolność do zabijania celów‑fibroblastów wzrastała bardziej niż po zastosowaniu powszechnych stymulatorów chemicznych, a wzmocnienie utrzymywało się co najmniej przez dwa dni. Te „Gel‑CAR‑M” aktywowały też geny związane z odpowiedzią immunologiczną i przebudową tkanki, jednocześnie wyciszając geny powiązane z fibrozą, sugerując, że doświadczenie żelu odcisnęło na komórkach bardziej antybliznowy profil.
Jak miększa powierzchnia przebudowuje zachowanie komórek
Aby zrozumieć, dlaczego żel miał znaczenie, zespół zbadał stan fizyczny receptorów CAR na powierzchni komórki. Fluorescencyjny znacznik wykazał, że CAR‑M przygotowane na hydrożelu miały niższe napięcie błony — zewnętrzna „skóra” komórki była bardziej rozluźniona. W tych warunkach cząsteczki CAR rozpraszały się z ciasnych klastrów na bardziej izolowane pojedyncze jednostki i pary. Testy biochemiczne pokazały, że te rozproszone receptory faworyzowały formy bardziej skłonne do wywołania sygnalizacji wewnątrzkomórkowej, w szczególności w szlakach takich jak ERK, które kontrolują aktywację i zdolność do zabijania. Naśladowanie obniżenia napięcia małą cząsteczką reprodukowało to samo rozprzestrzenianie receptorów i poprawę zabijania komórek docelowych, co wspiera hipotezę, że mechaniczne rozluźnienie błony wystarcza, by „wstępnie uzbroić” komórki zanim spotkają swoje cele. 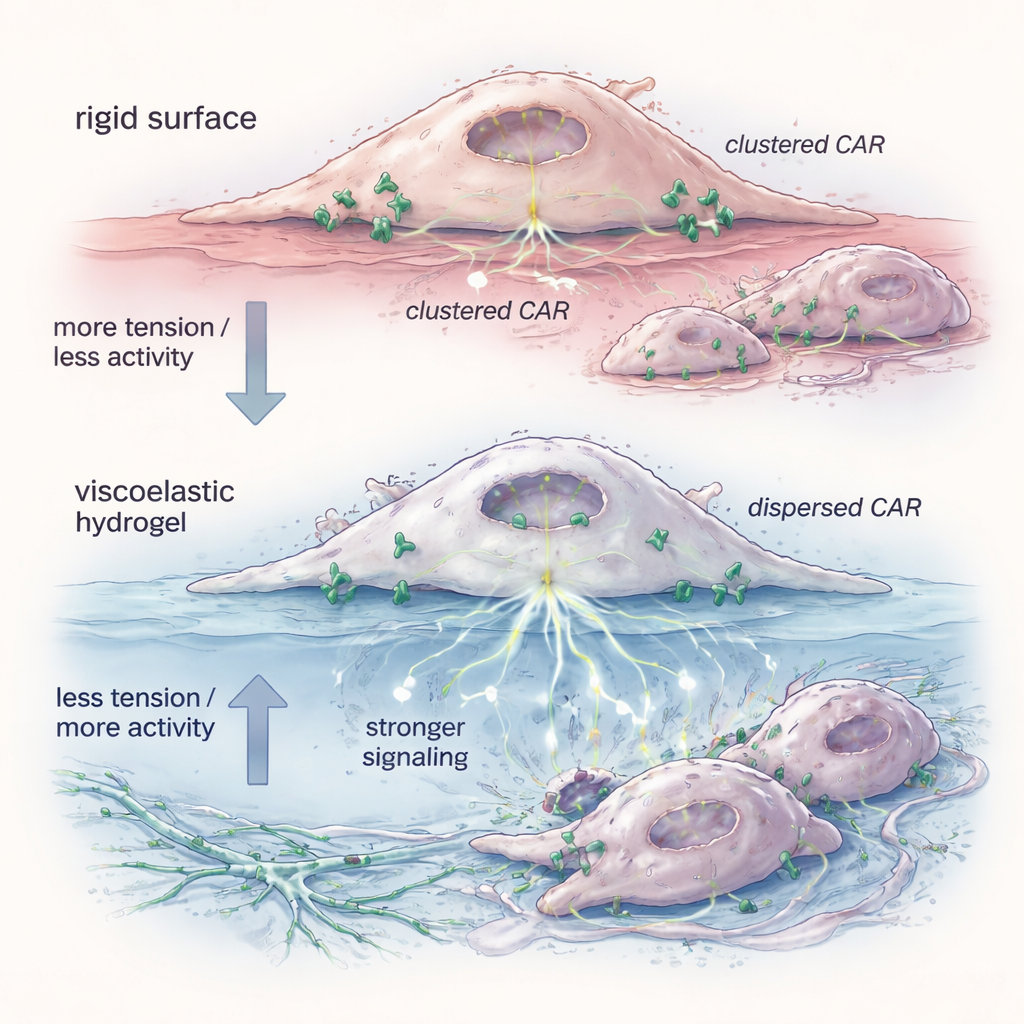
Naprawa zbliznowaciałych płuc u myszy
Ostatecznym testem był model myszy z farmakologicznie wywołanym włóknieniem płuc. Zwierzęta otrzymały albo zwykłe makrofagi, standardowe CAR‑M, albo hydrożelem aktywowane Gel‑CAR‑M. Wszystkie leczone myszy poprawiły się w porównaniu z nieleczonymi kontrolami, ale Gel‑CAR‑M wypadły najlepiej: ich płuca zawierały mniej kolagenu, więcej normalnych przestrzeni powietrznych i mniej fibroblastów pozytywnych na FAP. Analizy genetyczne tkanki płucnej wykazały, że Gel‑CAR‑M skuteczniej uspokajały sygnalizację zapalną i obniżały ekspresję genów związanych z bliznowaceniem niż standardowe CAR‑M. Śledzone komórki utrzymywały się w płucu co najmniej przez tydzień, a rozszerzone badania bezpieczeństwa przez 12 tygodni nie wykazały istotnych uszkodzeń narządów, nieprawidłowości we krwi ani oznak autoimmunizacji.
Nowy kierunek terapii komórkowych przeciw fibrozom
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że połączenie ukierunkowanej inżynierii komórek i inteligentnych materiałów może przekształcić wrodzone komórki odpornościowe w wysoce skuteczne, a jednocześnie niezbyt genetycznie skomplikowane narzędzia przeciw bliznom. Krótko umieszczając zmodyfikowane makrofagi na starannie dostrojonym miękkim żelu, naukowcy mechanicznie „ustawili” ich receptory powierzchniowe w bardziej reagującym trybie. U myszy z włóknieniem płuc przełożyło się to na lepsze usuwanie szkodliwych fibroblastów, rozkład nadmiaru kolagenu i częściową odbudowę normalnej struktury płuc — bez widocznych problemów bezpieczeństwa. Choć przed badaniami u ludzi wciąż wiele pracy, ta strategia sugeruje, że precyzyjne dostrajanie fizycznego otoczenia komórek terapeutycznych może kiedyś uczynić leczenie chorób włóknieniowych płuc bardziej skutecznym i precyzyjnym.
Cytowanie: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Słowa kluczowe: włóknienie płuc, terapia makrofagami CAR, wiskozelastyczny hydrożel, białko aktywacji fibroblastów, mechanobiologia komórkowa