Clear Sky Science · pl
Podstawa molekularna hamowania de novo metylacji DNA przez TCL1A
Jak komórki decydują, co zapamiętać
Każda komórka w twoim ciele zawiera zasadniczo tę samą sekwencję DNA, a jednak komórki mózgowe, krwi i skóry zachowują się bardzo różnie. Jednym ze sposobów, w jaki komórki „zapamiętują” swoją tożsamość, są chemiczne znaczniki dodawane do DNA — proces zwany metylacją DNA. W tym badaniu ujawniono, z atomową szczegółowością, jak niewielkie białko TCL1A może wyłączyć enzymy, które nanoszą te metylowe znaczniki. Ponieważ zarówno metylacja DNA, jak i TCL1A wiążą się z nowotworami i zaburzeniami rozrodu, zrozumienie tego molekularnego przeciągania liny może w przyszłości zainspirować nowe terapie.
Maszyneria znakowania DNA w komórce
Metylacja DNA działa jak ołówkowa kreska na marginesie genomu — pomaga wyciszać niektóre geny i stabilizować genom w trakcie rozwoju komórek. Dwa enzymy, DNMT3A i DNMT3B, są głównymi „pisarzami”, które umieszczają nowe znaczniki metylowe podczas wczesnego rozwoju i gdy komórki macierzyste się wyspecjalizowują. Gdy te enzymy są zmutowane lub źle regulowane, wzory znaków DNA mogą zostać pomieszane, co przyczynia się do zespołów rozwojowych i nowotworów krwi. TCL1A to białko najbardziej znane z roli w nowotworach komórek odpornościowych, gdzie bywa nadmiernie wytwarzane. Wcześniejsze prace sugerowały, że TCL1A może wiązać DNMT3A i DNMT3B i tłumić ich aktywność, ale nie było wiadomo, w jaki sposób dokładnie dochodzi do tego blokowania.
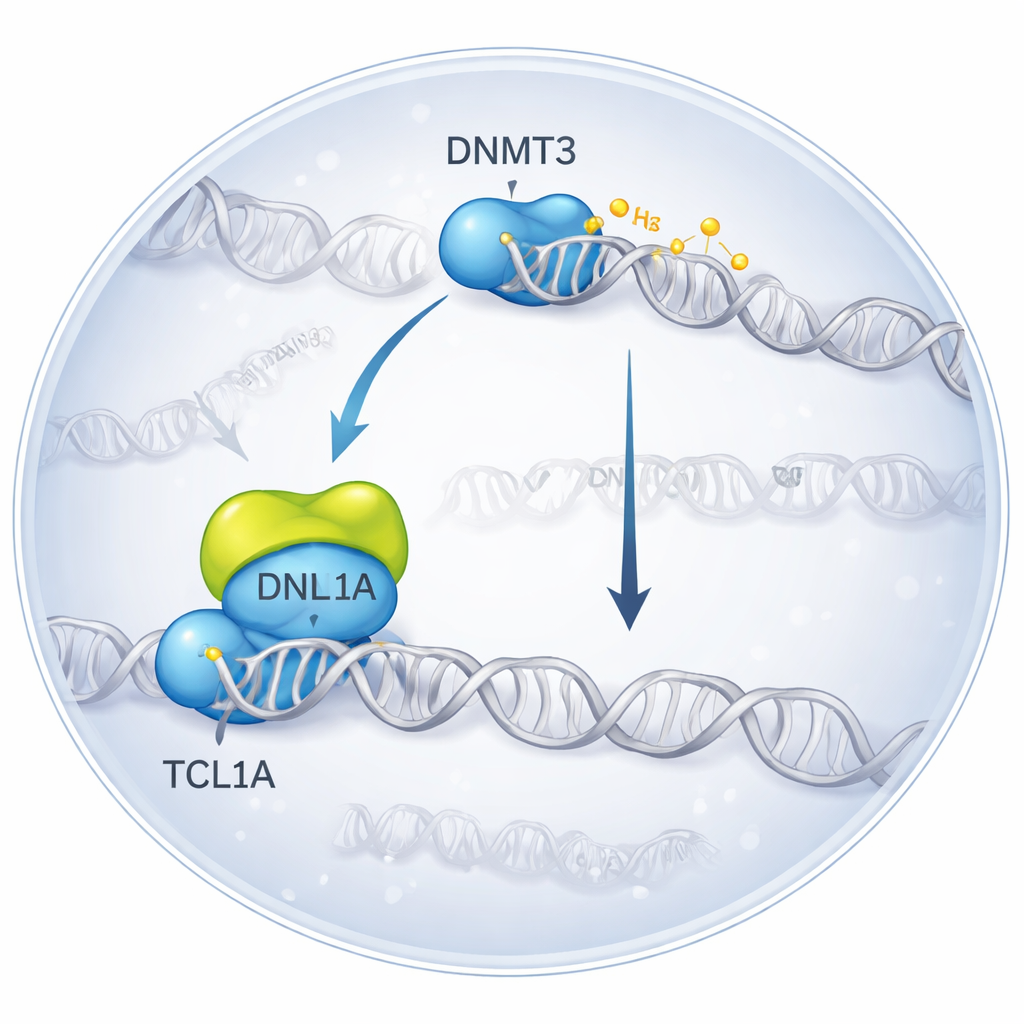
Zatrzymanie molekularnego spotkania w 3D
Naukowcy użyli krio‑elektronowej mikroskopii — techniki obrazowania błyskowo zamrożonych cząsteczek — aby zobrazować kompleks powstały, gdy DNMT3A wiąże TCL1A. Stwierdzili, że dwa cząsteczki DNMT3A łączą się w parę, a po każdej stronie na katalityczną część DNMT3A dokuje dimer TCL1A — właśnie ta część, która normalnie współdziała z białkami pomocniczymi i z DNA. Powierzchnia wiązania pokrywa się z miejscem, gdzie zwykle przyczepia się inny partner, DNMT3L, aby wzmocnić aktywność DNMT3A. W testach biochemicznych dodanie TCL1A silnie zmniejszało zdolność zarówno DNMT3A, jak i DNMT3B do metylowania DNA, nawet w obecności DNMT3L, co potwierdza, że opisana struktura odpowiada silnie zahamowanemu stanowi.
Zmiana kształtu, która zatyka enzym
Badając szczegóły, zespół zauważył, że wiązanie TCL1A nie polega jedynie na przykryciu miejsca aktywnego jak pokrywka. Zamiast tego powoduje subtelną, lecz szeroko zakrojoną zmianę konformacji DNMT3A. Dwa elastyczne regiony enzymu, znane jako pętla rozpoznająca cel i pętla katalityczna, odchylają się od pozycji, które zajmują, gdy DNMT3A jest związany z DNA. W aktywnej formie pętle te przylegają do DNA i tworzą kieszeń dla małej cząsteczki paliwa o nazwie SAM, która donoruje grupę metylową. Po przyłączeniu TCL1A pętla katalityczna składa się wewnątrz kieszeni SAM i ją zatyka, jednocześnie utrudniając DNA dostęp do enzymu. Pomiar wiązania potwierdził, że DNMT3A w kompleksie z TCL1A nie potrafi wykrywalnie chwytać ani DNA, ani SAM.
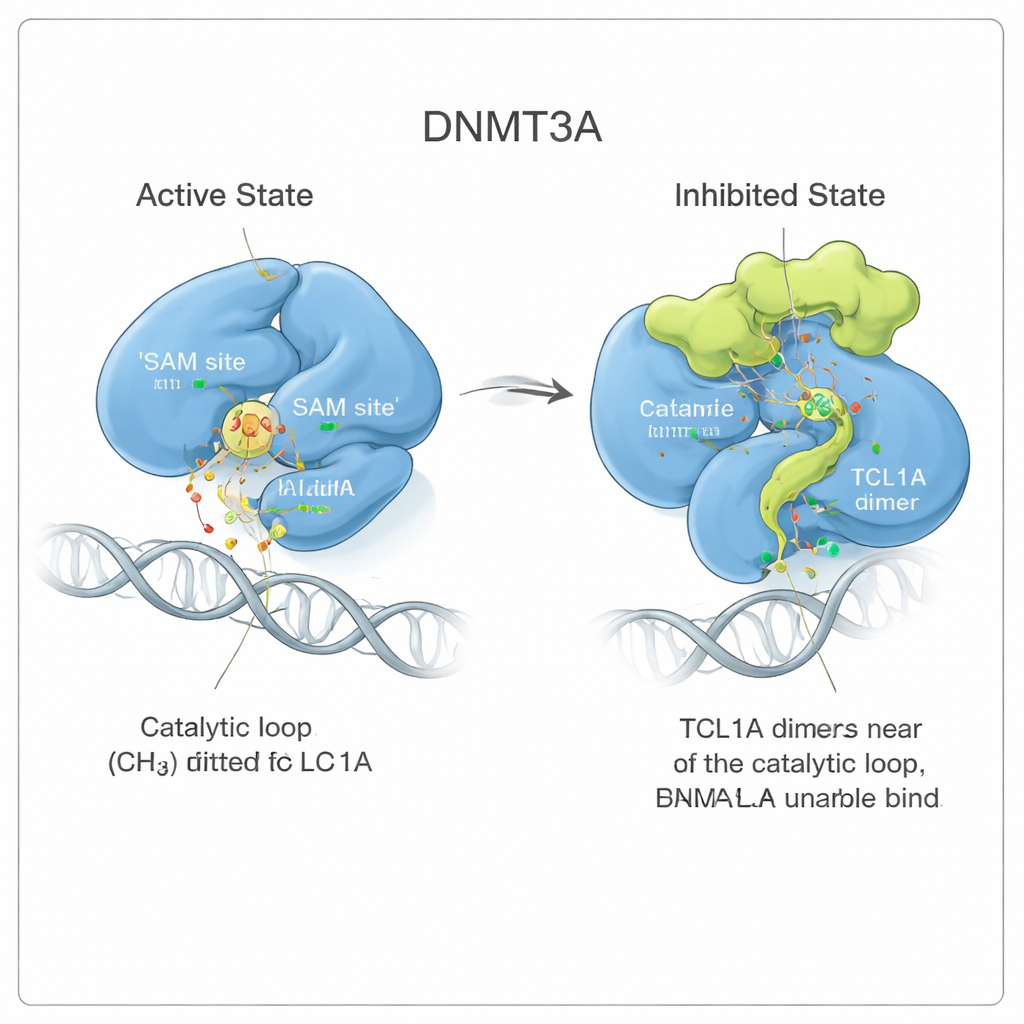
Obserwowanie dynamicznej blokady w ruchu
Aby zrozumieć, jak stabilna jest ta zahamowana konformacja, autorzy przeprowadzili długie symulacje dynamiki molekularnej — w istocie filmy oparte na fizyce przedstawiające cząsteczki w roztworze. Gdy DNMT3A był związany ze swoim aktywatorem DNMT3L, pętla katalityczna pozostawała w ciasnej, aktywnej pozycji. W obecności TCL1A ta pętla stała się znacznie bardziej ruchoma, wymachując, ale wielokrotnie zajmując kieszeń SAM jak wodorosty wirujące i mimo to zatykały odpływ. Ten ciągły ruch zmniejszał dostępne miejsce dla SAM ponad dziesięciokrotnie, wspierając model, w którym TCL1A wykorzystuje naturalną elastyczność DNMT3A, aby narzucić dynamiczną, a nie sztywną formę hamowania.
Konsekwencje dla komórek rozwijających się i chorób
Następnie zespół zapytał, co ta molekularna blokada oznacza dla rzeczywistych komórek. Zmodyfikowali mysie embrionalne komórki macierzyste tak, by produkowały ludzkie TCL1A w stadium, gdy komórki normalnie zwiększają metylację DNA podczas rozpoczynania różnicowania. Mapowanie metylacji w skali genomu wykazało, że komórki nadprodukujące TCL1A nie osiągały zwykłego wysokiego poziomu metylacji DNA, co bardzo przypominało komórki, u których jednocześnie wyłączono geny Dnmt3a i Dnmt3b. Mutant TCL1A, który słabo wiąże enzymy DNMT3, miał niewielki efekt, podkreślając, że kluczowe jest fizyczne oddziaływanie. Te ustalenia łączą mechanizm strukturalny z szerokimi zmianami epigenetycznymi w całym genomie.
Co to oznacza dla zdrowia
W sumie praca ujawnia, jak TCL1A może działać jako potężny hamulec dla enzymów nanoszących nowe markery metylacyjne DNA. Dokując w krytycznym interfesie, TCL1A przestawia elastyczne pętle w DNMT3A i DNMT3B tak, że nie mogą one już wiązać nici DNA ani chemicznego paliwa, prowadząc do globalnej utraty znaczników metylowych w komórkach. W normalnym rozwoju ten rodzaj precyzyjnej kontroli może pomagać w regulacji kiedy i gdzie metylacja jest dodawana. Gdy TCL1A jest niewłaściwie zlokalizowane lub nadmiernie produkowane, jak w niektórych nowotworach krwi i rzadkich zaburzeniach rozrodczych, ten sam mechanizm może zafałszować program epigenetyczny komórki. Zrozumienie tego oddziaływania na poziomie atomowym otwiera drogę do projektowania cząsteczek naśladujących lub przeciwdziałających efektom TCL1A, co potencjalnie pozwoli przywrócić zdrowe wzorce metylacji DNA.
Cytowanie: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Słowa kluczowe: metylacja DNA, DNMT3A, TCL1A, epigenetyka, nowotwór