Clear Sky Science · pl
Przykładowe metody podawania próbek w krystalografii rentgenowskiej białek ze szczególnym uwzględnieniem zużycia próbki
Obserwowanie cząsteczek w działaniu
Krystalografia rentgenowska pozwala naukowcom zobaczyć ułożenie atomów w białkach — maleńkich maszyn napędzających życie. Nowsze podejście, zwane krystalografią seryjną, idzie o krok dalej: potrafi uchwycić „molekularne filmy” białek w działaniu, na przykład enzymów przetwarzających lek lub białek fotosyntetycznych rozszczepiających wodę. Jest jednak pewien problem. Wiele ważnych białek trudno jest wytworzyć i zkrystalizować, a obecne eksperymenty mogą zużywać od miligramów do gramów cennego materiału. Niniejszy przegląd zadaje pozornie proste pytanie: jak wprowadzić kryształy w silne wiązki rentgenowskie, marnując przy tym jak najmniej próbki?
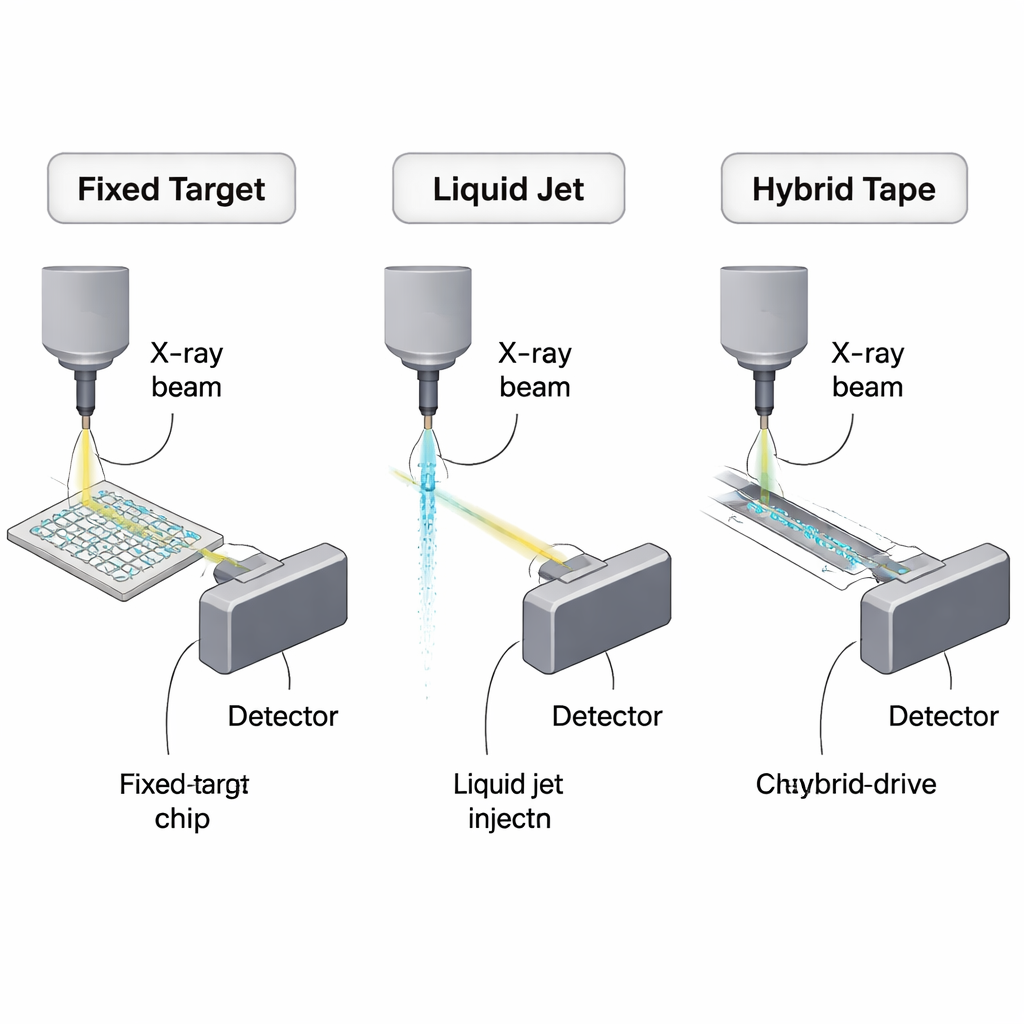
Dlaczego krystalografia seryjna potrzebuje lepszych metod podawania
Tradycyjna krystalografia polegała na pojedynczym dużym krysztale obracanym w wiązce rentgenowskiej. Krystalografia seryjna odwraca ten scenariusz: zamiast jednego dużego kryształu używa się tysięcy mikrokryształów, z których każdy jest użyty tylko raz i przepuszczany lub skanowany przez ultrajaskrawe impulsy rentgenowskie ze synchrotronów lub rentgenowskich laserów swobodnego elektronu (XFEL). Pozwala to na zbieranie danych w temperaturze pokojowej i szybkie „migawki” reakcji chemicznych, ale oznacza też konieczność stałego uzupełniania kryształów w tempie odpowiadającym seriom impulsów rentgenowskich, które mogą osiągać do milionów impulsów na sekundę. Większość zawiesiny kryształów nigdy nie trafia w wiązkę i jest odrzucana, dlatego zmniejszenie zużycia próbki stało się kluczowym wyzwaniem technicznym i ekonomicznym w tej dziedzinie.
Stałe cele: maleńkie chipy, które wykorzystują każdą kroplę
Jedną z głównych strategii jest unieruchomienie mikrokryształów na małych, stałych nośnikach zwanych stałymi celami. Zamiast rozpylania kryształów przez wiązkę, badacze rozmieszczają je w układach na krzemowych lub polimerowych chipach i przesuwają chip tak, aby każdy kryształ znalazł się w ognisku rentgenowskim tylko raz. W myślowym eksperymencie idealnym około 10 000 mikrokryształów modelowego białka mogłoby w zasadzie dostarczyć kompletnego zbioru danych przy użyciu jedynie około 450 nanogramów białka. Rzeczywiste urządzenia nie są jeszcze tak oszczędne, ale już redukują zapotrzebowanie do dziesiątek mikrogramów lub kilkuset mikrogramów — o rzędy wielkości lepiej niż wczesne eksperymenty seryjne. Przegląd porównuje siatki krzemowe, ultracienkie folie polimerowe i wielowarstwowe plastikowe chipy, oceniając ich zalety (niskie rozpraszanie tła, wzrost kryształów na chipie, zgodność z badaniami w temperaturze pokojowej) wobec praktycznych problemów, takich jak odwodnienie, niepożądane rozpraszanie od materiału chipu oraz dodatkowa „martwa objętość” wprowadzana przez ręczne pipetowanie.
Strumienie ciekłe i lepkie: szybkie, ale żerne
Inna grupa metod utrzymuje kryształy zawieszone w cieczy i dostarcza je ciągłym strumieniem przez wiązkę. Dysze generujące wirtualne strumienie gazowo‑dynamiczne tworzą włosowate dżety zdolne nadążyć za szybkim trybem XFEL, dzięki czemu są podstawowym narzędziem do badań czas‑rozwiązanych i eksperymentów mix‑and‑inject, w których reakcje wyzwalane są szybkim mieszaniem tuż przed naświetleniem. Jednak ponieważ dżety pracują ciągle, większość strumienia nigdy nie spotyka impulsu rentgenowskiego. Nawet przy starannym dostrojeniu, praktyczne eksperymenty zużywają znacznie więcej białka niż teoretyczne minimum — zwykle dziesiątki do setek mikrolitrów skoncentrowanej zawiesiny kryształów. Aby złagodzić ten problem, opracowano bardziej wydajne konstrukcje, takie jak dysze z podwójnym przepływem, które otaczają strumień kryształów płynem poświęcalnym, elektroprzędne wtryskiwacze „MESH” działające przy niższych przepływach oraz ekstrudery o wysokiej lepkości, wypychające kryształy zatopione w żelach lub lipidowych fazach sześciennych z prędkościami mikrolitrów na minutę lub wolniejszymi. Metody lepkie są szczególnie cenne dla delikatnych białek błonowych i dla badań w temperaturze pokojowej na synchrotronach, ale ich grubsze strumienie zwiększają rozpraszanie tła i są mniej odpowiednie dla najszybszych źródeł rentgenowskich.
Kropelki, taśmy i hybrydy: dopasowanie impulsów jeden do jednego
Trzecia, coraz bardziej kreatywna klasa „hybrydowych” podejść łączy stałe nośniki z kontrolowanym podawaniem cieczy lub kropel. Systemy z taśmą, na przykład, nanoszą krople lub cienkie paski cieczy na ruchomą folię polimerową, która przechodzi przez wiązkę; sterowanie ruchem pozwala badać etapy reakcji lub ekspozycję na gazy w określonych opóźnieniach. Systemy drop‑on‑demand idą krok dalej, używając urządzeń akustycznych lub piezoelektrycznych do wyrzucania nanolitrów a nawet pikolitrów kropelek tylko wtedy, gdy spodziewany jest impuls rentgenowski, co dramatycznie ogranicza marnotrawstwo. Niektóre projekty mieszają kroplę ligandu z wcześniej umieszczoną kroplą zawierającą kryształy na taśmie tuż przed wejściem w wiązkę, umożliwiając badania enzymologii czas‑rozwiązanej przy starannie dozowanych reagentach. Inne hybrydy, jak metoda LAMA na chipie, dodają maleńkie krople substratu bezpośrednio na kryształy umieszczone na stałych chipach. W tych rozwiązaniach zużycie białka raportowane w literaturze obejmuje szeroki zakres — od poziomów bliskich miligramom do kilku miligramów dla pełnych serii czas‑rozwiązanych — co pokazuje zarówno potencjał, jak i obecne wyzwania inżynieryjne związane z synchronizacją kropel, kryształów i impulsów rentgenowskich.
Jak blisko jesteśmy teoretycznego minimum?
Porównując dziesiątki opublikowanych eksperymentów z zastosowaniem stałych celów, wtryskiwaczy ciekłych i systemów hybrydowych, autorzy pokazują, że żadna z istniejących metod nie zbliża się do idealnego progu 450 nanogramów; nawet najlepsze urządzenia przekraczają go w przybliżeniu o dwie rzędy wielkości. Jednocześnie wyłaniają się wyraźne trendy. Stałe cele zazwyczaj używają najmniej białka i są atrakcyjne zawsze, gdy mieszanie czas‑rozwiązane nie jest konieczne lub można je zaprojektować na chipie. Dżety ciekłe wciąż dominują w najbardziej wymagających badaniach czas‑rozwiązanych na XFEL, ale pozostają zasobożerne, zwłaszcza gdy potrzeba wielu punktów czasowych. Hybrydowe schematy z kropelkami i taśmą oferują największe względne oszczędności, zwłaszcza gdy timing kropelek jest ściśle zsynchronizowany ze źródłem rentgenowskim. Patrząc w przyszłość, artykuł argumentuje, że dalszy postęp przyniosą lepsza kontrola mikrofluidyczna, automatyzacja eliminująca marnotrawne kroki manipulacyjne oraz wykorzystanie kompaktowych źródeł rentgenowskich i optymalizacji opartej na danych do wspólnego projektowania eksperymentów i systemów podawania, które będą coraz bardziej zbliżać zużycie białka do teoretycznego limitu.
Cytowanie: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Słowa kluczowe: krystalografia seryjna, krystalografia rentgenowska białek, dostarczanie próbek, rentgenowski laser swobodnego elektronu (XFEL), mikrofluidyka