Clear Sky Science · pl
Centrum nerwowe inżynierii narządów
Dlaczego okablowanie narządów ma znaczenie
Naukowcy zbliżają się do tworzenia w laboratorium narządów zastępczych, aby poradzić sobie z poważnym niedoborem dawców serc, wątrób, nerek i innych organów. Jednak większość sztucznych narządów koncentruje się na naczyniach krwionośnych i pomija inny kluczowy składnik: nerwy. Ten artykuł przeglądowy wyjaśnia, dlaczego elektryczne okablowanie organizmu jest niezbędne dla wzrostu narządów, codziennej funkcji i gojenia oraz jak badacze uczą się wplatać sieci nerwowe w hodowane w laboratorium narządy.
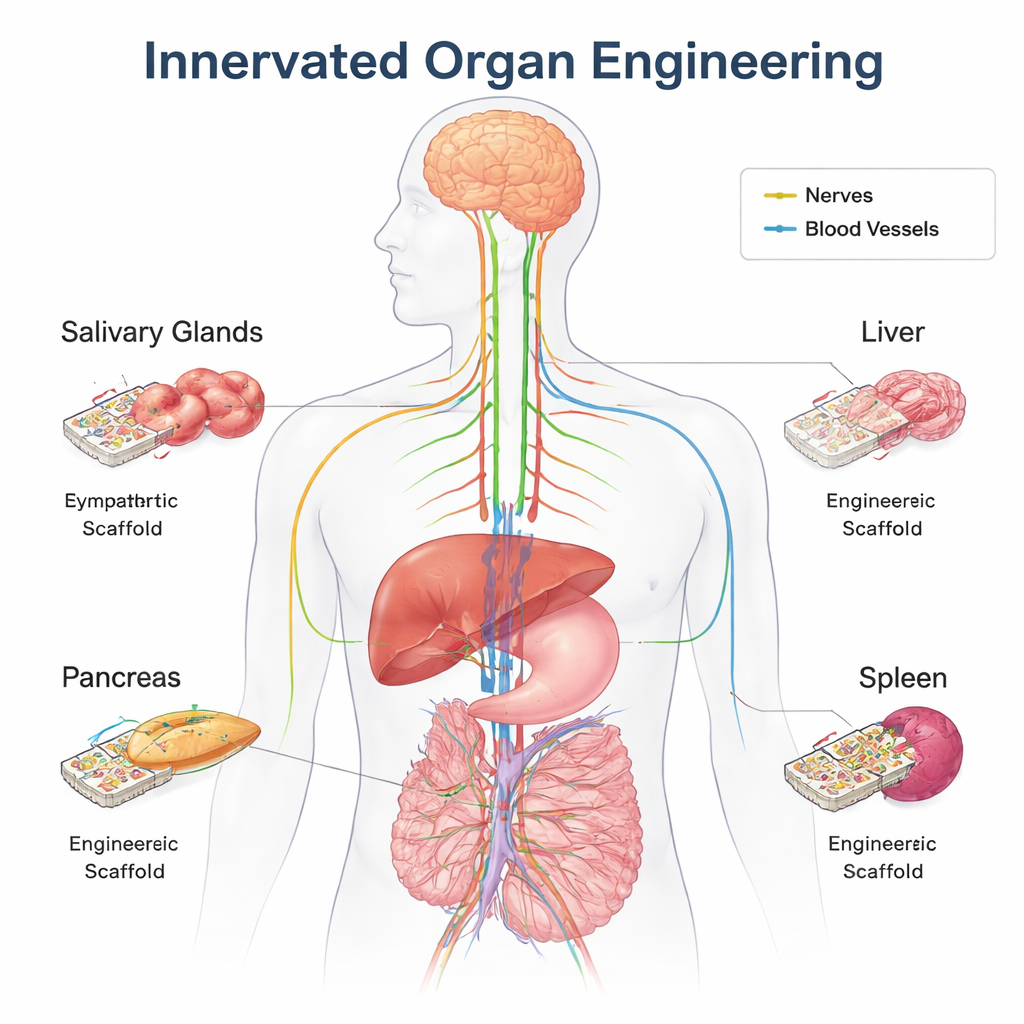
Ukryta sieć kontrolna w ciele
Każdy większy narząd jest przeniknięty włóknami nerwowymi, które nieustannie komunikują się z mózgiem i rdzeniem kręgowym. Poprzez autonomiczny układ nerwowy — gałęzie „walcz lub uciekaj” i „odpocznij i traw” — te nerwy dyskretnie regulują poziom cukru we krwi, trawienie, reakcje immunologiczne, przepływ krwi i wiele innych funkcji. Robią to, wysyłając chemiczne przekazy, takie jak acetylocholina i noradrenalina, oraz poprzez wykrywanie zmian, na przykład rozciągnięcia, temperatury czy poziomu składników odżywczych. Poza codzienną kontrolą, nerwy pomagają również kształtować narządy przed narodzinami, kierować gojeniem ran i wspierać komórki macierzyste odpowiedzialne za naprawę tkanek. W wielu miejscach nerwy rosną obok naczyń krwionośnych, korzystając z podobnych wskazówek kierunkowych, dlatego okablowanie i „instalacja hydrauliczna” rozwijają się równocześnie.
Dlaczego przeszczepy radzą sobie bez nerwów — a narządy laboratoryjne nie
Tradycyjne przeszczepy narządów zwykle wszczepia się bez ich pierwotnych połączeń nerwowych. Przeszczepiona wątroba czy nerka nadal mogą funkcjonować, ponieważ otrzymują hormony i inne sygnały przez krwioobieg, a z czasem u biorcy mogą odrosnąć nowe włókna nerwowe. Tego rodzaju „okresu łaski” nie ma w przypadku narządów inżynierowanych od podstaw. Konstrukty te zazwyczaj nie zawierają pełnego miksu dojrzałych typów komórek ani złożonej macierzy podporowej występującej w naturalnym narządzie. Precyzyjne połączenia nerwowe są szczególnie ważne do koordynacji wielu wyspecjalizowanych komórek w narządach takich jak trzustka, wątroba, gruczoły ślinowe czy śledziona. Autorzy argumentują, że w inżynierii narządów metodą „oddolną” — gdzie narządy składa się z małych elementów budulcowych — zaplanowana wcześniej innervacja powinna być traktowana jako wymaganie projektowe, a nie opcjonalny dodatek.
Jak nerwy kształtują cztery kluczowe narządy
Przegląd szczegółowo opisuje, jak nerwy wpływają na cztery przykładowe narządy. W trzustce włókna współczulne i przywspółczulne pomagają rzeźbić architekturę wysp produkujących insulinę podczas rozwoju, a później precyzyjnie regulują uwalnianie insuliny i glukagonu w odpowiedzi na wahania poziomu cukru we krwi. W gruczołach ślinowych wczesny wpływ przywspółczulny utrzymuje przy życiu nabłonkowe komórki macierzyste i kieruje rozgałęzianiem przewodów, które ostatecznie wydzielają ślinę; przecięcie tych nerwów w nieodpowiednim momencie zaburza prawidłowy rozwój gruczołu. Nerwy w wątrobie wyczuwają poziomy soli, wody, cukru i tłuszczu we krwi oraz dostosowują metabolizm, ciśnienie krwi i regenerację po urazie. W śledzionie włókna współczulne komunikują się bezpośrednio z komórkami układu odpornościowego, tłumiąc lub wzmacniając zapalenie i pomagając organizmowi reagować na infekcję i stres. W tych narządach utrata lub nieprawidłowe okablowanie nerwów wiąże się z cukrzycą, problemami trawiennymi, chorobami wątroby i upośledzoną odpornością.
Budowanie narządów z wbudowanym okablowaniem
Aby wprowadzić unaczynienie nerwowe do bioinżynieryjnych narządów, naukowcy łączą zaawansowane drukowanie 3D, przemyślane projekty rusztowań i komórki nerwowe pochodzące z komórek macierzystych. Drukowanie ekstruzyjne i oparte na świetle pozwala umieszczać różne typy komórek i materiały w precyzyjnych wzorach, podczas gdy specjalne hydrożele i polimery są dostrojone do podtrzymywania długich, rozgałęziających się włókien nerwowych. Badania już stworzyły drukowane sieci neuronowe, jednostki nerwowo-mięśniowe oraz miniaturowe tkanki przypominające mózg, które wykazują realistyczną aktywność elektryczną. Autorzy przedstawiają praktyczne plany dla unaczynionych wersji trzustki, gruczołu ślinowego, wątroby i śledziony: wyizolować lub otrzymać kluczowe komórki narządowe, wymieszać je z neuronami autonomicznymi (współczulnymi i przywspółczulnymi) w kompatybilnych bioatramentach, wydrukować je w kształty przypominające narządy i dojrzewać w bioreaktorach, aby nerwy miały czas wydłużyć się do tkanki przed implantacją.
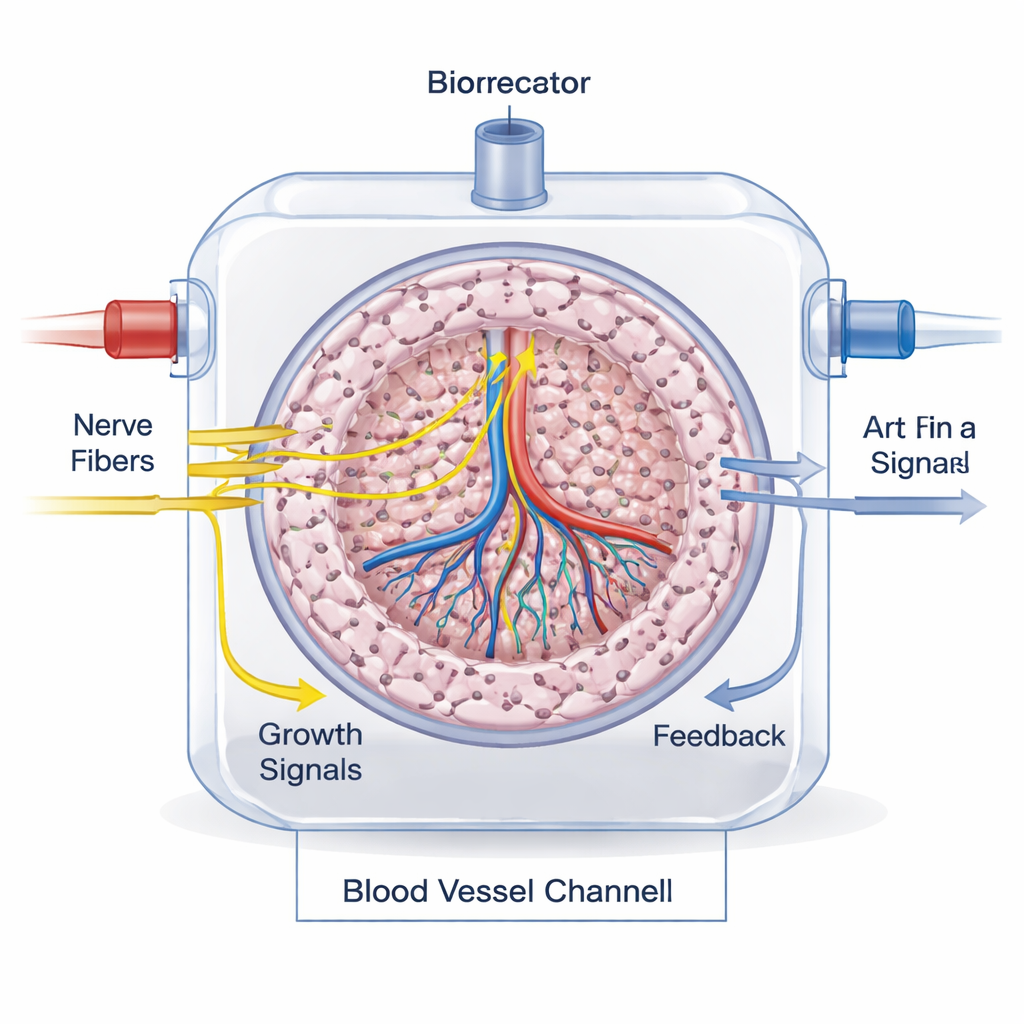
Pomiar, czy okablowanie działa
Sprawdzenie, czy nerwy są rzeczywiście zintegrowane i funkcjonalne, to duże wyzwanie. W laboratorium badacze barwią specyficzne białka nerwowe, mierzą neuroprzekaźniki testami biochemicznymi i używają obrazowania na żywo, by obserwować wzrost aksonów i reakcje komórek. Mikropłytkowe platformy „narząd-na-chipie” pomagają modelować realistyczny przepływ krwi i sygnalizację nerw‑narząd. U zwierząt, a w przyszłości u pacjentów, innervację można śledzić, łącząc barwienia tkanek, śledzenie nerwów i nowoczesne metody obrazowania, takie jak MRI, CT i PET z użyciem wyspecjalizowanych radioaktywnych związków, które uwidaczniają włókna współczulne lub przywspółczulne.
Od pomysłu do terapii
Artykuł konkluduje, że nerwy nie są luksusową cechą, lecz zasadniczym wymogiem dla naprawdę funkcjonalnych sztucznych narządów. Aby przejść od obiecujących demonstracji laboratoryjnych do rzeczywistych terapii, przyszłe prace muszą usprawnić drukowanie 3D na dużą skalę skomplikowanych sieci nerwowych, dopracować źródła komórek (zwłaszcza ludzkie neurony autonomiczne pochodzące z komórek macierzystych) oraz opracować praktyczne kliniczne narzędzia obrazowania do monitorowania integracji nerwowej po implantacji. Jeśli te przeszkody zostaną pokonane, nowej generacji narządy inżynieryjne mogłyby nie tylko zastępować utracone tkanki, lecz także płynnie włączać się w własne układy kontrolne organizmu, oferując bardziej niezawodne i realistyczne terapie dla cukrzycy, niewydolności wątroby, zaburzeń suchości jamy ustnej, niedoborów odporności i innych schorzeń.
Cytowanie: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Słowa kluczowe: inżynieria narządów, unaczynienie nerwowe, biofabrykacja, drukowanie 3D biokomponentów, autonomiczny układ nerwowy