Clear Sky Science · pl
Optyczna histologia o nadmiernej rozdzielczości próbek utrwalonych w formalinie i zatopionych w parafinie: wyzwania i możliwości
Widzieć więcej w przechowanych próbkach tkanek
Szpitale na całym świecie przechowują cienkie skrawki narządów pacjentów w blokach wosku, aby choroby, takie jak rak czy uszkodzenie nerek, mogły być badane przez lata. Artykuł przeglądowy wyjaśnia, jak nowe rodzaje mikroskopów świetlnych przekształcają te rutynowe próbki w potężne okna na chorobę, ujawniając detale znacznie mniejsze niż to, co mogą zobaczyć standardowe mikroskopy szpitalne. Postępy te mogą pomóc lekarzom wcześniej wykrywać choroby, lepiej rozumieć ich przebieg i precyzyjniej dopasowywać terapie.
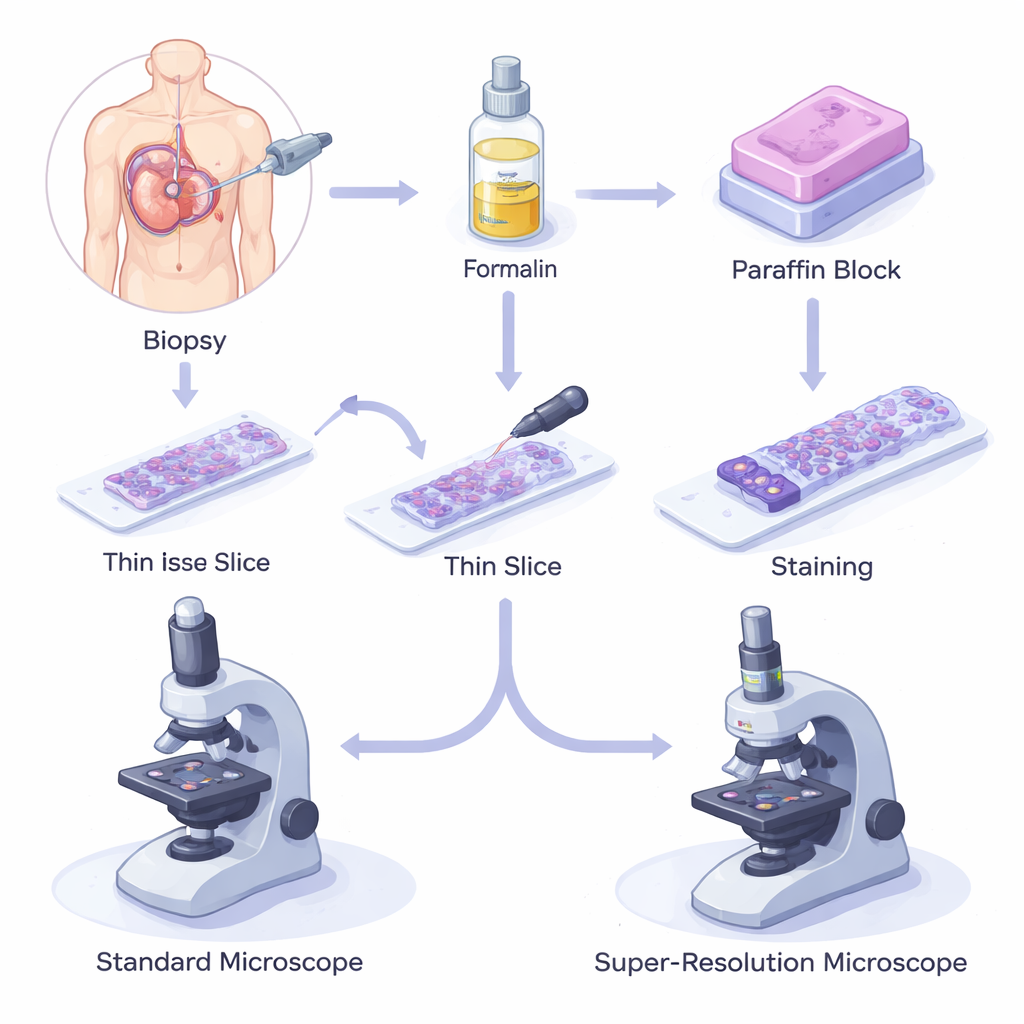
Jak tkanki konserwowane w wosku napędzają współczesną medycynę
Kiedy pacjent przechodzi biopsję, usuwa się mały fragment tkanki, utrwala go w chemicznym preparacie zwanym formaliną, aby zatrzymać rozkład, a następnie zatapia w parafinowym wosku. Blok jest krojony na włosowate sekcje, umieszczany na szkiełkach, barwiony i oglądany pod mikroskopem świetlnym. Metoda utrwalenia w formalinie i zatopienia w parafinie (FFPE) jest tania, niezawodna i pozwala przechowywać próbki przez dziesięciolecia w temperaturze pokojowej. W rezultacie miliony próbek FFPE są składowane w biobankach na całym świecie, wspierając wszystko, od badań podstawowych po zaawansowane analizy genetyczne i białkowe, tworząc trzon współczesnej diagnostyki i prognozowania.
Dlaczego zwykłe mikroskopy już nie wystarczają
Tradycyjne mikroskopy optyczne są ograniczone przez fizykę światła: detale mniejsze niż około 250 nanometrów rozmazują się. Wiele struktur związanych z chorobami — takich jak drobne filtry w nerkach, połączenia między komórkami nerwowymi czy drobne zmiany w architekturze DNA w jądrze — mieści się poniżej tego limitu. Obecne procedury często łączą standardową mikroskopię świetlną dla ogólnego przeglądu z mikroskopią elektronową dla nanometrowych detali, ale takie podejście jest wolne, kosztowne i wymaga zupełnie innego przygotowania próbek. Klinicyści i badacze poszukują zatem pojedynczego, elastycznego systemu, który byłby w stanie szybko skanować duże obszary, a jednocześnie powiększać, aby ujrzeć cechy na skali nanometrów w tych samych sekcjach FFPE, których już używają.
Nowe sposoby na wyostrzenie obrazu
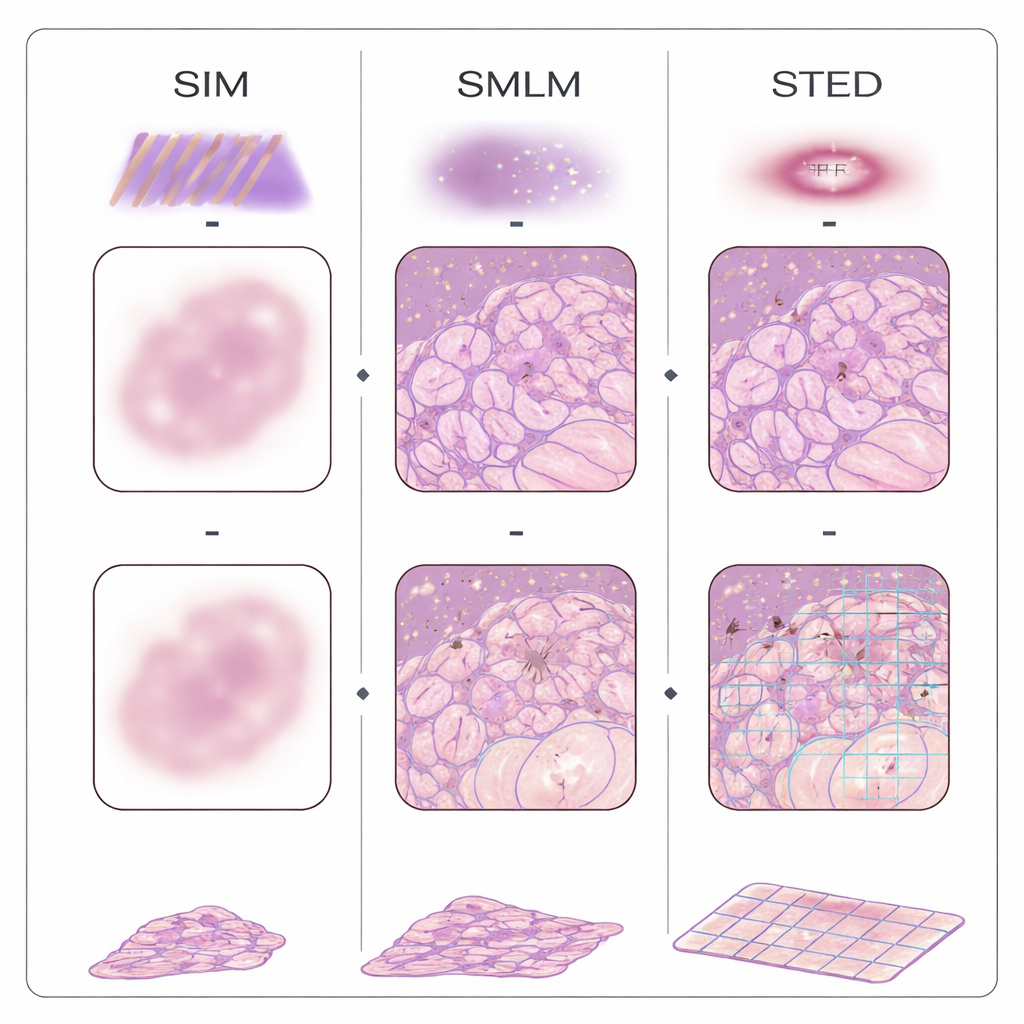
W ciągu ostatnich dwóch dekad kilka rodzin mikroskopów „o nadmiernej rozdzielczości” przełamało tradycyjną barierę rozdzielczości, wykorzystując znaczniki fluorescencyjne i sprytne układy optyczne. Metody lokalizacji pojedynczych cząsteczek włączają i wyłączają molekuły, określając ich położenie jedną po drugiej; strukturalna iluminacja projeksuje na tkankę paskowane wzory świetlne i używa obliczeń do odzyskania drobniejszych detali; wygaszanie wymuszonego emisji (STED) wyrzeźbia mały świecący punkt za pomocą wiązki w kształcie pączka; a podejścia oparte na fluktuacjach analizują subtelne migotanie obrazu, aby wywnioskować strukturę. Inna strategia, zwana mikroskopią rozszerzającą (expansion microscopy), unika skomplikowanej optyki przez fizyczne spulchnienie tkanki w żelu, dzięki czemu zwykłe mikroskopy mogą zobaczyć wcześniej niewidoczne detale. Metody te zostały już zastosowane do próbek FFPE z gruczołu piersiowego, jelita grubego, trzustki, nerki, mózgu, skóry, łożyska i innych narządów, ujawniając, jak mitochondria zmieniają się w nowotworach, jak zawodzi filtracja nerek oraz jak tworzą się grudki białkowe w chorobie Alzheimera.
Przeszkody na drodze do codziennego zastosowania
Mimo obiecujących perspektyw techniki te nie są jeszcze gotowe, by stać się rutynowymi narzędziami w większości laboratoriów patologicznych. Wiele systemów o nadmiernej rozdzielczości jest wolnych, obejmuje tylko niewielkie pola widzenia lub wymaga dziesiątek tysięcy obrazów do złożenia pojedynczego obrazu o wysokiej szczegółowości, co jest niepraktyczne, gdy patolog musi ocenić duże obszary tkanki. Same tkanki FFPE są optycznie trudne: rozpraszają światło, wykazują autofluorescencję i mogą ukrywać molekuły, które trzeba znakować, co wszystko razem może powodować rozmyte obrazy lub fałszywe struktury. Niektóre metody wymagają specjalnych barwników, niestandardowych buforów lub wieloetapowych zabiegów chemicznych, które trudno włączyć do standardowych procedur histologicznych. Do tego dochodzą wysokie koszty i złożoność obsługi instrumentów komercyjnych oraz konieczność intensywnego przetwarzania i przechowywania danych.
Łączenie inteligentnej optyki z inteligentnym oprogramowaniem
Aby przezwyciężyć te przeszkody, badacze łączą ulepszoną optykę z obrazowaniem bez użycia znaczników i sztuczną inteligencją. Metody wysokoprzepustowe, ograniczone dyfrakcją, takie jak ptychografia Fouriera i nieliniowa mikroskopia optyczna, mogą szybko skanować duże, nawet niebarwione sekcje FFPE i dostarczać ilościowych map struktury tkanki. Platformy patologii cyfrowej obecnie rejestrują całe szkiełka w wysokiej rozdzielczości i wykorzystują uczenie maszynowe do wykrywania guzów oraz oceniania biomarkerów, takich jak HER2, Ki‑67 i PD‑L1. Modele głębokiego uczenia potrafią nawet przekształcać obrazy o niskiej rozdzielczości w widoki o zwiększonej rozdzielczości, co potencjalnie zmniejsza zapotrzebowanie na niektóry specjalistyczny sprzęt, jednocześnie lepiej wykorzystując istniejące archiwa biopsji.
Co to oznacza dla przyszłych pacjentów
Autorzy stwierdzają, że prawdziwa „histologia o nadmiernej rozdzielczości” próbek FFPE — łącząca szczegóły na skali nanometrów, dużą prędkość, rozsądne koszty i zgodność z obecnymi procedurami laboratoryjnymi — nie została jeszcze w pełni zrealizowana, ale jest w zasięgu ręki. W miarę jak metody optyczne staną się szybsze i bardziej niezawodne, a analiza oparta na AI dojrzeje, narzędzia te mogą ujawniać subtelne wczesne zmiany w tkankach, które dziś pozostają niezauważone, poprawiać dokładność diagnoz i ukierunkowywać bardziej spersonalizowane decyzje terapeutyczne. W dłuższej perspektywie przekształcenie każdego zarchiwizowanego bloku wosku w mapę choroby o wysokiej rozdzielczości mogłoby zrewolucjonizować zarówno badania, jak i opiekę kliniczną.
Cytowanie: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Słowa kluczowe: mikroskopia o nadmiernej rozdzielczości, tkanki FFPE, patologia cyfrowa, obrazowanie optyczne, diagnostyka onkologiczna