Clear Sky Science · pl
Nanozymes rozszerzające granice biokatalizy
Małe pomocniki, które przyspieszają chemię
Od warzenia piwa po trawienie posiłku — nasze życie opiera się na niewidocznych pomocnikach zwanych katalizatorami, które przyspieszają reakcje chemiczne. Przez ponad sto lat uważano, że biologiczne katalizatory to jedynie kruche białka, a później także katalityczne RNA. Ten przegląd przedstawia „nanozymy” – maleńkie zaprojektowane cząstki, które zachowują się jak enzymy, lecz zbudowane są z trwałych materiałów, takich jak metale, tlenki czy węgiel. Mogą przetrwać ciepło, zimno i surowe warunki, i zaczynają zmieniać sposób, w jaki myślimy o chemii w systemach żywych, chorobach, przemyśle, a nawet o pochodzeniu życia.
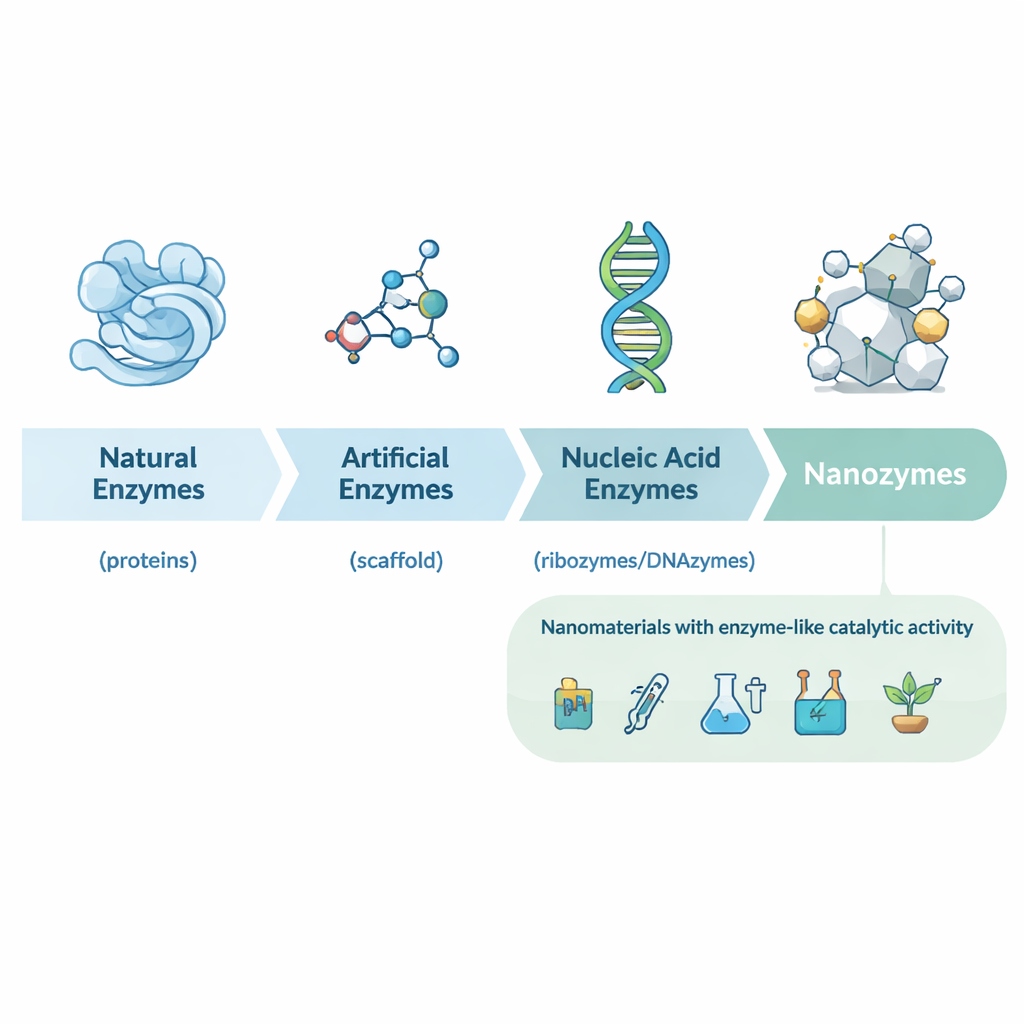
Od naturalnych enzymów do zaprojektowanych nanokatalizatorów
Artykuł najpierw przeprowadza przez historię biokatalizy, od wczesnych odkryć białkowych enzymów w drożdżach i sokach żołądkowych, przez rybozymy (katalityczne RNA), po szeroką gamę sztucznych enzymów zbudowanych z małych cząsteczek i przeciwciał. Tradycyjne katalizatory są potężne, lecz często drogie, niestabilne i trudne do masowej produkcji. Na początku XXI wieku badacze odkryli, że niektóre nanomateriały — na przykład nanocząstki tlenku żelaza — mogą naśladować zachowanie klasycznych enzymów, takich jak peroksydaza chrzanowa. Doprowadziło to do koncepcji nanozymów: cząstek o rozmiarach nanometrów, których własna struktura nadaje im aktywność podobną do enzymów, zamiast polegania na przyłączonych białkach czy małych molekułach katalitycznych.
Czym nanozymy różnią się od enzymów
W odróżnieniu od enzymów, które mają pojedynczą, precyzyjnie ukształtowaną kieszeń aktywną, nanozymy eksponują wiele aktywnych miejsc na swoich powierzchniach. Miejsca te mogą występować na krawędziach kryształów, w defektach lub na granicach między dwoma materiałami i łącznie mogą przetwarzać wiele cząsteczek jednocześnie. Pojedyncze miejsce aktywne w nanozymie jest zwykle mniej wydajne niż miejsce w enzymie, lecz jedna nanocząstka może mieścić tysiące takich miejsc, więc jej całkowita moc katalityczna może dorównywać lub przewyższać enzymy naturalne. Ich aktywność można również dostroić przez zmianę rozmiaru, kształtu, domieszkowania chemicznego i powłok powierzchniowych — podobnie jak regulacja architektury i okablowania małej maszyny. Ponieważ są zbudowane z odpornych ciał stałych zamiast delikatnie złożonych białek, nanozymy działają w wysokich i niskich temperaturach czy w silnych roztworach soli, które szybko unieruchomiłyby większość enzymów.
Jak działają nanozymy i jak się je mierzy
Autorzy pokazują, że nanozymy często podążają za tymi samymi podstawowymi zasadami kinetycznymi, które biochemicy stosują do enzymów, takimi jak zachowanie Michaelisa–Menten, gdzie prędkość reakcji zależy od tego, jak łatwo katalizator wiąże i przekształca substrat. Istnieją jednak istotne odmienności. Jedna cząstka może zawierać wiele typów miejsc aktywnych, więc pojedynczy nanozym może przeprowadzać różne reakcje lub nawet sprzeczne działania, np. jednocześnie tworzyć i usuwać reaktywne formy tlenu. To może dawać złożone, „nieklasyczne” krzywe kinetyczne, które ukrywają wiele procesów pod jednym gładkim przebiegiem. Przegląd wyjaśnia, jak badacze rozkładają te zachowania, szacują, ile naprawdę istnieje miejsc aktywnych, i porównują ogólną aktywność różnych nanozymów przy użyciu zunifikowanych jednostek — wszystko to jest kluczowe, by przemienić ciekawy materiał w niezawodne narzędzie.
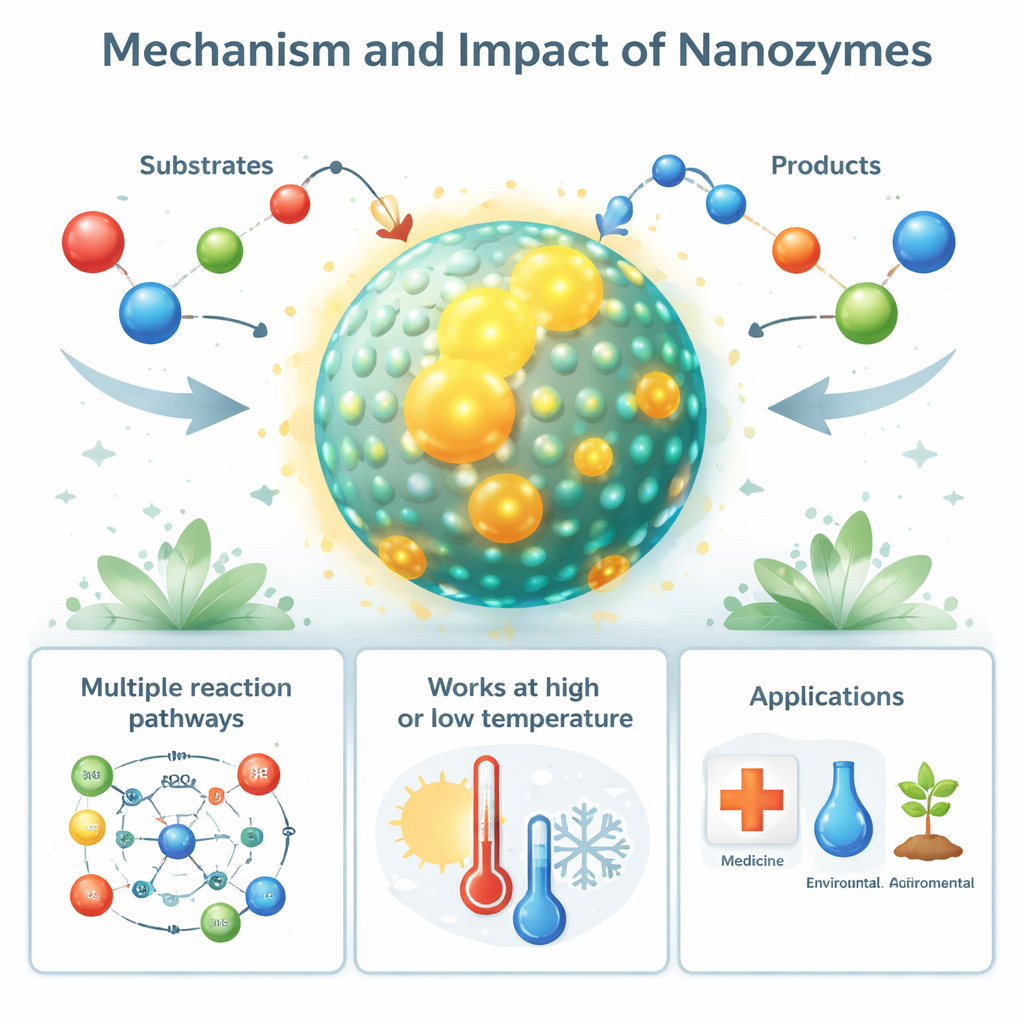
Od naturalnych nanozymów do zastosowań w praktyce
Co interesujące, zachowanie podobne do nanozymów nie ogranicza się do laboratorium. Niektóre biologiczne nanostruktury, takie jak białkowe klatki wypełnione żelazem (ferrytyna) czy magnetyczne cząstki w bakteriach (magnetosomy), działają jak naturalne nanozymy, pomagając kontrolować szkodliwe reaktywne formy tlenu. Nawet związane z chorobami włókna białkowe, jak złogi amyloidowe w chorobie Alzheimera, mogą wykazywać aktywność peroksydazopodobną, która uszkadza pobliskie komórki. W zastosowaniach praktycznych syntetyczne nanozymy służą jako tańsze, bardziej odporne zamienniki enzymów w testach diagnostycznych, biosensorach i analizach przemysłowych. Ich zdolność do generowania lub usuwania reaktywnych form tlenu jest wykorzystywana do zabijania komórek nowotworowych i bakterii, ochrony tkanek przed stresem oksydacyjnym oraz pomocy roślinom w znoszeniu suszy, zasolenia i zanieczyszczeń.
Projektowanie nowej generacji inteligentnych katalizatorów
Patrząc w przyszłość, autorzy wskazują kluczowe wyzwania: określenie dokładnych struktur atomowych, które pełnią funkcję miejsc aktywnych, poprawa selektywności reakcji tak, by nanozymy działały tylko tam i wtedy, gdzie są potrzebne, oraz zapewnienie bezpieczeństwa i stabilności wewnątrz organizmu. Wymieniają zaawansowane techniki obrazowania, symulacje kwantowe i uczenie maszynowe jako potężne narzędzia do przewidywania i optymalizacji wydajności nanozymów. Ponieważ nanozymy mogą działać w ekstremalnych warunkach, reagować na światło, ciepło, dźwięk lub pola magnetyczne, a czasem przeprowadzać kilka reakcji w sekwencji, mogą stać się podstawą nowych terapii, technologii środowiskowych i procesów przemysłowych. Przegląd konkluduje, że nanozymy poszerzają samo pojęcie biokatalizy i mogą nawet dostarczać wskazówek, jak prymitywne katalizatory napędzały chemię wczesnego życia.
Cytowanie: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Słowa kluczowe: nanozymy, biokataliza, nanocząstki, naśladowcy enzymów, reaktywne formy tlenu