Clear Sky Science · pl
Czujniki nanoporowe do wykrywania konformacji białek i peptydów do zastosowań przy łóżku pacjenta
Dlaczego maleńkie kształty białek mogą zmienić następne badanie kontrolne
Wraz ze starzeniem się społeczeństw choroby takie jak Alzheimer, Parkinson, choroby serca i nowotwory stają się coraz częstsze. Wiele z tych schorzeń zaczyna się w momencie, gdy istotne białka i małe fragmenty białkowe (peptydy) subtelnie zmieniają kształt na długo przed pojawieniem się objawów. Dzisiejsze testy kliniczne zwykle mierzą, ile danego biomarkera jest obecne, a nie czy jego kształt jest prawidłowy czy zniekształcony. Ten artykuł opisuje technologię zwaną sensingiem nanoporowym, która może elektrycznie „wyczuć” kształt i chemię pojedynczych cząsteczek białek, i argumentuje, że może ona stać się podstawą przyszłych testów przyłóżkowych działających w ciągu minut na małym urządzeniu.
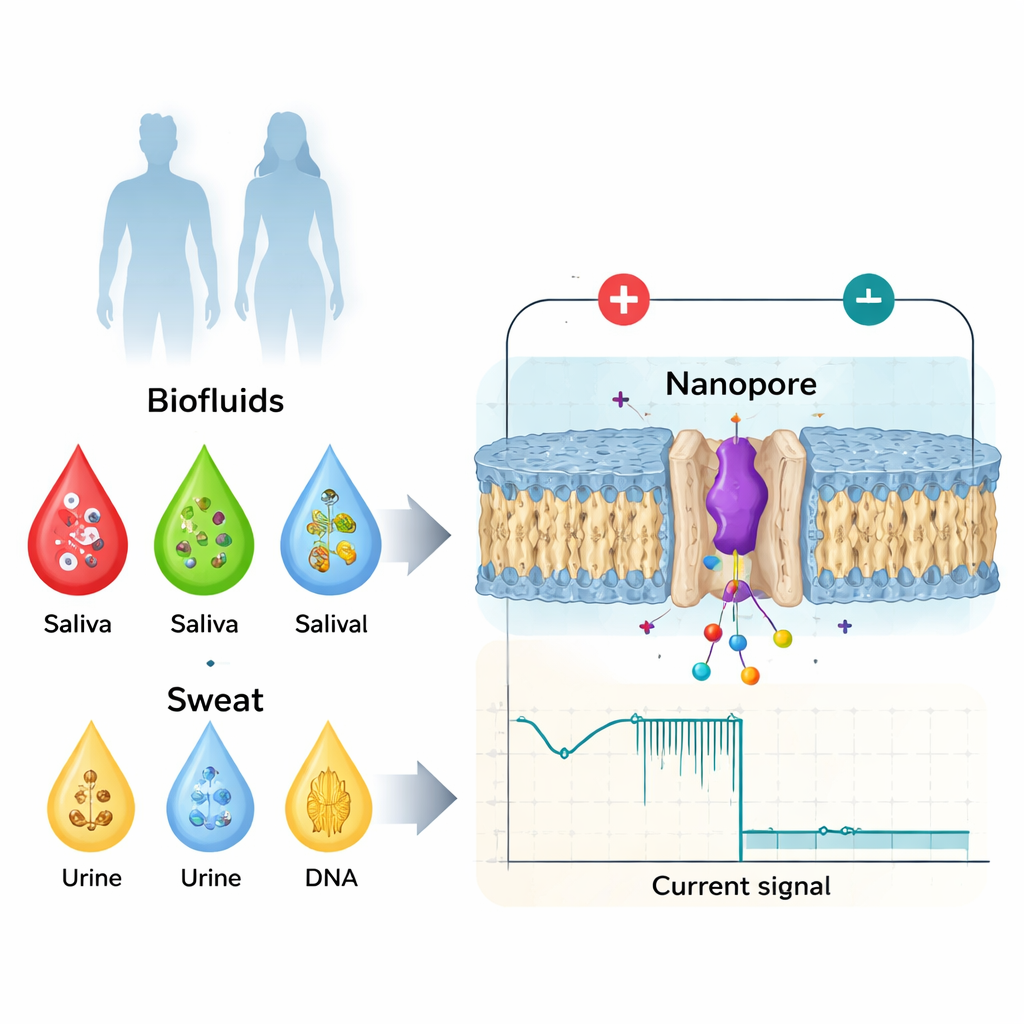
Od prostych badań krwi do biomarkerów rozpoznających kształt
Lekarze już wykorzystują wiele biomarkerów pobieranych z krwi, śliny, moczu czy potu — takich jak białka, hormony czy małe cząsteczki — do monitorowania stanu zdrowia i chorób. Tradycyjnie skupiano się na dużych zmianach: nadmiarze białka, uszkodzeniach DNA czy obecności wirusowego składnika. Jednak biologia bywa bardziej subtelna. To samo białko może być włączone lub wyłączone przez drobne zmiany w jego strukturze, przez chemiczne znaczniki dodawane po jego syntezie, lub przez lustrzane wersje jego cegiełek konstrukcyjnych. Te niewielkie zmiany mogą zmieniać, jak białko wiąże partnerów, tworzy agregaty czy przekazuje sygnały, i są powiązane z zaburzeniami krzepnięcia, chorobami neurodegeneracyjnymi i nowotworami. Standardowe narzędzia szpitalne, takie jak spektrometria mas, testy oparte na przeciwciałach czy obrazowanie o wysokiej rozdzielczości, są potężne, lecz kosztowne, wolne, wymagają wysoko wykwalifikowanego personelu i zwykle nie nadają się do szybkiego, prostego zastosowania przy łóżku pacjenta.
Co robi nanopora inaczej
Sensing nanoporowy odwraca problem do góry nogami. Zamiast uśredniać wyniki dla bilionów cząsteczek, bada je pojedynczo, gdy przechodzą przez maleńki otwór w membranie o szerokości zaledwie kilku miliardowych metra. Przyłożone napięcie powoduje przepływ jonów przez pory, co tworzy stały prąd elektryczny. Gdy białko lub peptyd wchodzi do pory, częściowo blokuje ten prąd. Głębokość spadku prądu, czas jego trwania i drobne szczegóły kształtu sygnału zależą od rozmiaru, ładunku i konformacji cząsteczki (jej trójwymiarowego złożenia). Poprzez staranne projektowanie poru — wykorzystując białka inżynieryjne lub materiały częściowo stałe — badacze mogą utrzymać pojedyncze biomolekuły wystarczająco długo, by uzyskać bogate elektryczne „odciski palców”, które rozróżniają nie tylko różne białka, ale też subtelne warianty tego samego biomarkera.
Odczytywanie zmian istotnych dla chorób, molekuła po molekule
Przegląd podkreśla, jak nanopory zostały już wykorzystane do rozróżniania medycznie istotnych różnic, których inne metody mają trudność dostrzec. Potrafią rozróżnić peptydy różniące się jednym aminokwasem, wykrywać warianty hemoglobiny związane z chorobami bezpośrednio z krwi oraz odróżniać krótkie peptydy podobne do hormonów różniące się tylko jednym elementem budulcowym, a nawet lustrzaną formą tego elementu. Nanopory mogą także wykrywać modyfikacje potranslacyjne — małe chemiczne znaczniki, takie jak grupy fosforanowe, cukrowe czy siarczanowe — które kontrolują, czy białka zaangażowane w choroby Alzheimera, Parkinsona, krzepnięcie krwi czy nowotwory zachowują się normalnie czy patologicznie. W niektórych eksperymentach pojedyncza enzymatyczna cząsteczka lub białko wiążące jest utrzymywane wewnątrz poru, a zmiany w jej sygnale elektrycznym ujawniają w czasie rzeczywistym, jak wiąże partnerów lub przeprowadza reakcje, co potencjalnie ujawnia niewłaściwie działające ścieżki w chorobie.
W kierunku szybkich testów przy łóżku pacjenta
Ponieważ każde zdarzenie blokowania odpowiada jednej cząsteczce, urządzenia nanoporowe mogą być wyjątkowo czułe, wykrywając zaledwie tysiące kopii biomarkera w złożonym płynie. Autorzy omawiają strategie pokonywania kluczowych przeszkód dla zastosowań klinicznych: zwiększanie szybkości chwytania rzadkich molekuł, stabilizowanie membran lub użycie hybrydowych porów stało-biologicznych oraz zastosowanie uczenia maszynowego do automatycznej klasyfikacji złożonych wzorców elektrycznych w jasne kategorie diagnostyczne. Pokazują również, jak podejścia pośrednie — takie jak dołączanie znaczników DNA czy partnerów wiążących — mogą wzmocnić słabe sygnały lub pozwolić na jednoczesne pomiary wielu biomarkerów, zachowując przy tym dużą część szczegółów konformacyjnych, które czynią nanopory wyjątkowymi.
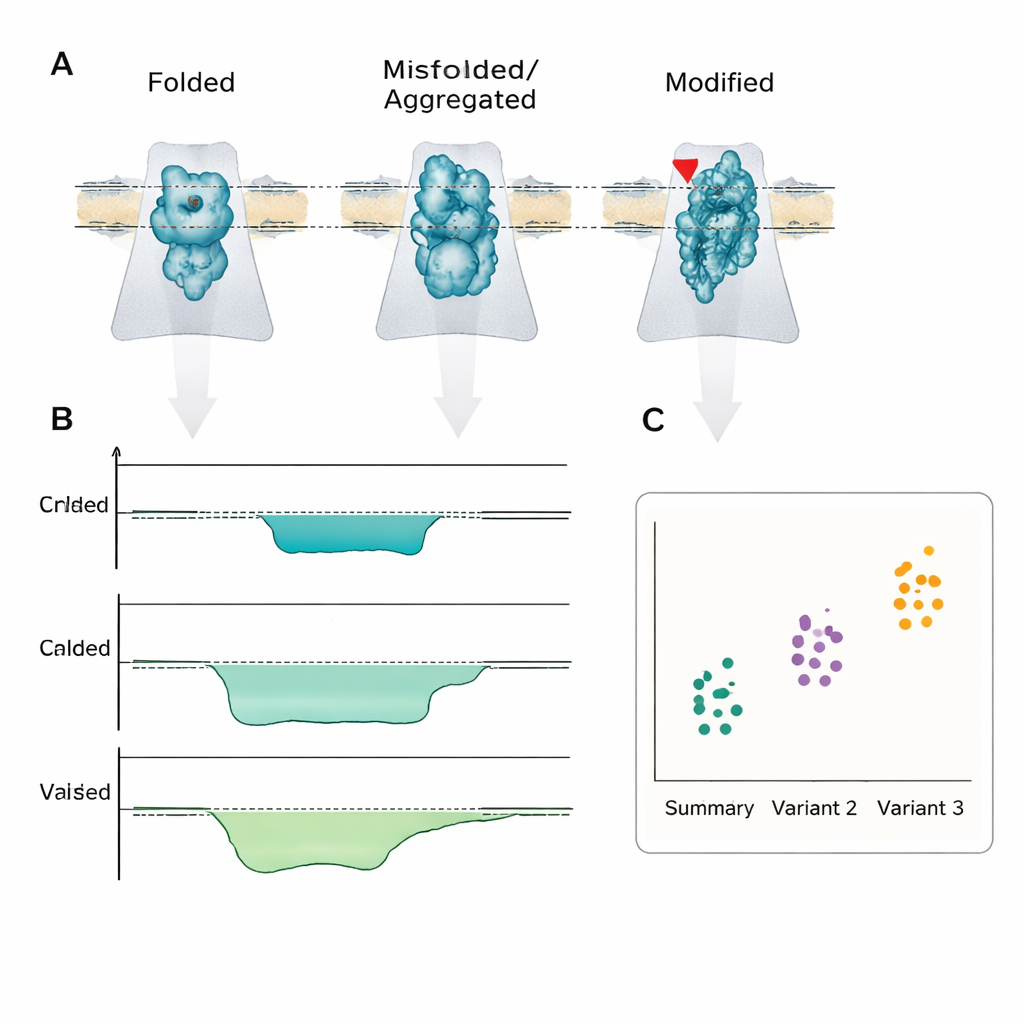
Co to może znaczyć dla pacjentów
Główne przesłanie jest takie, że choroba często zależy mniej od ilości białka, a bardziej od tego, która forma kształtowa lub chemiczna jest obecna. Sensing nanoporowy jest jedną z nielicznych technologii, które mogą bezpośrednio odczytywać te różnice na poziomie pojedynczych cząsteczek, na tyle szybko i prosto, by można go było zintegrować z przenośnymi urządzeniami. Chociaż nadal pozostają znaczące wyzwania inżynieryjne i w zakresie standaryzacji, autorzy twierdzą, że podobnie jak sekwenatory DNA oparte na nanoporach trafiły do kliniki, sensory białek i peptydów oparte na nanoporach w końcu mogą dostarczać szybkie testy przy łóżku pacjenta, które nie tylko stwierdzą „coś jest nie tak”, lecz także ujawnią dokładne molekularne nieprawidłowe złożenie lub modyfikację leżącą u podstaw stanu pacjenta.
Cytowanie: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Słowa kluczowe: czujniki nanoporowe, biomarkery białkowe, diagnostyka przy łóżku pacjenta, modyfikacje potranslacyjne, choroby konformacyjne