Clear Sky Science · pl
Elektronika inspirowana biologią: miękkie, biohybrydowe i „żywe” interfejsy nerwowe
Delikatne urządzenia dla układu nerwowego
Od interfejsów mózg–komputer pozwalających ludziom poruszać ramionami robotycznymi po stymulatory głębokie łagodzące objawy choroby Parkinsona — elektronika komunikująca się z naszymi nerwami szybko przestaje być fantastyką i staje się medyczną rzeczywistością. Jednak współczesne urządzenia wciąż są w gruncie rzeczy kawałkami metalu i krzemu wprowadzanymi w tkankę miękką jak budyń. Ten przegląd wyjaśnia, jak naukowcy przeprojektowują te narzędzia, by przypominały ciało — były bardziej miękkie, biologicznie aktywne, a nawet częściowo żywe — z nadzieją na bezpieczniejsze, trwalsze implanty nerwowe, które będą pomagać w gojeniu mózgu i nerwów.
Dlaczego tradycyjne implanty nie wystarczają
Konwencjonalne implanty nerwowe, takie jak matryce Utah czy elektrody do stymulacji głębokiej, zbudowane są z sztywnych metali i krzemu. Materiały te są miliony razy sztywniejsze niż tkanka mózgowa, która zachowuje się bardziej jak galaretka niż szkło. To niedopasowanie utrudnia urządzeniom dopasowanie do subtelnych ruchów i kształtów mózgu. W miarę jak tkanka przesuwa się z każdym uderzeniem serca i oddechem, sztywne elektrody ocierają się i ciągną, powodując drobne urazy. Organizm rozpoznaje te obce obiekty i uruchamia reakcję immunologiczną, otaczając je gęstą blizną z komórek podporowych. Z czasem ta blizna zwiększa oporność elektryczną między urządzeniem a pobliskimi neuronami, pogarszając jakość sygnału i skracając czas, przez jaki implant działa niezawodnie.
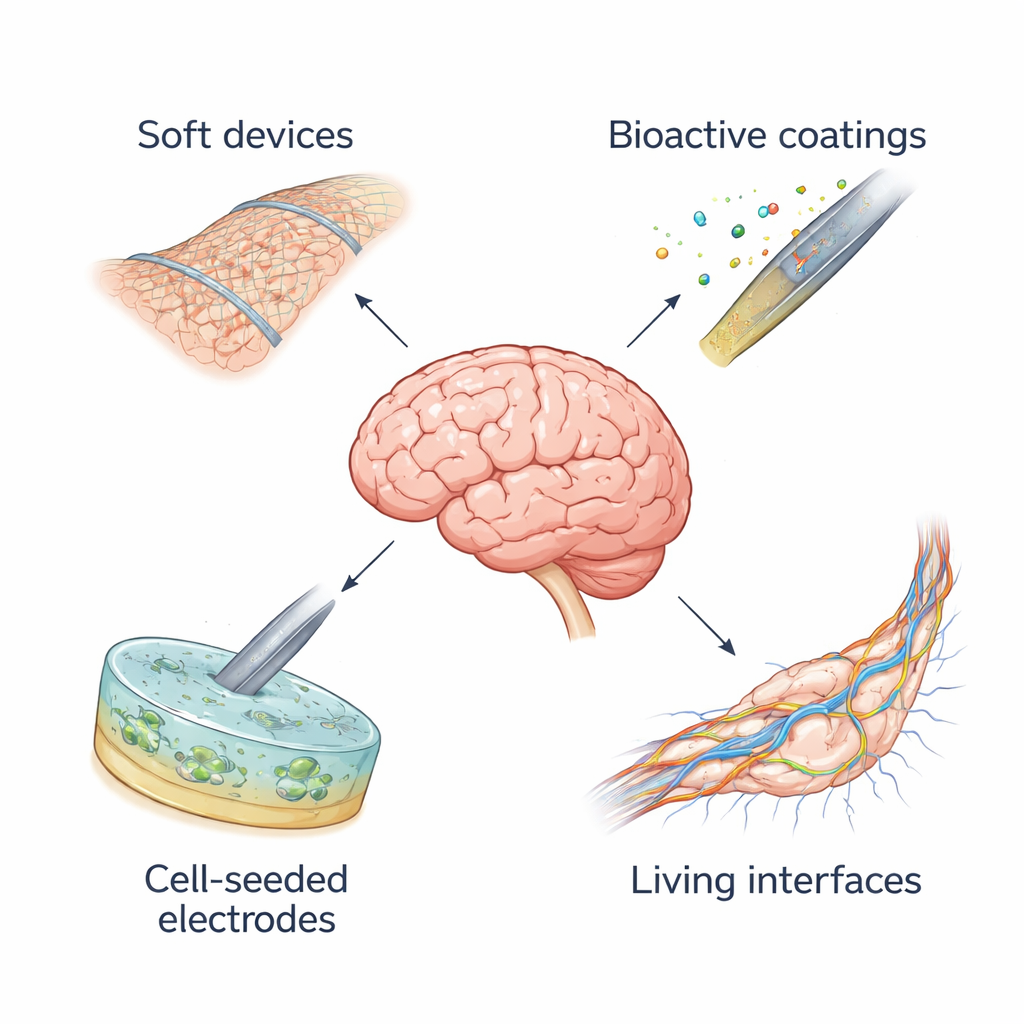
Miękkie urządzenia, które poruszają się razem z mózgiem
Aby zmniejszyć to uszkodzenie, badacze tworzą elektronikę „biomimetyczną” — urządzenia, których właściwości fizyczne naśladują tkankę, z którą mają kontakt. Zamiast grubych, sztywnych prętów inżynierowie opracowują ultra‑cienkie folie, elastyczne włókna i otwarte struktury siatkowe, które mogą się zginać i zwijać jak żywe komórki. Miękkie polimery, rozciągliwe guma i żele bogate w wodę pomagają dopasować się do miękkości mózgu i tłumić siły wywołujące zapalenie. Niektóre z tych urządzeń splatają przewodzące tworzywa lub nanomateriały, takie jak grafen, w elastyczne rdzenie, zachowując wysoką jakość rejestracji elektrycznej przy jednoczesnym znacznym obniżeniu sztywności. Kilka miękkich interfejsów, w tym implanty w postaci nici i cienkie siatki osiadłe na powierzchni mózgu, już trafia do badań klinicznych u ludzi, pokazując, że delikatniejsza mechanika może współistnieć z zaawansowaną elektroniką.
Powierzchnie, które zapraszają komórki, zamiast je odpychać
Uczynienie urządzeń miększymi to tylko część rozwiązania. Komórki mózgu reagują też na chemiczny „odczucie” powierzchni implantu. Elektronika bioaktywna wykorzystuje to, powlekając elektrody składnikami biologicznymi, które układ nerwowy już zna i akceptuje — na przykład białkami macierzy zewnątrzkomórkowej lub krótkimi cząsteczkami sprzyjającymi wzrostowi nerwów. Takie powłoki mogą zachęcać neurony do zbliżania się do elektrod, tłumić aktywność komórek odpornościowych i zmniejszać powstawanie blizny. Niektóre powłoki zaprojektowano tak, by stopniowo uwalniały leki, na przykład przeciwzapalne lub czynniki wzrostu, dokładnie tam, gdzie są potrzebne, przemieniając bierny przewód w inteligentny interfejs dostarczający leki. Wyzwanie polega na utrzymaniu tych delikatnych warstw stabilnymi i skutecznymi przez lata wewnątrz organizmu.
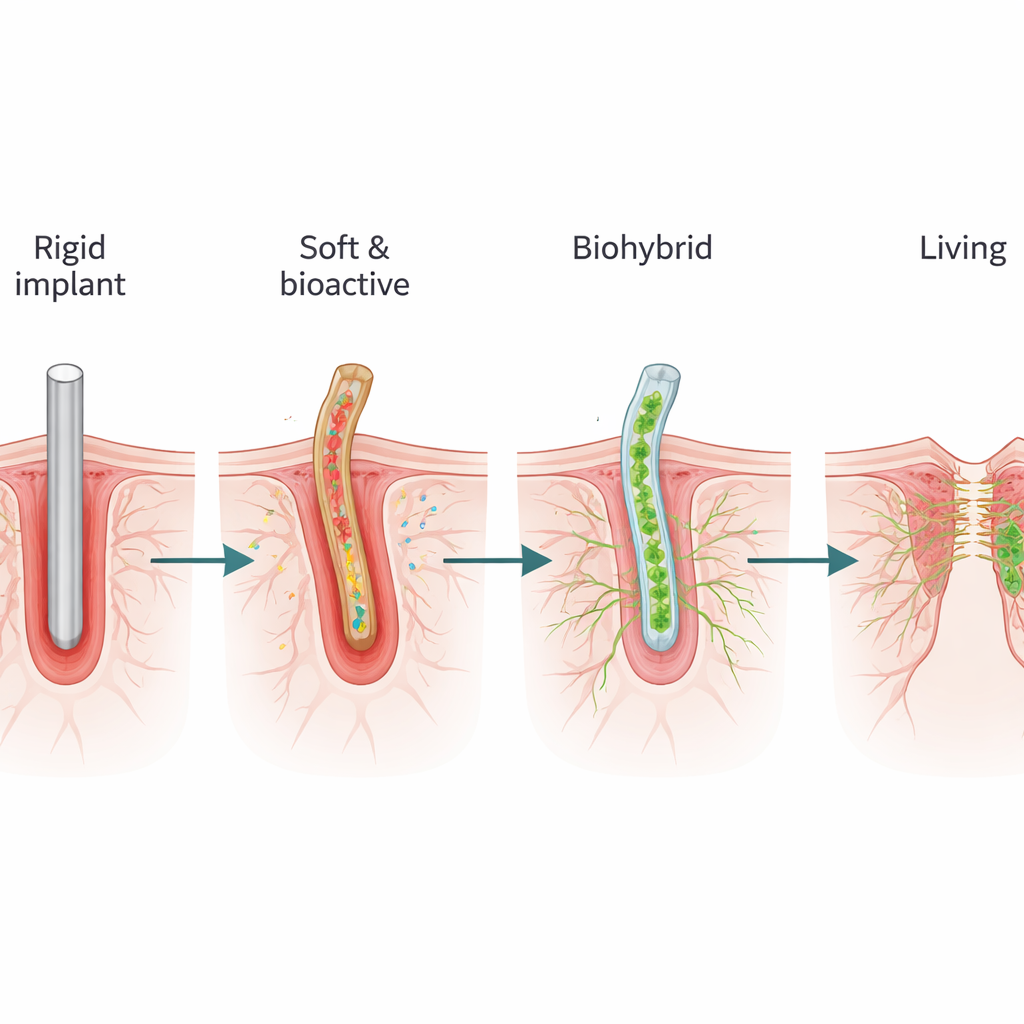
Łączenie żywych komórek z układami elektronicznymi
Idąc dalej, urządzenia „biohybrydowe” włączają do elektroniki faktycznie żywe komórki. W jednej strategii komórki są hodowane na elektrodach przed implantacją, czasem w miękkim hydrożelu imitującym tkankę mózgową. Po wszczepieniu ta żywa warstwa może wydzielać pomocne cząsteczki, przyciągać włókna nerwowe i tworzyć biologiczny pomost między sztywnym sprzętem a tkanką gospodarza. Wczesne wersje, takie jak stożkowate elektrody przyciągające włókna nerwowe do wnętrza, zapewniły stabilne zapisy przez ponad dekadę u ludzi. Nowsze podejścia nasadzają elektrody komórkami macierzystymi, neuronami lub komórkami mięśniowymi, dążąc nie tylko do odczytu lub stymulacji aktywności, lecz także do regeneracji uszkodzonych szlaków i przywracania utraconych funkcji, np. ruchu po urazie nerwu. Systemy te muszą rozwiązać trudne problemy związane z utrzymaniem komórek przy życiu, ukierunkowaniem ich wzrostu i zapewnieniem, że nie będą migrować ani tworzyć niepożądanych połączeń.
W pełni żywe „przewody” dla mózgu
Na najbardziej ambitnym krańcu znajdują się „żywe interfejsy”, zbudowane w całości z materiałów biologicznych i komórek. Tutaj długie pęczki włókien nerwowych hodowanych w laboratorium pełnią rolę żywych kabli, które można wszczepić, by ponownie połączyć obszary mózgu lub zlikwidować przerwy w uszkodzonych nerwach. Zamiast przepuszczać prąd przez metal, te konstrukty wykorzystują naturalne synapsy — punkty kontaktowe między neuronami — do przekazywania sygnałów. W mózgu takie żywe ścieżki zaprojektowano do przenoszenia określonych komunikatów chemicznych, jak dopamina, co rodzi nadzieje na leczenie schorzeń takich jak choroba Parkinsona poprzez odbudowę utraconych obwodów zamiast jedynie maskowania objawów impulsami elektrycznymi. Ponieważ te urządzenia są w pełni biologiczne, dobrze integrują się z tkanką gospodarza, ale wymagają nowych metod monitorowania i kontroli, często opierając się na obrazowaniu i stymulacji z użyciem światła zamiast tradycyjnych przewodów.
Co to oznacza dla przyszłej opieki nad mózgiem i nerwami
Razem miękkie, bioaktywne, biohybrydowe i w pełni żywe interfejsy szkicują mapę drogową ku technologiom nerwowym, które współpracują z ciałem, zamiast z nim walczyć. Miększa mechanika i przyjaźniejsze powierzchnie mogą zmniejszać bliznowacenie i wydłużać żywotność urządzeń; dodanie żywych komórek, a ostatecznie całych tkankowych dróg, mogłoby pozwolić implantom naprawiać lub zastępować uszkodzone obwody, a nie tylko z nich odczytywać. Wciąż pozostaje wiele przeszkód naukowych, produkcyjnych i regulacyjnych, zwłaszcza dla systemów zawierających komórki i w pełni żywych. Kierunek jest jednak jasny: implanty mózgu i nerwów przyszłości będą bardziej przypominać i zachowywać się jak precyzyjnie zaprojektowana tkanka żywa niż jak sztywne urządzenia.
Cytowanie: Boufidis, D., Garg, R., Angelopoulos, E. et al. Bio-inspired electronics: Soft, biohybrid, and “living” neural interfaces. Nat Commun 16, 1861 (2025). https://doi.org/10.1038/s41467-025-57016-0
Słowa kluczowe: interfejsy nerwowe, elektronika biohybrydowa, miękkie implanty, interfejs mózg‑komputer, inżynieria tkankowa