Clear Sky Science · pl
Oświetlając wpływ acetylacji N‑terminalnej: od białka do fizjologii
Jak maleńkie chemiczne znaczniki mogą zmieniać zachowanie białek
Każda komórka w twoim ciele jest wypełniona białkami, które muszą poprawnie się fałdować, trafiać we właściwe miejsce, składać się w molekularne maszyny i być usuwane, gdy ulegną uszkodzeniu. Ten przeglądowy artykuł bada subtelną, lecz bardzo powszechną zmianę chemiczną na jednym końcu wielu białek — zwaną acetylacją N‑terminalną — i pokazuje, jak ta mała „czapeczka” pomaga kontrolować wszystko, od wzrostu komórek i reakcji na stres po rozwój serca i funkcje mózgu.
Kap białkowy, o którym większość z nas nigdy nie słyszała
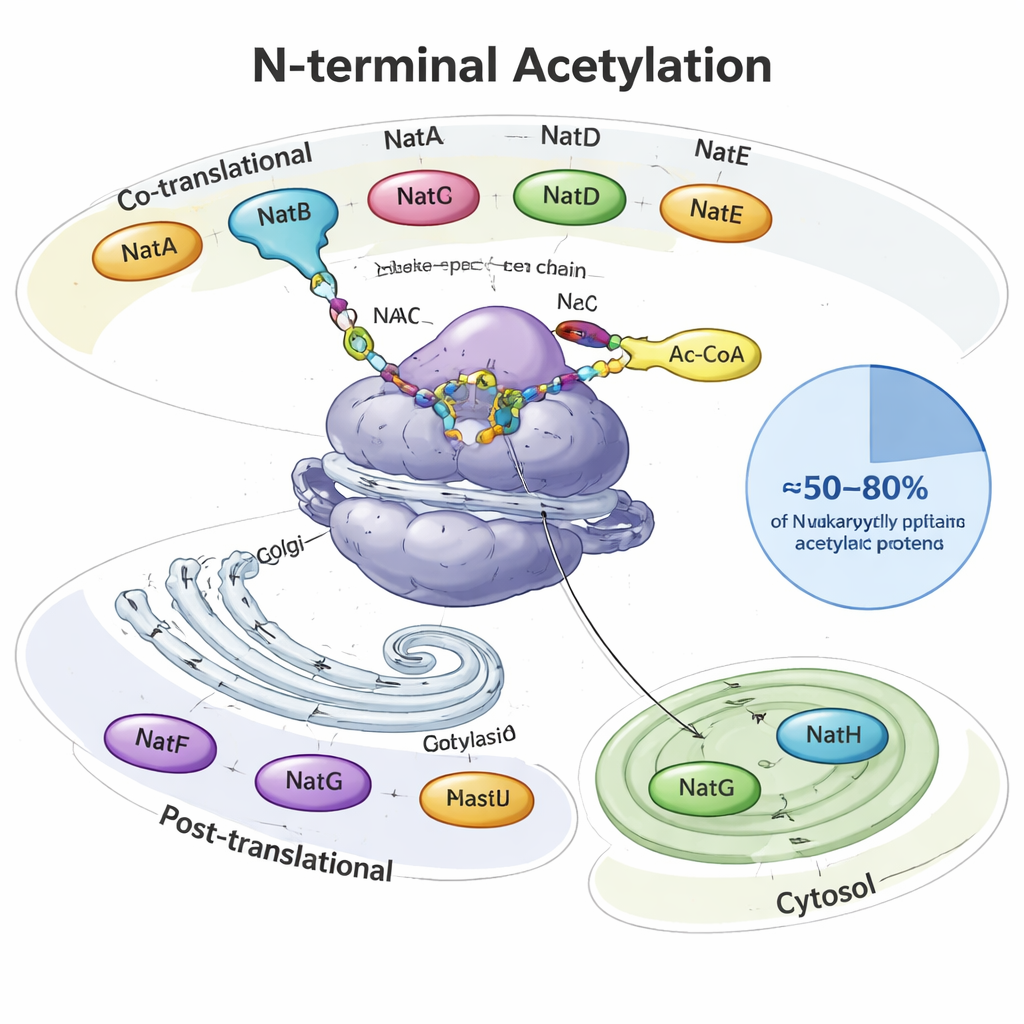
Gdy białko jest syntetyzowane, wyłania się z komórkowej fabryki białek — rybosomu — niczym rosnący włókno. Na samym początku — na końcu N‑terminalnym — wiele białek eukariotycznych otrzymuje grupę acetylową, maleńki dwuwęglowy „kapturek”. Specjalistyczne enzymy zwane N‑terminalnymi acetylotransferazami (NAT) wykonują tę pracę, używając powszechnej metabolicznej cząsteczki (acetyl‑CoA) jako dawcy. U drożdży, roślin i zwierząt osiem głównych typów NAT (NatA–NatH) dzieli między siebie zadania. Niektóre działają, gdy białko jest wciąż syntetyzowane, inne pracują po zakończeniu syntezy i są umiejscowione w konkretnych lokalizacjach, takich jak aparat Golgiego czy plastydy roślinne. Razem modyfikują mniej więcej połowę do czterech piątych wszystkich białek komórkowych, przy czym każdy NAT rozpoznaje preferowane sekwencje startowe składające się z dwóch do czterech aminokwasów.
Wiele enzymów, każdy ze swoją specjalnością
NatA, NatB i NatC to główni wykonawcy, działający przy rybosomie i obejmujący szerokie obszary „acetylomu N‑terminalnego”. Sam NatA może modyfikować około 40% białek ludzkich, zwykle tych, których pierwszy metionin został przycięty. NatB i NatC działają na białka, które zachowują początkowy metionin, lecz różnią się preferencjami względem sąsiednich aminokwasów. Inne NAT są bardziej selektywne: NatD koncentruje się na kilku histonach pakujących DNA, NatF celuje w białka transbłonowe w Golgim, NatG działa wewnątrz plastydów roślinnych, a NatH (NAA80) kończy specjalny, dwuetapowy proces dojrzewania aktyny, głównego składnika szkieletu komórkowego. Artykuł zestawia prace strukturalne i biochemiczne pokazujące, jak podjednostki pomocnicze zakotwiczają te enzymy do rybosomów lub błon i dopasowują, na które białka działają.
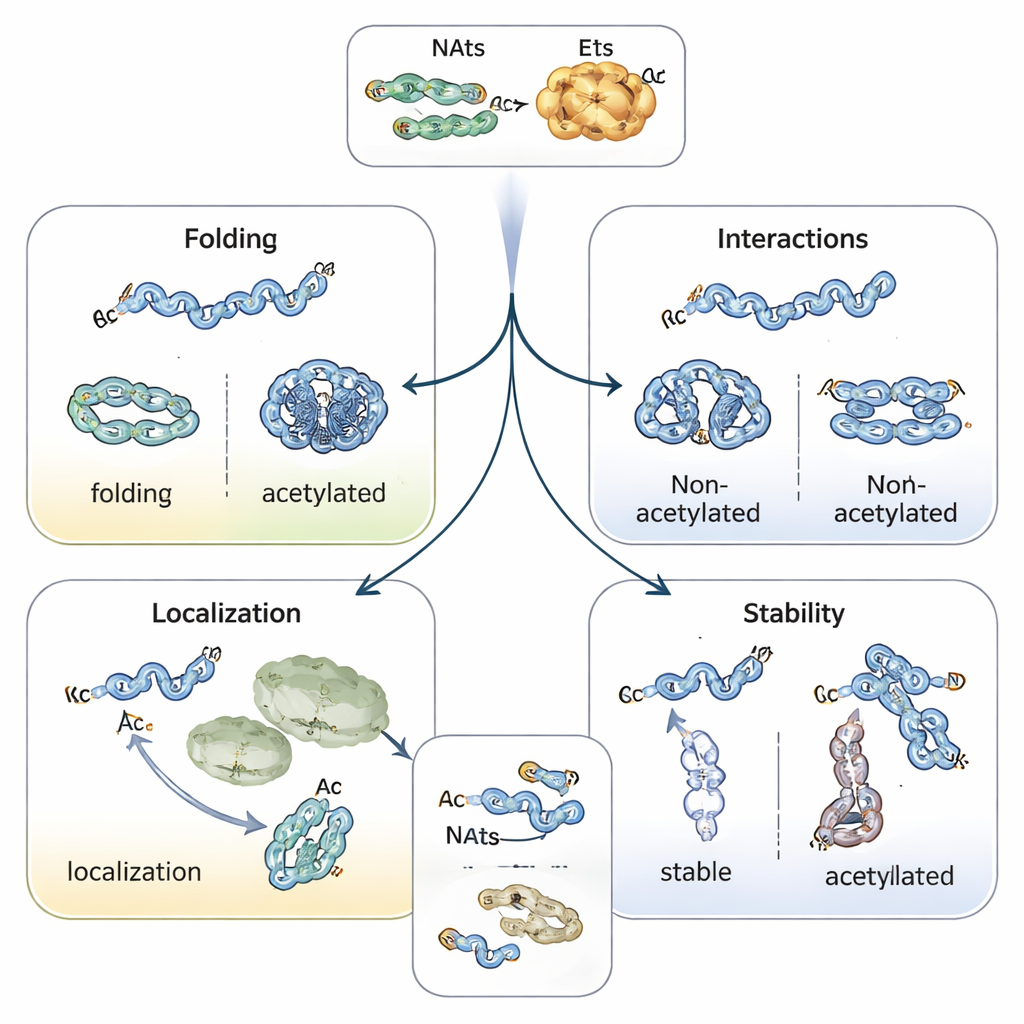
Sterowanie fałdowaniem, lokalizacją i żywotnością białek
Dodanie acetylowego kapturka zmienia chemiczną naturę początku białka, często stabilizując struktury helikalne i wpływając na proces fałdowania. Na przykład białko związane z chorobą Parkinsona — alfa‑synukleina — ma tendencję do mniejszego tworzenia skupisk i przyjmuje bezpieczniejszy kształt, gdy jego koniec N jest acetylowany. Tropomiozyna, partner aktyny, znacznie lepiej wiąże i reguluje włókna aktynowe, gdy jest właściwie acetylowana. U roślin i zwierząt acetylacja N‑terminalna może działać jak etykieta adresowa, pomagając białkom trafiać do chloroplastów, lizosomów czy Golgiego. Być może najbardziej uderzające jest jej znaczenie dla określania czasu życia białek: niechroniony koniec N może być odczytany jako „sygnał degradacji” przez enzymy znakujące ubikwityną, podczas gdy acetylacja może maskować ten sygnał i stabilizować białko — albo w niektórych przypadkach tworzyć warunkowy znacznik rozpoznawany tylko wtedy, gdy białko jest nieprawidłowo sfałdowane lub nie znajduje się w odpowiednim kompleksie.
Od fizjologii komórkowej po rozwój i choroby
Ponieważ acetylacja N‑terminalna obejmuje tak wiele białek, zaburzenia w działaniu NAT mają szerokie konsekwencje dla całych organizmów. Usunięcie NatA, NatB lub NatC w organizmach modelowych często powoduje poważne defekty rozwojowe, zmienione reakcje na stres, a nawet śmiertelność, podczas gdy bardziej wyspecjalizowane enzymy, takie jak NatF i NatH, wywołują węższe problemy, np. zwapnienia mózgu czy utratę słuchu. U ludzi dziedziczne mutacje w kilku genach NAT leżą u podstaw rzadkich zespołów neurorozwojowych z niepełnosprawnością intelektualną, wadami serca czy osłabieniem mięśni. Te same mechanizmy często są nadaktywne w nowotworach, gdzie podwyższone poziomy NAT korelują ze złym rokowaniem i mogą napędzać wzrost guza, przerzuty oraz oporność na terapię. Zmiany w acetylacji N‑terminalnej wpływają także na białka skłonne do agregacji, takie jak alfa‑synukleina i huntingtyna, łącząc tę modyfikację z mechanizmami chorób neurodegeneracyjnych.
Przyszłe kierunki i obietnice medyczne
Autorzy konkludują, że chociaż znamy już większość podstawowych enzymów dodających te N‑terminalne kapturki, wciąż rozumiemy tylko część konkretnych celów białkowych i reguł regulacyjnych. Główny wniosek mówi, że acetylacja na początku białka często chroni je przed przedwczesnym zniszczeniem, jednocześnie tworząc zależne od kontekstu sygnały dla kontroli jakości. Kluczowe otwarte pytania to ustalenie, które ligazy ubikwitynowe odczytują które wzory N‑terminalne, oraz odkrycie, czy istnieje enzym zdolny do usuwania tych kapturków. Ponieważ NAT znajdują się na skrzyżowaniu stabilności białek, regulacji genów i reakcji na stres komórkowy, selektywne inhibitory NAT — a być może przyszłe narzędzia modyfikujące acetylację N‑terminalną konkretnych białek związanych z chorobą — wyłaniają się jako obiecujące kierunki dla nowych terapii w onkologii, chorobach serca i neurodegeneracji.
Cytowanie: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Słowa kluczowe: modyfikacja białka, acetylacja N‑terminalna, kontrola jakości białek, choroby neurodegeneracyjne, biologia nowotworów