Clear Sky Science · pl
Metylacja RNA m6A modyfikuje odpowiedź przeciwwirusową w celiakii
Kiedy wirus i gluten współdziałają
Choroba trzewna bywa postrzegana jako prosty problem żywieniowy: zjesz gluten i twoje jelito ucierpi. To badanie pokazuje jednak głębszą historię, w której powszechny wirus jelitowy i drobny chemiczny znacznik na naszych cząsteczkach RNA współdziałają, popychając układ odpornościowy w kierunku trwałych uszkodzeń. Zrozumienie tej ukrytej warstwy kontroli może pomóc wyjaśnić, dlaczego tylko niektórzy ludzie rozwijają celiakię, oraz wskazać nowe terapie wykraczające poza dietę bezglutenową. 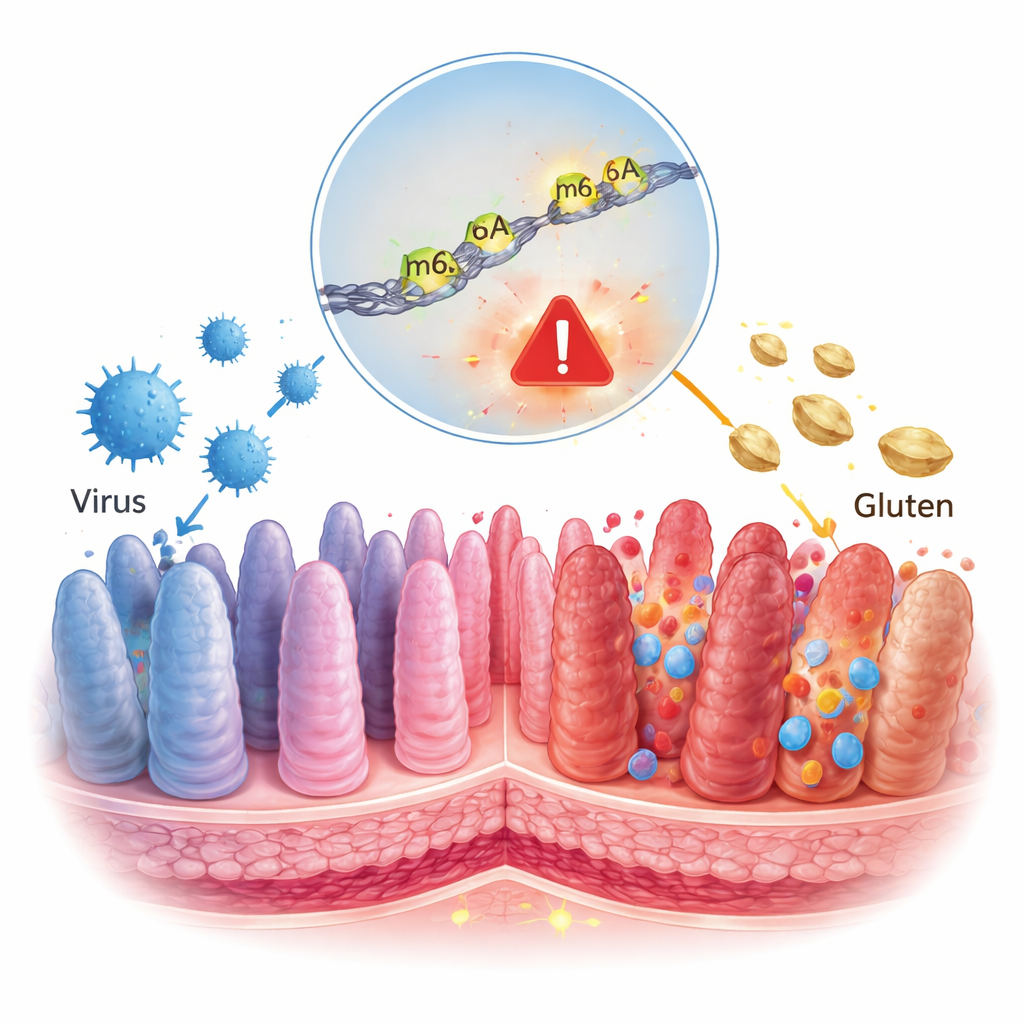
Ukryty znacznik na naszych genetycznych przekazach
Nasze komórki nieustannie odczytują geny i przepisują je na RNA, krótkie „wiadomości”, które mówią komórce, jakie białka ma wytworzyć. Te wiadomości nie są stałe; można je ozdobić chemicznymi znakami działającymi jak zakreślacze, zmieniającymi intensywność odczytu przekazu. Jednym z najpowszechniejszych znaków jest m6A, drobna modyfikacja liter RNA. Wiadomo, że wirusy zmieniają te oznaczenia RNA w zakażonych komórkach, a wcześniejsze prace już łączyły m6A ze sposobem, w jaki gluten wywołuje stan zapalny w jelicie celiaka. Autorzy tej pracy zapytali, czy wirusowo wywołana zmiana m6A może pomóc przestawić układ odpornościowy z tolerancji pokarmowej na atak.
Dane od pacjentów z celiakią
Naukowcy najpierw zbadali krew i biopsje jelita od osób z aktywną celiakią oraz od osób bez celiakii. Stwierdzili, że pacjenci z celiakią mieli wyższe poziomy przeciwciał przeciwko reowirusowi, dwuniciowemu wirusowi RNA, który infekuje jelito, co sugeruje częstszą lub silniejszą ekspozycję. W tkance jelitowej tych pacjentów kluczowe geny ostrzegające o infekcji wirusowej, zwłaszcza gen o nazwie IRF7, były aktywowane na wyższym poziomie, razem z cząsteczkami zapalnymi takimi jak STAT1 i chemoatraktantem komórek odpornościowych CXCL10. Jednocześnie mechanizmy dodające i odczytujące znaki m6A były bardziej aktywne, a całkowity poziom m6A na RNA był wyższy. Ekspresja genów przeciwwirusowych rosła i malała równolegle z genami związanymi z m6A, co sugeruje, że ten sam system kontroli może napędzać zarówno obronę przeciwwirusową, jak i uszkodzenia autoimmunologiczne.
Jak gluten wzmacnia alarm wirusowy
Aby zbadać związek przyczynowo-skutkowy, zespół zbudował model podobny do celiakii w komórkach jelitowych hodowanych w laboratorium. Naśladowali zakażenie wirusowe, używając syntetycznego dwuniciowego RNA, a następnie dodali strawione fragmenty glutenu podobne do tych, które pojawiają się w jelicie po posiłku. Sam wirusowy substytut zwiększał zarówno IRF3, jak i IRF7, dwa główne przełączniki odpowiedzi przeciwwirusowej. Jednak po dodaniu glutenu IRF7 wykazywał silny dodatkowy wzrost, podczas gdy IRF3 nie. Naukowcy odkryli, że w tych warunkach wzrosła liczba znaków m6A w określonym regionie RNA IRF7, oraz że to RNA fizycznie wchodziło w interakcję z enzymem zapisującym m6A (METTL3) i enzymem usuwającym te znaki (ALKBH5). Zwiększenie m6A, zarówno przez dodanie więcej METTL3, jak i przez zmniejszenie ALKBH5, podnosiło poziomy IRF7 jeszcze bardziej, łącząc bezpośrednio synergiczne działanie glutenu i wirusa z tą modyfikacją RNA. 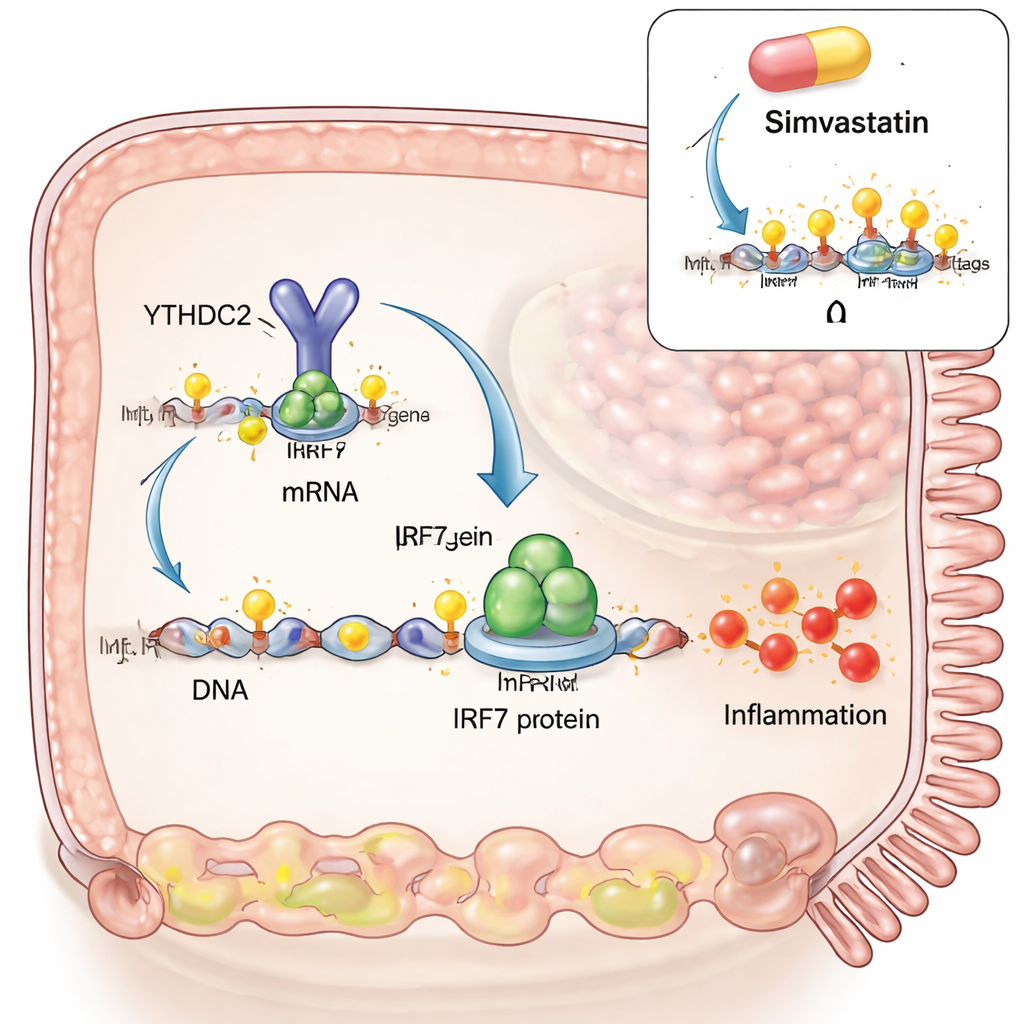
Molekularny pośrednik i zaskakujący lek
Następnie autorzy zapytali, w jaki sposób znaki m6A na RNA IRF7 rzeczywiście zmieniają zachowanie komórki. Zaprojektowali wersję RNA IRF7 kodującą ten sam białkowy kod, ale pozbawioną miejsc m6A. Ten RNA dawał podobne ilości transkryptu, ale znacznie mniej białka IRF7 i nie potrafił uruchomić genów zapalnych takich jak STAT1 i CXCL10. Brakującym ogniwem był białkowy czytnik zwany YTHDC2, który normalnie wiąże m6A w obrębie regionu kodującego i pomaga efektywnej translacji do białka. Bez miejsc m6A YTHDC2 nie mógł się już przyłączyć do RNA IRF7. Zablokowanie enzymu zapisującego m6A, METTL3, w modelu komórkowym zmniejszyło poziom białka IRF7 i CXCL10, obniżając odpowiedź zapalną. Lek obniżający poziom cholesterolu, simwastatyna, który ostatnio wykazano, że redukuje m6A w innych tkankach, również obniżył m6A na RNA IRF7, zmniejszył ilość białka IRF7 w komórkach i osłabił geny związane z IRF7 w świeżo pobranych biopsjach jelita od pacjentów z celiakią hodowanych egz vivo. Porównania wielkoskalowe profili ekspresji genów sugerowały, że simwastatyna przesuwa tkankę celiakalną w stronę profilu bardziej zbliżonego do tego u pacjentów na diecie bezglutenowej.
Co to oznacza dla osób z celiakią
Ta praca kreśli obraz, w którym wirus jelitowy i gluten działają razem na precyzyjnie regulowanej warstwie kontroli RNA. U osób podatnych zakażenie wirusowe zdaje się zwiększać znakowanie m6A RNA IRF7 w komórkach jelitowych. Następnie ekspozycja na gluten dodatkowo wzmacnia ten oznakowany sygnał, prowadząc do większej ilości białka IRF7, silniejszych alarmów przeciwwirusowych i wyższych poziomów cząsteczek zapalnych, które przyczyniają się do autoimmunologicznego ataku na wyściółkę jelita. Poprzez stłumienie znaków m6A — genetycznie lub za pomocą leku takiego jak simwastatyna — reakcję łańcuchową można złagodzić, przynajmniej w modelach laboratoryjnych i egz vivo. Dla czytelników niebędących specjalistami kluczowy przekaz jest taki, że celiakia to nie tylko kwestia tego, co jesz, lecz także tego, jak infekcje i subtelne chemiczne modyfikacje RNA wpływają na decyzję układu odpornościowego o tolerancji lub ataku. Celowanie w te znaczniki RNA mogłoby kiedyś uzupełniać dietę bezglutenową i inspirować nowe terapie dla szerszego zakresu chorób autoimmunologicznych.
Cytowanie: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Słowa kluczowe: choroba trzewna (celiakia), metylacja RNA, odporność przeciwwirusowa, IRF7, simwastatyna