Clear Sky Science · pl
CRISPR-AuNP: optymalizacja fizykochemiczna platformy z nanocząstkami złota dla opłacalnej i modułowej niewirusowej edycji genów w HSPC
Umożliwienie edycji genów większej liczbie pacjentów
Narzędzia do edycji genów, takie jak CRISPR, już zmieniły życie osób z dziedzicznymi chorobami krwi, ale terapie te pozostają kosztowne, technicznie wymagające i w dużej mierze ograniczone do kilku wyspecjalizowanych ośrodków. W artykule opisano nowy sposób dostarczania CRISPR do krwiotwórczych komórek macierzystych przy użyciu maleńkich cząstek na bazie złota, które można przygotować na ławce laboratoryjnej w zaledwie kilka godzin. Celem jest uproszczenie, obniżenie kosztów i ułatwienie wdrażania potężnych metod edycji genów w większej liczbie miejsc na świecie.
Dlaczego komórki macierzyste krwi są ważne
Krwiootwórcze komórki macierzyste i progenitorowe żyją w szpiku kostnym i nieustannie odnawiają wszystkie różne typy komórek krwi w organizmie. Jeśli lekarze będą mogli bezpiecznie naprawić mutacje powodujące choroby w tych komórkach, jednorazowe leczenie mogłoby zapewnić dożywotnie wyleczenie schorzeń takich jak anemia sierpowata czy niektóre niedobory odporności. Obecnie najczęściej stosowaną metodą wprowadzania CRISPR do tych komórek jest elektroporacja — proces wykorzystujący impulsy elektryczne do tworzenia otworów w błonach komórkowych. Choć skuteczna, elektroporacja jest agresywna dla komórek, wymaga drogiego sprzętu i specjalistycznych odczynników oraz trudno ją skalować lub wdrożyć w miejscach o ograniczonych zasobach. Bezpieczniejsze wektory wirusowe sprawdzają się w wielu terapiach genowych, ale są mniej odpowiednie do dostarczania CRISPR, ponieważ długo produkują narzędzia edycyjne, zwiększając ryzyko zmian pozabiegowych.
Budowa maleńkiego nośnika z złota
Naukowcy postanowili udoskonalić wcześniej opisany system z nanocząstkami złota, który przenosił składniki CRISPR na swojej powierzchni. W wcześniejszych projektach RNA prowadzące białko tnące CRISPR było zakotwiczone bezpośrednio do jądra złotego, a następnie parowane z białkiem Cas9. Taki układ działał przyzwoicie dla jednego typu enzymu CRISPR, ale słabo sprawdzał się z Cas9, kluczowym dla wielu strategii terapeutycznych. Analizując zachowanie Cas9 i jego prowadzącego RNA w kwaśnych warunkach używanych podczas składania cząstek, zespół odkrył, że duplex prowadzącego RNA stawał się niestabilny na powierzchni złota, co skutkowało niewielką lub żadną ilością aktywnego Cas9 przyczepionego do cząstki. Mikroskopia konfokalna zasugerowała też, że polimerowa powłoka, mająca pomóc cząstkom uciec z pęcherzyków komórkowych, złuszczała się zanim zdążyła zadziałać.
Stopniowy redesign platformy
Aby przezwyciężyć te problemy, naukowcy przebudowali system od podstaw w trzech etapach. Po pierwsze, zamiast kotwiczyć gołe RNA do złota i dopiero potem dodawać białko, najpierw tworzyli kompletne kompleksy rybonukleoproteinowe CRISPR (białko plus prowadzące RNA), a dopiero potem zetknęli je z powierzchnią złota. Zidentyfikowali lekko kwaśne warunki, które pozwalały tym kompleksom wiązać się z cząstkami przy jednoczesnym zachowaniu aktywności białka tnącego. Następnie otoczyli naładowane cząstki specjalnie zaprojektowanymi polimerami łączącymi łańcuchy dodatnio naładowane — potrzebne do ucieczki z pęcherzyków komórkowych — z giętkimi, hydrofilowymi fragmentami polietylenoglikolu, które zapobiegają koagulacji. Poprzez pomiary rozmiaru, ładunku powierzchniowego i zawartości białka wykazali, że można powtarzalnie załadować dziesiątki kompleksów CRISPR na cząstkę przy utrzymaniu stabilności w roztworze.
Przełamywanie obrony komórki
Nawet przy lepszym załadowaniu, cząstki drugiej generacji wciąż miały problem z kluczową przeszkodą: wydostaniem CRISPR z wewnętrznych pęcherzyków komórkowych do miejsca, gdzie znajduje się DNA. Zespół systematycznie dostroił więc chemię warstwy polimerowej i stosunek między grupami dodatnimi na polimerze a grupami ujemnymi w kompleksie CRISPR. Odkryli, że dodanie większej liczby krótkich łańcuchów polietylenoglikolu i kontrolowanej liczby siarkowych kotwic poprawiało zarówno stabilność cząstek, jak i zdolność do zaburzania błon endosomalnych bez uszkadzania komórek. W ostatecznym, trzeciej generacji projekcie najpierw tworzyli zwartościowe kompleksy CRISPR z polimerem, a następnie przyłączali je do skoncentrowanych jąder ze złota. Mikroskopia elektronowa pokazała cienką powłokę CRISPR i polimeru wokół każdej złotej kulki, a obrazowanie w żywych komórkach macierzystych potwierdziło, że ładunek może wydostać się do wnętrza komórki i dotrzeć do jądra.
Wyniki edycji z różnymi narzędziami CRISPR
Aby przetestować skuteczność zoptymalizowanych cząstek, badacze celowali w gen beta-2-mikroglobulina, który koduje białko obecne na powierzchni niemal wszystkich komórek krwi i jest łatwy do zmierzenia cytometrią przepływową. Używając platformy trzeciej generacji osiągnęli ponad 10% precyzyjnych zaburzeń tego genu w pierwotnych ludzkich krwiotwórczych komórkach macierzystych i progenitorowych — poziomy uznawane za istotne dla wielu zastosowań terapeutycznych — przy jednoczesnym utrzymaniu wysokiej przeżywalności komórek. Chociaż ta wydajność jest niższa niż to, co można osiągnąć przy elektroporacji, system z złotem nie wymagał specjalistycznego sprzętu i powodował minimalny stres komórek. Co ważne, ta sama platforma mogła być używana z różnymi białkami CRISPR, w tym Cas9, Cas12a i nowszym enzymem Cas12a-M29-1, osiągając podobne poziomy edycji i bez wykrywalnej toksyczności, co podkreśla modułowy charakter konstrukcji.
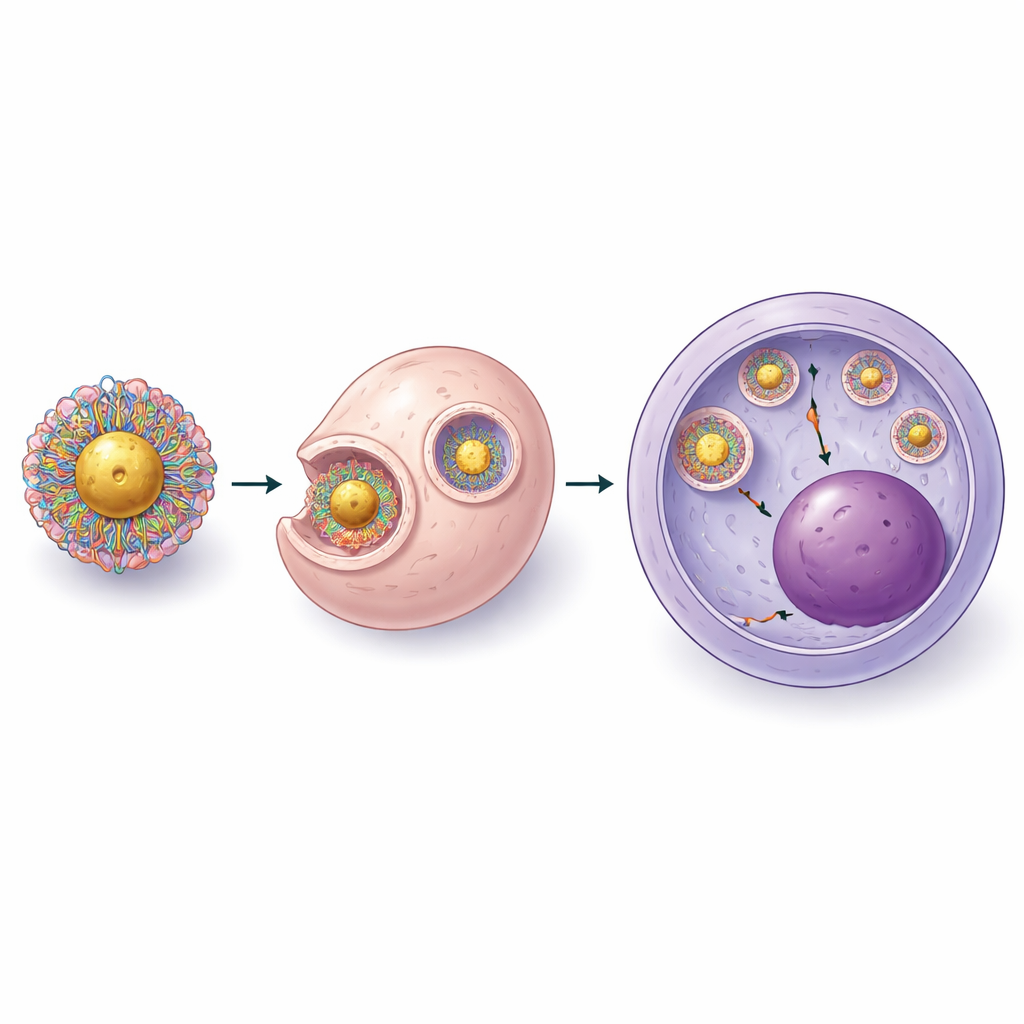
Co to może znaczyć dla przyszłych terapii
Mówiąc wprost, praca ta pokazuje, że można zbudować mały, starannie zaprojektowany nośnik na bazie złota, który dostarczy narzędzia CRISPR do wrażliwych krwiotwórczych komórek macierzystych bez użycia prądu czy wirusów, korzystając z gotowych materiałów za mniej niż siedemdziesiąt dolarów na milion komórek. Choć potrzebne są dalsze udoskonalenia, aby dorównać efektywności najlepszych obecnych metod klinicznych — zwłaszcza przy chorobach wymagających bardzo wysokiego udziału skorygowanych komórek — ta platforma składana na ławce obniża praktyczne bariery dla przeprowadzania zaawansowanej edycji genów. Przy dalszych poprawkach i testach bezpieczeństwa takie nanocząstki mogłyby pomóc rozszerzyć korzyści terapii opartych na CRISPR poza ośrodki specjalistyczne, czyniąc leczenie o charakterze leczniczym bardziej dostępne dla pacjentów na całym świecie.
Cytowanie: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Słowa kluczowe: edycja genów CRISPR, nanocząstki złota, hematopoetyczne komórki macierzyste, dostarczenie niewirusowe, nanomedycyna