Clear Sky Science · pl
Przemyślenie genomiki dystrofii mięśniowej twarzowo-obojczykowo-ramiennej w erze telomer-do-telomer: pułapki w ukrytym krajobrazie powtórzeń D4Z4
Dlaczego ta historia o chorobie mięśni ma znaczenie
Dystrofia mięśniowa twarzowo-obojczykowo-ramienna (FSHD) jest jedną z częstszych dziedzicznych chorób prowadzących do zaników mięśni, często osłabiając mięśnie twarzy i barków u pozornie zdrowych młodych dorosłych. Przez lata badacze koncentrowali się na pojedynczym odcinku DNA blisko końca chromosomu 4 jako winowajcy. Nowe badanie pokazuje, że obraz jest znacznie bardziej skomplikowany: podobne powtórzenia DNA występują rozsiane po całym genomie, a wiele standardowych testów laboratoryjnych nie potrafi ich odróżnić. Zrozumienie tego ukrytego krajobrazu jest niezbędne dla dokładnej diagnostyki, lepszych badań i w końcu bezpieczniejszych terapii.
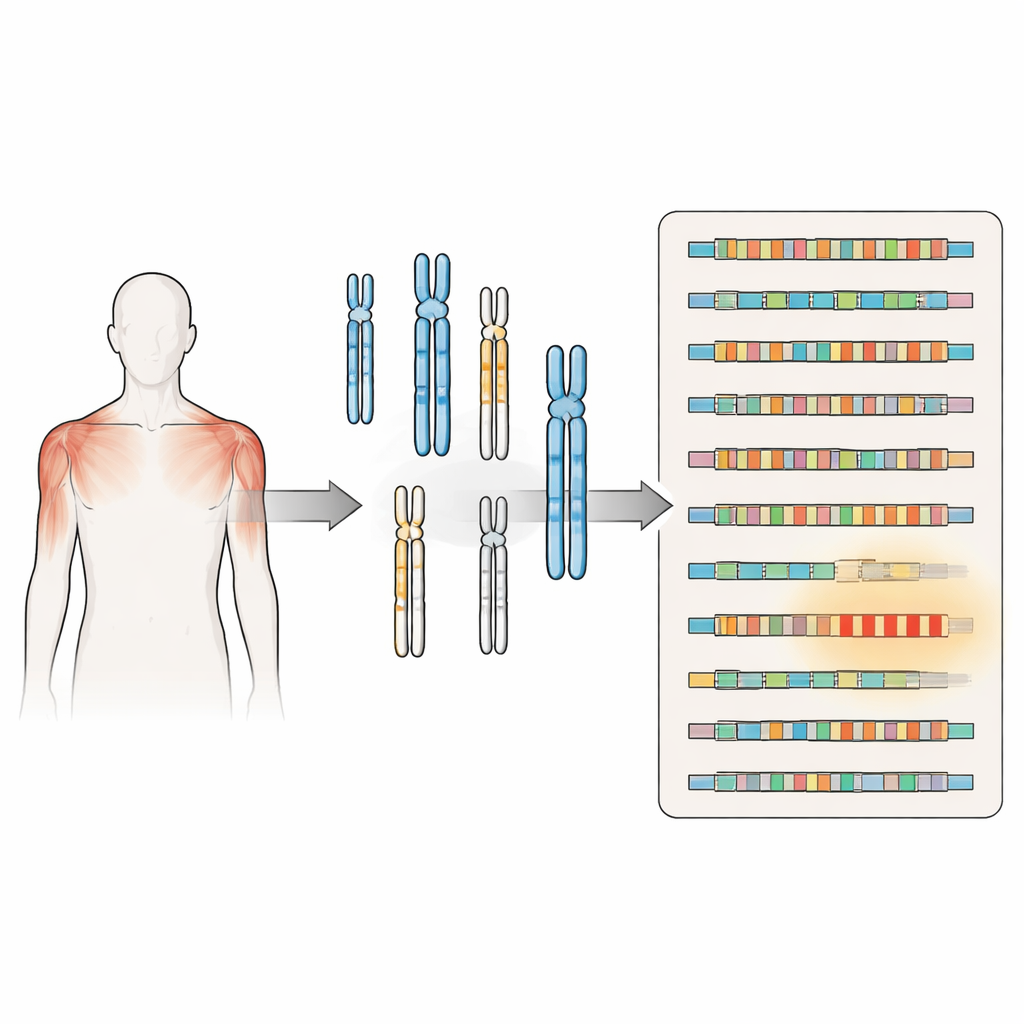
Dokładniejsze spojrzenie na zagadkowe schorzenie mięśni
FSHD od dawna wiązano ze skracaniem powtarzalnej sekwencji DNA zwanej D4Z4 blisko końca chromosomu 4. Gdy ten region powtórzeń kurczy się poniżej pewnego rozmiaru i występuje na określonym tle genetycznym, umożliwia produkcję białka zwanego DUX4, które może uszkadzać komórki mięśniowe. Druga postać choroby powstaje, gdy mutacje dotyczą genów normalnie utrzymujących ten region w zwartej, wyciszonej formie, co ponownie pozwala na pojawienie się DUX4. Obie drogi zbiegają się w tym samym problemie: gen, który powinien być w dużej mierze wyłączony w mięśniach dorosłych, staje się sporadycznie aktywny, przyczyniając się do osłabienia i zaniku mięśni.
Ukryte powtórzenia w całym genomie
Wcześniejsze mapy ludzkiego genomu były niekompletne, zwłaszcza w regionach bogatych w powtórzenia DNA przy końcach chromosomów i w pobliżu centromerów. Korzystając z nowego złożenia genomu ludzkiego telomer-do-telomer, które wypełnia te luki, autorzy ponownie przeskanowali cały genom, używając sekwencji D4Z4 z chromosomu 4 jako wzorca wyszukiwania. Odkryli klastry i pojedyncze kopie powtórzeń podobnych do D4Z4 na co najmniej dziesięciu dodatkowych chromosomach. Niektóre z tych powtórzeń są strukturalnie kompletne i leżą obok sygnałów, które mogłyby stabilizować RNA podobne do DUX4, co sugeruje, że w odpowiednich warunkach mogą one wytwarzać spokrewnione białka lub cząsteczki RNA.
Kiedy testy laboratoryjne widzą więcej niż jedno miejsce naraz
Badania nad FSHD i diagnostyka często opierają się na testach, które amplifikują specyficzne fragmenty DNA lub RNA za pomocą krótkich starterów, strategii znanej jako PCR. Te startery zostały pierwotnie zaprojektowane w założeniu, że powtórzenia D4Z4 występują tylko na chromosomach 4 i 10. Łącząc przewidywania komputerowe z eksperymentami na komórkach niosących pojedyncze ludzkie chromosomy, autorzy pokazują, że wiele szeroko stosowanych zestawów starterów wiąże się nie tylko z regionem związanym z chorobą na chromosomie 4, lecz także z podobnymi powtórzeniami rozsianymi po genomie. Startery skierowane do głównego eksonu DUX4 lub sąsiednich długich RNA niekodujących często amplifikują produkty z kilku chromosomów jednocześnie, co uniemożliwia ustalenie, skąd dokładnie pochodzi dany sygnał.
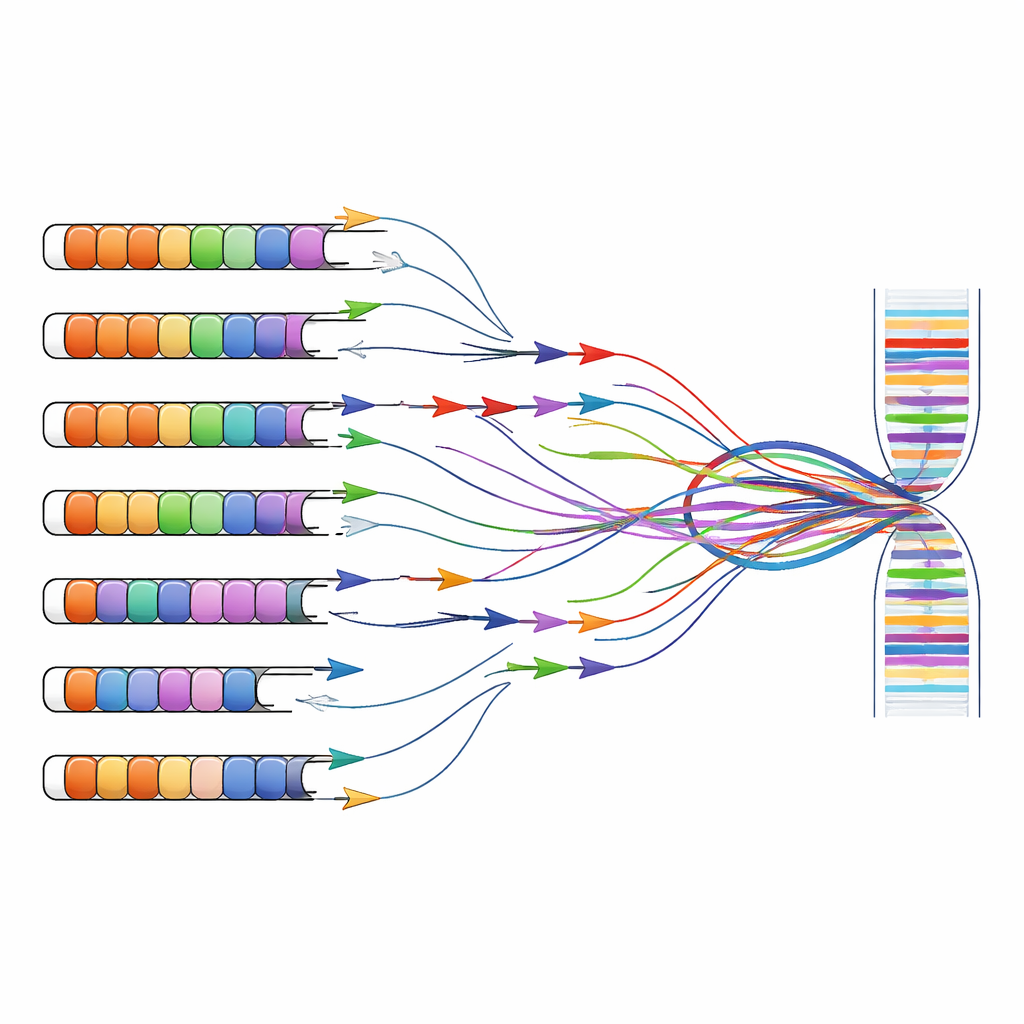
Przemyślenie narzędzi diagnostycznych i badawczych
Ten problem wielu lokalizacji wykracza poza podstawowe badania i dotyczy także kliniki. Nowsze testy mierzące metylację DNA (znak chemiczny związany z wyciszaniem genów) lub wykorzystujące sekwencjonowanie krótkich odczytów często łączą sygnały z wielu niemal identycznych powtórzeń. W rezultacie pomiary „metylacji D4Z4” czy „transkryptów DUX4” w publicznych zbiorach danych mogą faktycznie odzwierciedlać mieszaninę wkładów z chromosomu 4, chromosomu 10 i innych miejsc. Autorzy argumentują, że aby poprawnie powiązać zmiany genetyczne z objawami, konieczne jest teraz stosowanie metod świadomych powtórzeń, które wyróżniają poszczególne locus — na przykład sekwencjonowania długich odczytów, które może obejmować całe bloki powtórzeń i uchwycić ich wzory metylacji oraz produkty RNA w całości.
Co to znaczy dla pacjentów i przyszłych terapii
Badanie nie obala kluczowej roli skróconego regionu D4Z4 na chromosomie 4 w FSHD, ale pokazuje, że ten region znajduje się w zatłoczonym sąsiedztwie podobnych sekwencji. Sygnały niegdyś uważane za dowód aktywności w locus chorobowym mogą w rzeczywistości częściowo pochodzić od jego genomowych „kuzynów”. Dla pacjentów oznacza to, że najbardziej wiarygodne narzędzia diagnostyczne będą te, które fizycznie rozróżniają dokładny chromosom i układ powtórzeń zaangażowany, zamiast polegać wyłącznie na pośrednich pomiarach. Dla naukowców i twórców leków podkreśla to potrzebę bardzo specyficznych projektów, które unikają przypadkowego celowania w nieszkodliwe powtórzenia gdzie indziej w genomie. W erze telomer-do-telomer zrozumienie i leczenie FSHD zależeć będzie od dostrzeżenia pełnego krajobrazu powtórzeń, nie tylko pojedynczego punktu orientacyjnego.
Cytowanie: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Słowa kluczowe: dystrofia mięśniowa twarzowo-obojczykowo-ramienna, powtórzenia D4Z4, DUX4, genom telomer-do-telomer, diagnostyka genetyczna