Clear Sky Science · pl
Sztuczne chaperony: od konwencjonalnych projektów po inteligentne systemy
Pomoc dla cząsteczek, by składały się właściwie
W każdej żywej komórce długie łańcuchy białek i materiału genetycznego muszą zginać się i skręcać, aby przyjąć odpowiednie kształty potrzebne do prawidłowego działania. Gdy ulegają nieprawidłowemu fałdowaniu, mogą się zlepiać, tracić swoje funkcje, a nawet wywoływać choroby, takie jak neurodegeneracja. Przyroda korzysta z molekuł „chaperonów”, które porządkują ten mikroskopijny tłum, lecz naturalni pomocnicy są kosztowni, wrażliwi i trudni do zastosowania poza komórką. Ten artykuł opisuje, jak naukowcy tworzą dziś sztuczne chaperony — zaprojektowane narzędzia, które potrafią nakierować zbłąkane cząsteczki z powrotem na właściwe tory i które można włączać i wyłączać jak inteligentne systemy.
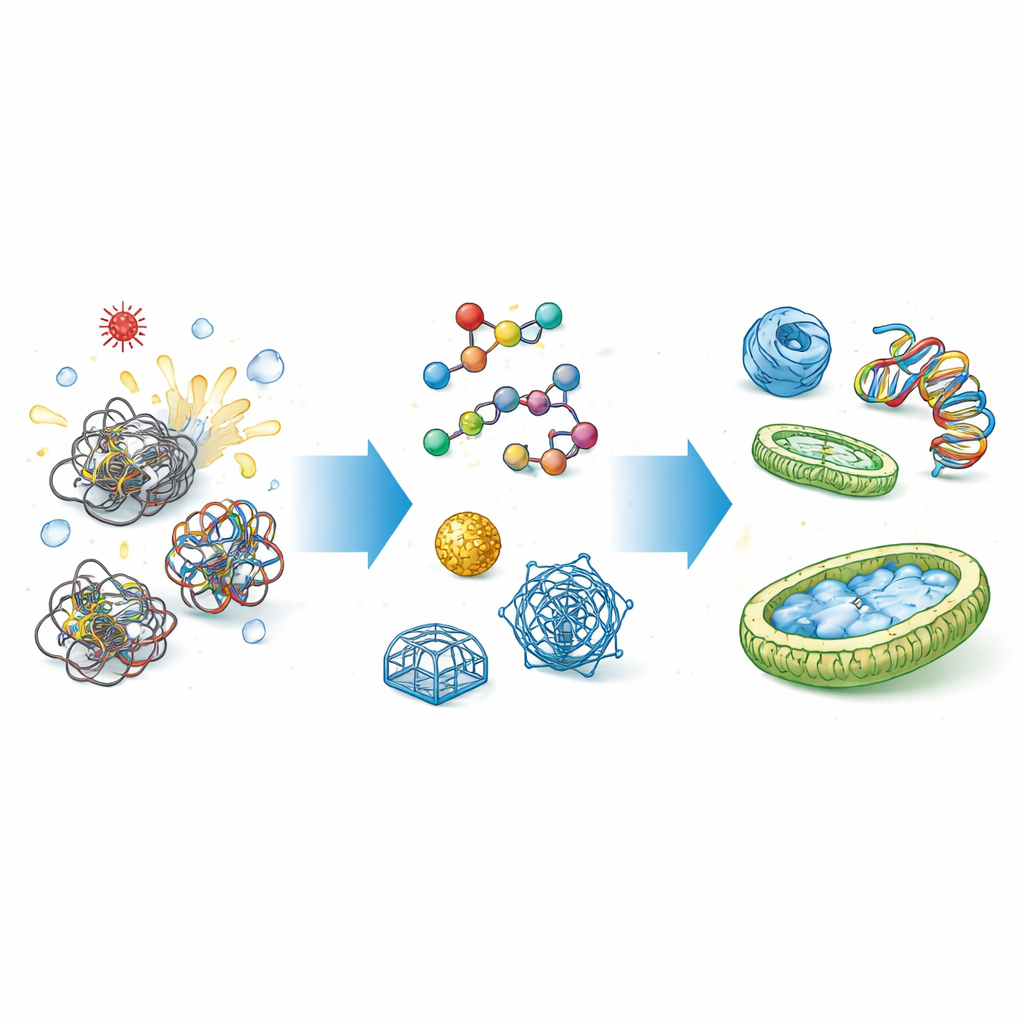
Dlaczego komórki potrzebują pomocników fałdowania
Białka i kwasy nukleinowe (takie jak DNA i RNA) nie rodzą się w pełni ukształtowane; muszą zwijać się w skomplikowane struktury trójwymiarowe. Droga do tych kształtów jest pełna pułapek, gdzie łańcuchy mogą utknąć lub się zlepiać. Naturalne chaperony, takie jak białka szoku cieplnego, chwytają te wiotkie łańcuchy, osłaniają ich lepkie fragmenty i zapewniają chronioną przestrzeń do prawidłowego fałdowania. Podobne funkcje występują w przypadku kwasów nukleinowych, gdzie chaperony pomagają rozplątać węzły i przeorganizować pary zasad. Gdy ta kontrola zawodzi, skutkiem mogą być utrata funkcji, toksyczne agregaty, choroby oraz kosztowne niepowodzenia w przemysłowej produkcji białek.
Od prostych chemikaliów do projektowanych polimerów
Pierwsze sztuczne chaperony to stosunkowo proste związki chemiczne zmieniające warunki otoczenia cząsteczek. Niektóre rozpuszczalniki i detergenty potrafią ukryć lepkie regiony białek, zapobiegać agregacji i dać im drugą szansę na poprawne ponowne złożenie. Niektóre małe kwasy tłuszczowe, na przykład, pomagają mutantowemu kolagenowi fałdować się prawidłowiej i łagodzą stres wewnątrz komórek dotkniętych chorobami dziedzicznymi. Jednak takie chemiczne pomoce zwykle trzeba stosować w wysokich dawkach, trudno je dopasować do konkretnych celów i mogą zaburzać inne składniki w złożonych mieszankach. Aby uzyskać większą kontrolę, badacze zwrócili się ku większym, szytym na miarę polimerom — elastycznym łańcuchom, które można ozdabiać naładowanymi lub hydrofilowymi odgałęzieniami, by bardziej selektywnie obejmować DNA, RNA i białka.
Zestaw narzędzi: polimery i nanogele
Projektowane polimery mogą przyłączać się do naładowanych szkieletów DNA lub odsłoniętych miejsc na białkach, wygładzając krajobraz energetyczny tak, że te molekuły szybciej i pewniej znajdują preferowane kształty. W przypadku kwasów nukleinowych polimery kationowe (dodatnio naładowane) mogą neutralizować odpychanie między nićmi, przyspieszając wiązanie zasad, wymianę nici oraz tworzenie egzotycznych struktur wykorzystywanych w obliczeniach DNA i biosensorach. Dla białek polimery takie jak specjalnie ukształtowane pętle poli(etylenu glikolu) czy syntetyczne polianiony mogą przewyższać niektóre naturalne chaperony w zapobieganiu agregacji wywołanej ciepłem. Inne systemy łączą elastyczne polimerowe chaperony z krótkimi peptydami, aby przebudowywać błony podobne do komórkowych w płaskie nanoarkusze lub pęcherzyki, tworząc odwracalne platformy dwuwymiarowe do dostarczania ładunku i inżynierii tkankowej.

Budowa inteligentnych, przełączalnych chaperonów
Ponad samym utrzymywaniem i uwalnianiem klientów, nowoczesne sztuczne chaperony potrafią reagować na otoczenie. Naukowcy zbudowali nanogele, nanocząstki i sieci polimerowe, których uścisk na białkach wzmacnia się lub słabnie wraz ze zmianami kwasowości, temperatury, światła czy obecności konkretnych związków, jak glukoza. Na przykład niektóre micele stają się bardziej hydrofobowe przy łagodnie kwaśnym pH, naśladując naturalne chaperony przez wychwytywanie zagrożonych białek i uwalnianie ich, gdy pH znów się zmieni. Polimery reagujące na temperaturę zapadają się lub rozszerzają po przekroczeniu progu, pozwalając na sekwestrację uszkodzonych białek w jednym zakresie temperatur i uwalnianie zrefoldowanych w innym. Grupy czułe na światło mogą działać jako molekularne przełączniki, włączając lub wyłączając ścieżki składania DNA błyskiem, podczas gdy cząstki reagujące na cukry mogą chronić terapeutyczny hormon i uwalniać go preferencyjnie przy wysokim poziomie glukozy we krwi.
Co to oznacza dla medycyny i technologii
Artykuł konkluduje, że sztuczne chaperony ewoluują od prostych stabilizatorów chemicznych do wysoce programowalnych „narzędzi molekularnych”, które potrafią rozpoznawać, chronić i przebudowywać różne struktury biologiczne na żądanie. Poprzez ostrożne balansowanie sił przyciągania i odpychania oraz wprowadzanie czułości na sygnały takie jak pH, ciepło, światło czy stres mechaniczny, te systemy mogą składać docelowe molekuły we właściwym miejscu i czasie. W dłuższej perspektywie takie inteligentne pomocniki mogą uczynić przemysłową produkcję białek bardziej wydajną, wyostrzyć biosensory, zasilić komputery molekularne i zaoferować nowe sposoby zwalczania chorób związanych z nieprawidłowym fałdowaniem białek — potencjalnie w tym schorzeń takich jak choroba Alzheimera — jednocześnie wiernie naśladując subtelną kontrolę, jaką komórki już osiągają.
Cytowanie: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Słowa kluczowe: sztuczne chaperony, fałdowanie białek, inteligentne polimery, nanomedycyna, materiały reagujące na bodźce