Clear Sky Science · pl
Radzenie sobie z cuproptozą: od przearanżowania metabolizmu do terapeutycznego wykorzystania w nowotworach
Kiedy pomocny metal obraca się przeciwko rakowi
Miedź jest powszechnie znana jako składnik przewodów elektrycznych i instalacji wodociągowych, ale działa też dyskretnie w naszych komórkach, pomagając enzymom w wytwarzaniu energii i chroniąc przed uszkodzeniami. Ten artykuł przeglądowy opisuje zaskakujący zwrot: przy odpowiednich warunkach nadmiar miedzi może skłonić komórki nowotworowe do szczególnego rodzaju śmierci. Zrozumienie tego procesu — nazwanego „cuproptozą” — może otworzyć nowe możliwości leczenia guzów, które wymknęły się standardowym terapiom.
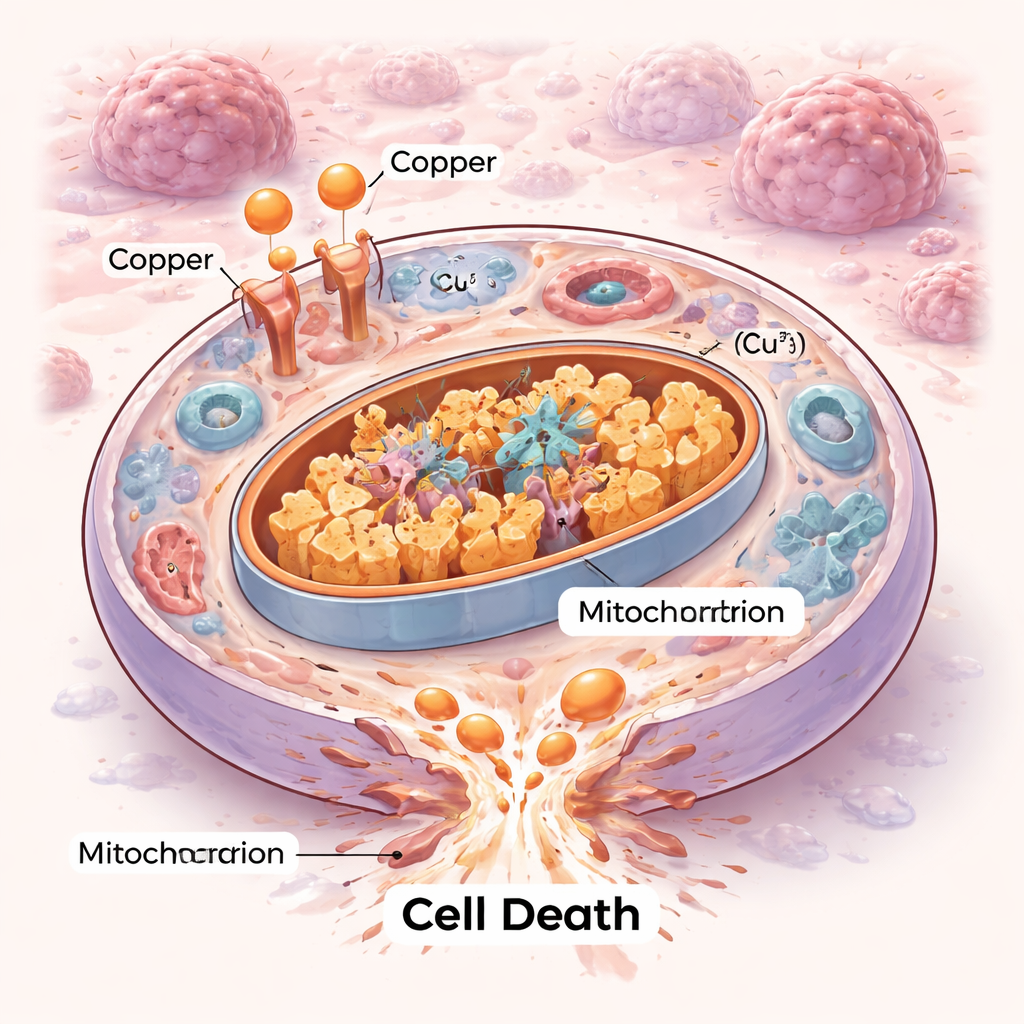
Nowy sposób, w jaki komórki mogą umierać
Komórki nie umierają wszystkie w ten sam sposób. Przez dekady naukowcy zmapowali uporządkowane programy autodestrukcji, takie jak apoptoza, oraz nowsze formy, na przykład ferroptoza. Cuproptoza dokłada nowy rozdział. W tym mechanizmie nadmiar miedzi zalewa elektrociepłownie komórki — mitochondria — i wiąże się ze specyficznymi enzymami metabolicznymi, które normalnie pomagają spalać paliwo. To wiązanie powoduje agregację tych enzymów i destabilizuje drobne centra żelazo–siarkowe niezbędne do funkcjonowania mitochondriów. Efektem jest rodzaj wewnętrznego zatoru i mechanicznej awarii, którego komórka nie potrafi naprawić, kończący się śmiercią przez proteotoksyczność, a nie klasycznymi drogami samobójczymi.
Jak komórki nowotworowe kontrolują miedź i energię
Ponieważ miedź jest równocześnie niezbędna i potencjalnie niebezpieczna, komórki utrzymują rozbudowaną logistykę jej transportu. Dedykowane transportery wprowadzają miedź do komórki, białka opiekuńcze (chaperony) odprowadzają ją do mitochondriów i innych celów, a magazynujące związki, takie jak metalotioneiny i glutation, wychwytują nadmiar. Guzy często przearanżowują ten system. Niektóre nasilały importerów lub chaperonów, by zaspokoić wysokie zapotrzebowanie na energię; inne zwiększają eksportery albo białka magazynujące, by uniknąć przeciążenia miedzią. Równocześnie wiele nowotworów przestawia swój metabolizm — przełączając się między spalaniem cukrów przy powierzchni komórki a głębszym oddychaniem mitochondrialnym. Autorzy przeglądu wskazują, że cuproptoza najsilniej uderza w komórki wciąż w dużym stopniu zależne od mitochondriów, co czyni guzy o takim profilu metabolicznym szczególnie podatnymi.
Główne przełączniki regulujące wrażliwość na miedź
Duże komórkowe „decyzje” wpływają na to, czy cuproptoza może zajść. Supresor guza p53, na przykład, ma skłonność do odciągania komórek od szybkiej fermentacji cukrów w kierunku bardziej uporządkowanego wykorzystania paliwa przez mitochondria. Poprzez to działanie, a także przez modyfikowanie obsługi enzymów wiążących miedź, p53 może zwiększać podatność nowotworów na śmierć wywołaną miedzią — podczas gdy mutacyjne formy p53 często robią odwrotnie. Natomiast czynnik hipoksji HIF‑1α, aktywowany w słabo natlenionych rdzeniach guzów, pomaga komórkom uciec przed cuproptozą, wyciszając kluczowe enzymy mitochondrialne i wzmacniając „osłony” wiążące miedź. Inne szlaki, takie jak Wnt/β‑katenina i AKT, promują odporność przez zwiększanie eksportu miedzi lub chemiczne modyfikowanie istotnych białek, tak że nie reagują już na nadmiar miedzi. Razem te sieci działają jak termostaty, podnosząc lub obniżając wrażliwość guza na terapie oparte na miedzi.
Miedź, układ odpornościowy i inteligentniejsze dostarczanie leków
Rola miedzi nie ogranicza się do bezpośredniego zabijania komórek nowotworowych; kształtuje też środowisko odpornościowe wokół guzów. Kontrolowany stres miedziowy może sprawić, że umierające komórki rakowe stają się bardziej „widoczne”, uwalniając sygnały zagrożenia, które rekrutują i aktywują limfocyty T, komórki dendrytyczne i makrofagi. Miedź wpływa także na poziomy punktów kontrolnych immunologicznych, takich jak PD‑L1, których guzy używają do wyłączania odpowiedzi T, co sugeruje możliwości łączenia leków celujących w miedź z nowoczesnymi immunoterapiami. Ponieważ wolna miedź może uszkadzać zdrowe tkanki, badacze opracowują precyzyjne narzędzia — małocząsteczkowe jonofory, które kierują miedź selektywnie do komórek nowotworowych, oraz platformy nanomedyczne pakujące miedź lub leki napędzane miedzią w docelowe cząstki albo hydrożele. Technologie te mają na celu podnieść poziom miedzi do śmiertelnych stężeń wewnątrz guzów, jednocześnie utrzymując resztę organizmu w bezpiecznym zakresie.
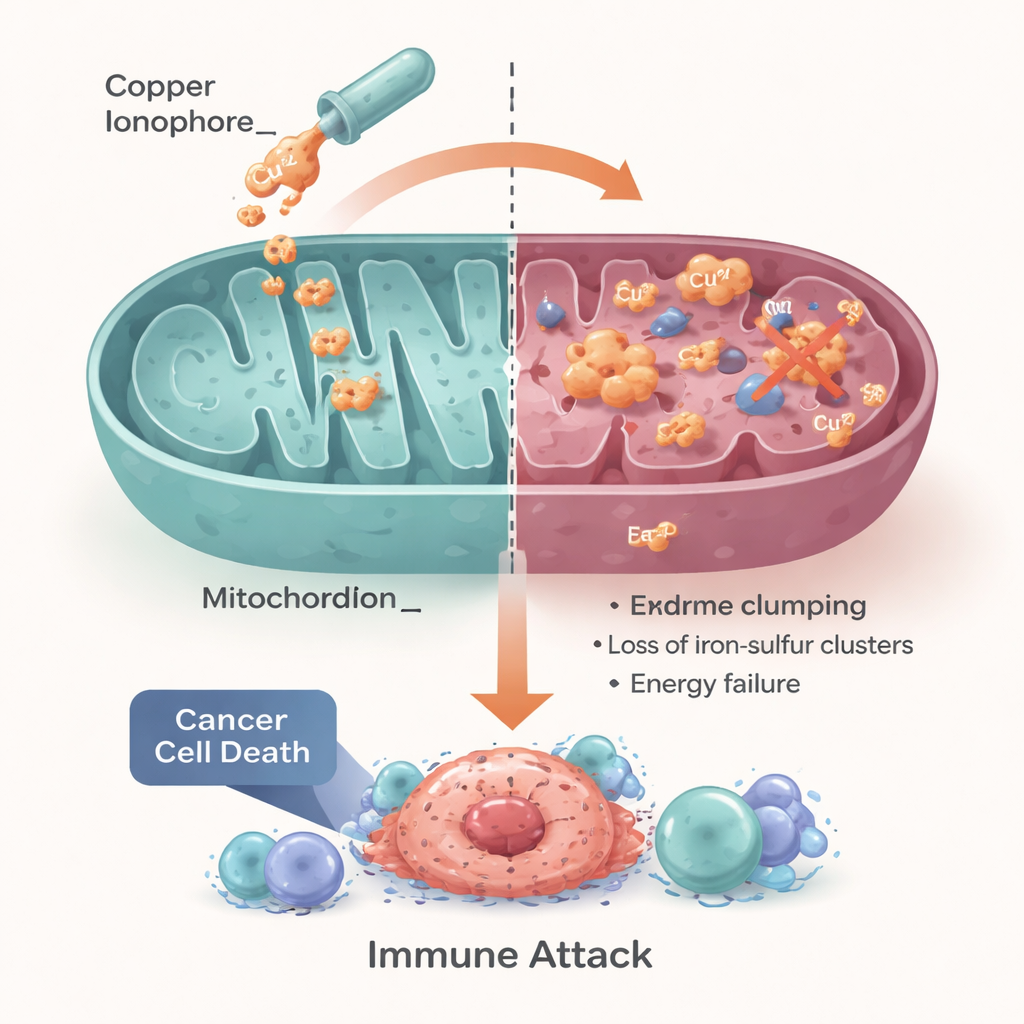
Przekształcenie komórkowej słabości w terapię
Autorzy konkludują, że cuproptoza przemienia podstawową komórkową potrzebę — staranne zarządzanie miedzią i energią — w potencjalne piętę Achillesa nowotworu. Nowotwory z zaburzoną gospodarką miedzi lub nadmiernym poleganiem na metabolizmie mitochondrialnym mogą być szczególnie wrażliwe na strategie oparte na miedzi, w tym na repurposing leków takich jak disulfiram i elesclomol, a także na nanoprodukty kolejnej generacji. Podkreślają jednak, że sukces zależeć będzie od dopasowania odpowiednich pacjentów do odpowiedniego podejścia, przy użyciu biomarkerów raportujących o transporterach miedzi, aktywności mitochondrialnej oraz o statusie immunologicznym i tlenowym guza. Jeśli te przeszkody zostaną pokonane, wykorzystanie cuproptozy mogłoby dać onkologom nowy, napędzany metalem dźwignię do leczenia guzów, które obecnie mają niewiele dobrych opcji.
Cytowanie: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Słowa kluczowe: cuproptoza, metabolizm miedzi, terapia nowotworów, metabolizm guza, immunoterapia przeciwnowotworowa