Clear Sky Science · pl
Powiązane z odcinkiem początkowym aksonu mikrogleje regulują aktywność neuronów i percepcję wzrokową
Immunologiczni pomocnicy kształtują to, co widzimy
Nasza zdolność do widzenia i rozpoznawania obiektów zależy od błyskawicznych sygnałów elektrycznych w mózgu. Przez wiele lat większość zasług przypisywano neuronom, klasycznym „komórkom przewodzącym”. To badanie pokazuje, że drugi typ komórek, przypominający komórki układu odpornościowego — mikrogleje — dyskretnie pomaga dostroić te sygnały w krytycznym punkcie startowym na neuronach. Skupiając się na niewielkim obszarze, gdzie zaczynają się impulsy nerwowe, autorzy wykazują, że specjalna grupa mikroglejów może zwiększać aktywność wybranych neuronów i tym samym wpływać na to, jak dokładnie myszy rozróżniają wzory wzrokowe.
Strażnicy przy „strefie wyzwalania” nerwu
Każdy neuron pobudzający ma krótki odcinek u podstawy, odcinek początkowy aksonu (AIS), gdzie po raz pierwszy generowane są impulsy elektryczne. Badacze odkryli, że około jedna piąta mikroglejów w korze wzrokowej tworzy ciasne, trwałe kontakty z tym konkretnym miejscem, oplatając procesem znaczną część długości AIS. Te mikrogleje związane z AIS mają charakterystyczne kształty i profile aktywności genów w porównaniu z innymi mikroglejami, w tym wyższe poziomy cząsteczek adhezyjnych i sygnalizacyjnych, które pomagają im przyczepiać się do AIS. Jedna z takich cząsteczek, integryna β1, wydaje się szczególnie istotna dla tworzenia tego zwartego połączenia między wypustką mikrogleju a neuronem.
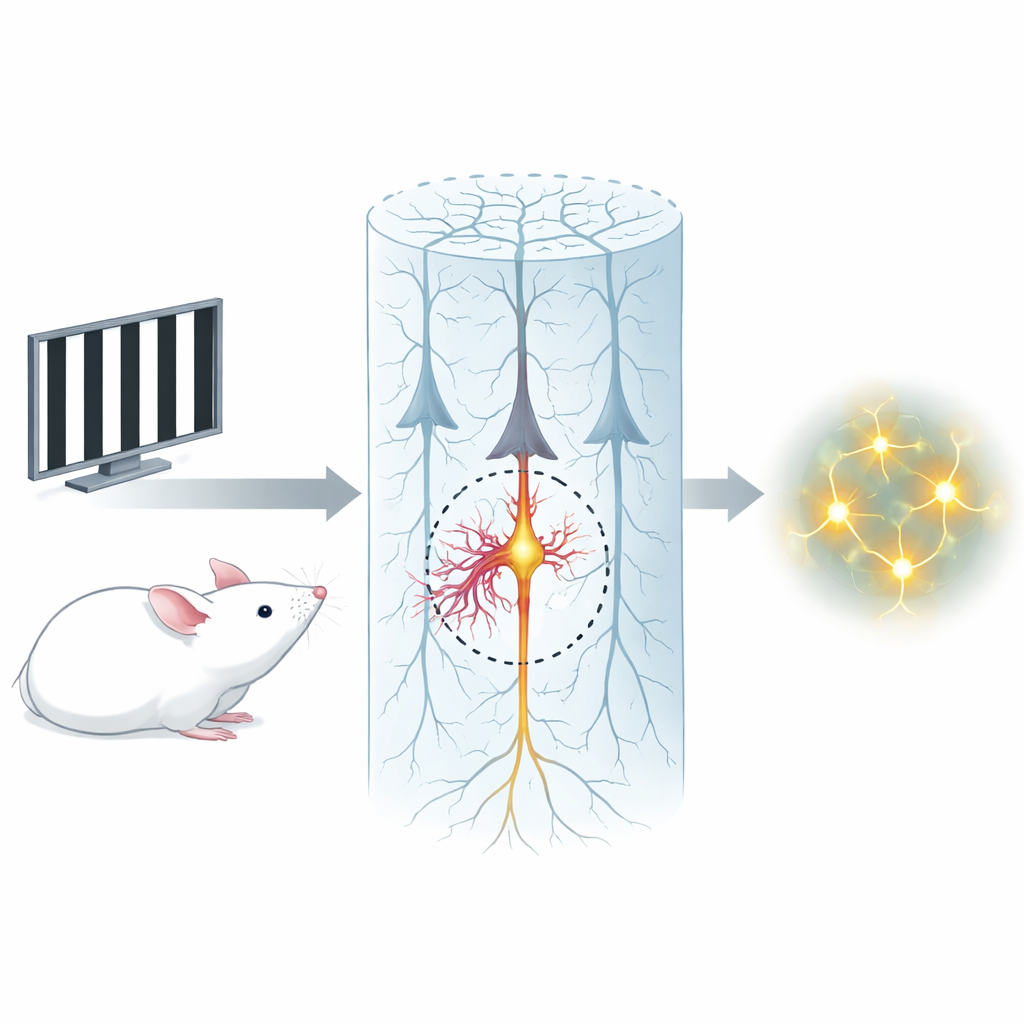
Jak mikrogleje dają neuronowi dodatkowy impuls
Wykorzystując parowane zapisy elektryczne w preparatach tkankowych, zespół sprawdził, czy te „mikrogleje AIS” rzeczywiście zmieniają sposób, w jaki ich partnerskie neurony się wyładowują. Krótkie depolaryzowanie komórki mikroglejowej stykającej się z AIS powodowało, że związany z nią neuron generował więcej potencjałów czynnościowych w odpowiedzi na to samo pobudzenie, mimo że nie występowały między nimi synapsy. Efektu tego nie obserwowano dla mikroglejów dotykających jedynie ciała komórkowego neuronu lub nie stykających się wcale, co wskazuje na kontakt z AIS jako czynnik kluczowy. Badania mechanistyczne wykazały, że gdy te mikrogleje ulegają depolaryzacji, uwalniają jony potasu przez kanał zwany THIK‑1 bezpośrednio do bardzo wąskiej szczeliny przy AIS. Ten niewielki, lokalny wzrost stężenia potasu powoduje subtelną depolaryzację strefy wyzwalania neuronu, obniżając próg wejścia potrzebny do wywołania wyładowania, nie zaburzając przy tym ogólnej równowagi synaptycznej.
Od bodźca wzrokowego do pulsów mikroglejów
Aby sprawdzić, czy takie zmiany napięcia mikroglejów zachodzą naturalnie, badacze użyli szybkich optycznych czujników napięcia, by obserwować mikrogleje u świadomych myszy oglądających przemieszczające się wzory. Stymulacja wzrokowa wywoływała krótkie zdarzenia depolaryzacyjne głównie w wypustkach mikroglejów, a nie w ich ciałach komórkowych. Zdarzenia te zależały od receptorów muskarynowych reagujących na neuroprzekaźnik acetylocholinę oraz od kanału jonowego NALCN, który pozwala na napływ sodu do mikroglejów. Po każdej depolaryzacji mikrogleje używały THIK‑1 do uwolnienia potasu i przywrócenia stanu spoczynkowego. Zablokowanie THIK‑1 uniemożliwiało to przywrócenie, co potwierdza, że wypływ potasu z mikroglejów stanowi wbudowany mechanizm resetujący, naturalnie angażowany podczas przetwarzania sensorycznego.
Wzmacnianie małej, lecz potężnej podgrupy neuronów
Rejestracja zmian wapniowych w korze wzrokowej ujawniła, że tylko mniejszość neuronów reagowała bardzo silnie na poruszające się prążki. Te wysoce responsywne komórki często były tymi, których AIS były kontaktowane przez mikrogleje. Gdy THIK‑1 został zablokowany lub usunięty specyficznie z mikroglejów, lub gdy depolaryzacja mikroglejów była optycznie tłumiona, sygnały wapniowe neuronów związanych z AIS spadały znacząco, podczas gdy pobliskie neurony bez kontaktów z AIS pozostawały w dużej mierze niezmienione. Zakłócenie fizycznego połączenia AIS–mikroglej przez usunięcie integryny β1 w mikroglejach wywołało podobną selektywną utratę silnie reagujących neuronów. We wszystkich przypadkach zmniejszała się ogólna synchronizacja i łączność całych zespołów neuronalnych reagujących na bodźce wzrokowe.
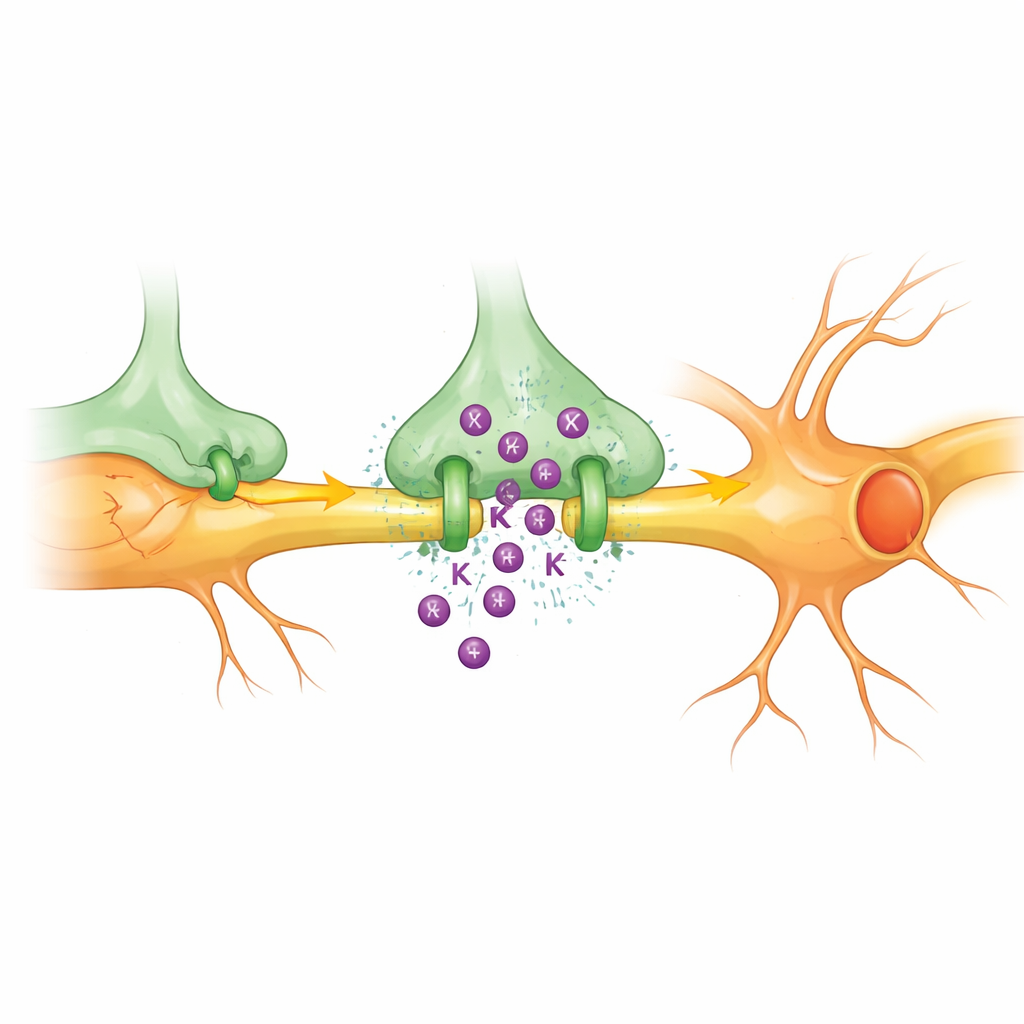
Od kontaktu komórka–komórka do jasnego widzenia
Na koniec autorzy zapytali, czy to mikroskopijne partnerstwo ma znaczenie dla zachowania. Myszy zostały wytrenowane do zadania wzrokowego Go/No‑Go — lizania dla jednej orientacji prążków i powstrzymywania się dla innej. Po treningu ich wydajność spadła gwałtownie, gdy THIK‑1 został zablokowany w korze wzrokowej, gdy THIK‑1 został usunięty z mikroglejów lub gdy zerwano kontakty AIS–mikroglej zależne od integryny β1. Myszy popełniały więcej fałszywych alarmów i gorzej rozróżniały orientacje, mimo że podstawowe obwody pozostawały nienaruszone. Wyniki te sugerują, że niewielka, wyspecjalizowana grupa mikroglejów przy strefie wyzwalania neuronu może selektywnie wzmacniać kluczowe neurony, zacieśniać koordynację zespołową i w ten sposób wyostrzać percepcję wzrokową. W istocie komórki pochodzenia immunologicznego przy AIS działają jak precyzyjne regulatory, wykorzystując krótką falę potasu, by pomóc mózgowi zdecydować, co widzi.
Cytowanie: Wang, Y., Wang, Q., Gao, C. et al. The axon initial segment-associated microglia regulate neuronal activity and visual perception. Cell Res 36, 249–271 (2026). https://doi.org/10.1038/s41422-026-01218-8
Słowa kluczowe: mikrogleje, odcinek początkowy aksonu, pobudliwość neuronalna, <keyword>sygnalizacja potasowa