Clear Sky Science · pl
Dynamiczna siła magneto‑mechaniczna w lizosomach indukuje trwałą repolaryzację makrofagów dla odporności antynowotworowej
Wykorzystanie delikatnych sił do przebudzenia układu odpornościowego
Nowotwory często przetrwają, uśpiewając mechanizmy obronne organizmu. W badaniu tym zbadano zaskakujący sposób przywracania ich aktywności: poprzez fizyczne pociągnięcie za małe komory wewnątrz komórek odpornościowych za pomocą magnetycznie napędzanych nanocząstek. Zamiast polegać wyłącznie na lekach, badacze stosują starannie dostrojone siły mechaniczne wewnątrz komórek, by przeprogramować makrofagi w długotrwałych bojowników przeciw nowotworom.
Dlaczego guzy lite są trudne do leczenia
Nowoczesne immunoterapie przeciwnowotworowe, takie jak przeciwciała blokujące punkty kontrolne czy modyfikowane komórki odpornościowe, zrewolucjonizowały leczenie niektórych nowotworów krwi. W przypadku wielu pacjentów z guzami litymi, np. raka płuca, podejścia te pomagają jednak jedynie nielicznym. Jednym z głównych powodów jest mikrośrodowisko guza. Guzy są otoczone ochronną niszą wypełnioną komórkami i sygnałami tłumiącymi odporność. Makrofagi, które mogą albo atakować guzy (stan przypominający M1), albo je wspierać (stan M2), często zostają „wypchnięte” w tryb sprzyjający nowotworowi — M2. Trwałe odwrócenie tego „złego” zaprogramowania okazało się trudne przy użyciu samych konwencjonalnych leków biochemicznych.
Przekształcanie nanocząstek w maleńkie silniki mechaniczne
Zespół zaprojektował magnetyczne nanomotory — nanoskali cząstki tlenku żelaza domieszkowanego cynkiem, pokryte dodatnio naładowanym polimerem — które są łatwo połykanie przez makrofagi i koncentrują się w lizosomach, komórkowych centrach recyklingu i sygnalizacji. Po wejściu do wnętrza zewnętrzne, obracające się pole magnetyczne powoduje, że cząstki układają się w łańcuchy przypominające pręty i wirują, mieszając gęsty płyn w lizosomach i tworząc maleńkie wirowania. Symulacje komputerowe i eksperymenty na modelowych błonach wykazały, że odpowiednio dostrajając częstotliwość obrotu, można ustawić naprężenie ścinające na błonę lizosomalną w optymalnym zakresie: na tyle silne, by błona stała się krótkotrwale przepuszczalna, ale nie tak silne, by uległa trwałemu zniszczeniu.
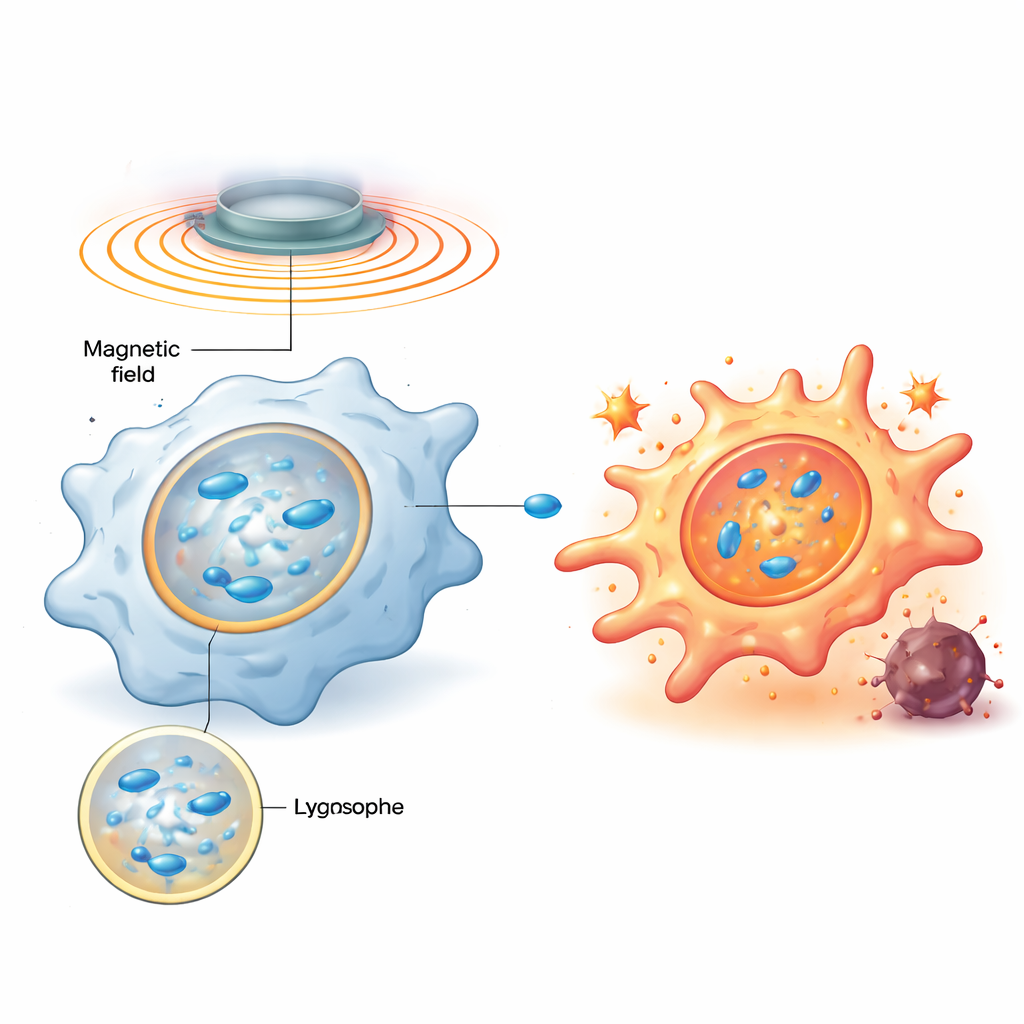
Mechaniczny impuls uruchamia alarm biochemiczny
Gdy błona lizosomu zostaje chwilowo zaburzona, białko wiążące cukry o nazwie galektyna‑9 natychmiast przybywa do uszkodzonych miejsc, pełniąc funkcję czujnika tego stresu mechanicznego. Badanie pokazuje, że to z kolei aktywuje kluczowy enzym czujnik energetyczny AMPK, który następnie wzmacnia szlak sygnałowy NF‑κB — dobrze znany z roli w wywoływaniu odpowiedzi zapalnych i przeciwdrobnoustrojowych. Te sygnały wspólnie przestawiają metabolizm makrofagów z cichego, oszczędnego trybu energetycznego na szybką glikolizę, wzorzec powiązany z wrogo nastawionym, podobnym do M1 zachowaniem. Co ważne, po wyłączeniu pola magnetycznego lizosom naprawia się, a sygnalizacja ustępuje; po ponownym włączeniu pola ta sama droga jest ponownie aktywowana. Programowalne cykle włącz/wyłącz pozwalają badaczom wielokrotnie „stuknąć” ten mechaniczny przełącznik bez zabijania komórek.
Przeedukowanie makrofagów do walki z guzami
W hodowlach komórkowych magnetycznie indukowana przepuszczalność lizosomalna — nazwana MagLMP — przekształciła makrofagi wtłoczone w stan wspierający guz, podobny do M2, z powrotem w prozapalny stan przypominający M1. Tak przeprogramowane komórki produkują więcej cytokin zapalnych i utrzymywały profil podobny do M1 przez dni, nawet w pożywkach pochodzących z guzów, które zwykle skłaniają je ku M2. W modelach mysich z guzami osadzenie magnetycznych nanomotorów w nowotworach i stosowanie codziennych cykli pola obrotowego spowolniło wzrost kilku typów nowotworów. Po eksperymentalnym usunięciu makrofagów korzyść w dużej mierze zanikała, co pokazuje, że te komórki są kluczowe dla działania terapii. Analiza pojedynczych komórek (single‑cell RNA sequencing) tkanki guza wykazała ponadto, że MagLMP zwiększyło odsetek makrofagów o profilu podobnym do M1, zwiększyło liczbę neutrofili przeciwnowotworowych i efektorowych komórek CD8, oraz podniosło ekspresję genów związanych z NF‑κB i glikolizą w makrofagach.
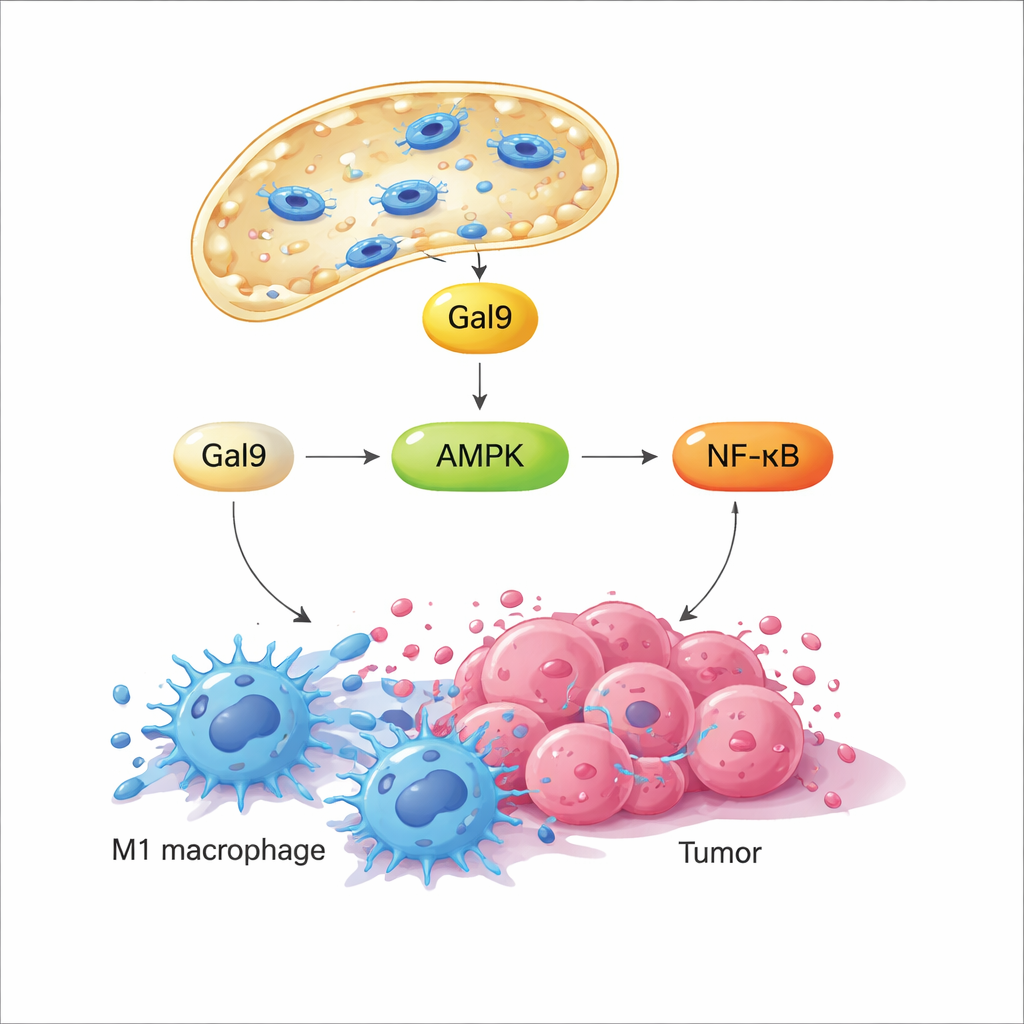
Od kontroli miejscowej do terapii systemowej
Badacze zapytali następnie, czy podejście to może działać bardziej jak terapia realnego świata, podawana przez krwiobieg. Wstrzyknęli nanomotory dożylnie i użyli prostego zewnętrznego magnesu, aby skoncentrować je w guzach, wykazując efektywne pobieranie przez makrofagi w łożu guza. Kolejne leczenie MagLMP ponownie przesunęło makrofagi w stronę stanu podobnego do M1 i zahamowało wzrost guza. W mysich modelach raka płuca wczesnego stadium, rosnącego wewnątrz płuca, połączenie prowadzenia magnetycznego z cyklicznym MagLMP znacząco wydłużyło przeżycie: około jedna trzecia leczonych myszy żyła ponad 300 dni, w porównaniu do zaledwie kilku tygodni u zwierząt kontrolnych. Połączenie MagLMP z inhibitorem punktu kontrolnego PD‑1 dodatkowo wzmocniło kontrolę guza w trudno poddających się terapii modelach.
Nowy sposób kontroli odporności od środka
Praca ta pokazuje, że drobne, dobrze kontrolowane siły mechaniczne wewnątrz konkretnego organellum można wykorzystać do sterowania zachowaniem układu odpornościowego u żywych zwierząt. Poprzez wielokrotne i odwracalne „dźganie” lizosomów, MagLMP aktywuje oś galektyna‑9–AMPK–NF‑κB, która przeprogramowuje makrofagi w trwałych bojowników antynowotworowych bez szeroko zakrojonego uszkadzania komórek. Dla niespecjalistów kluczowa myśl jest taka, że sygnały fizyczne — dostarczane przez magnetycznie napędzane nanomotory — mogą działać jak pokrętło na układ odpornościowy, oferując nową klasę narzędzi uzupełniających leki w przyszłych immunoterapiach nowotworów.
Cytowanie: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Słowa kluczowe: immunoterapia nowotworów, reprogramowanie makrofagów, nanocząstki magnetyczne, mechanotransdukcja, sygnalizacja lizosomalna