Clear Sky Science · pl
Przejściowa mechaniczna aktywacja kanału Piezo1 ułatwia ex vivo ekspansję hematopoetycznych komórek macierzystych
Produkcja większej liczby ratujących życie komórek krwi
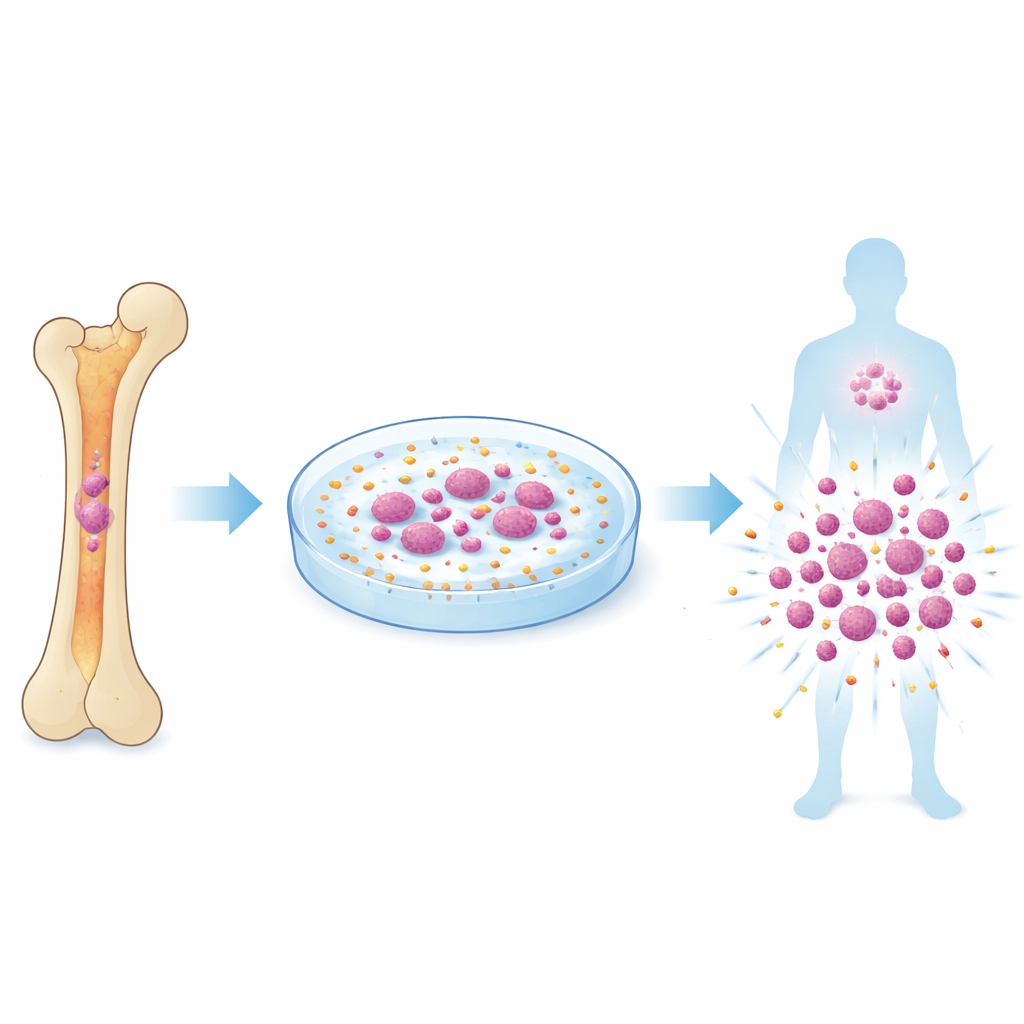
Przeszczepy szpiku kostnego mogą wyleczyć niektóre nowotwory krwi i choroby genetyczne, ale lekarze często są ograniczeni przez niewielką liczbę prawdziwych krwiotwórczych komórek macierzystych dostępnych od dawcy. Badanie to ujawnia zaskakujący sposób hodowli tych rzadkich komórek poza organizmem poprzez delikatne „dotykanie” ich małymi plastikowymi kulkami, które pobudzają mechaniczny czujnik na ich powierzchni. Praca sugeruje nową, potencjalnie bezpieczniejszą drogę do uzyskania wystarczającej liczby komórek macierzystych, tak aby więcej pacjentów mogło skorzystać z przeszczepu.
Dlaczego rozrost komórek krwi jest tak trudny
Komórki macierzyste krwi znajdują się głęboko w naszych kościach i przez całe życie dostarczają wszystkich czerwonych krwinek, białych krwinek i płytek krwi. Przeszczepienie tych komórek może zresetować uszkodzony system krwiotwórczy, jak w leczeniu białaczki, ale tylko wtedy, gdy dostępna jest wystarczająca liczba zdrowych komórek macierzystych i pozostają one w pełni funkcjonalne. Próby ich powiększania w naczyniach laboratoryjnych często zawodzą: komórki zwykle przestają się samoodnawiać lub tracą długoterminową zdolność do odbudowy układu krwionośnego. Większość obecnych metod opiera się na koktajlach czynników wzrostu i modyfikacjach genetycznych, ale nie odtwarzają w pełni złożonego fizycznego środowiska szpiku kostnego, gdzie komórki macierzyste nieustannie odczuwają pchnięcia, pociągnięcia i ciśnienie.
Ukryty mechaniczny przełącznik na komórkach macierzystych
Naukowcy skupili się na białku o nazwie Piezo1, maleńkim kanałopodobnym zaworze w błonie komórkowej, który otwiera się, gdy błona jest zgięta lub rozciągnięta, pozwalając na napływ jonów wapnia i uruchomienie sygnałów wewnątrzkomórkowych. Badając wiele typów komórek krwi, odkryli, że Piezo1 jest szczególnie obfity w prawdziwych hematopoetycznych komórkach macierzystych. Gdy usunięto Piezo1 genetycznie lub zablokowano go lekiem, komórki hodowane w naczyniach nie mogły dobrze się rozszerzać ani odbudowywać krwi u myszy po przeszczepieniu. Co ciekawe, ciągłe stymulowanie Piezo1 chemicznymi aktywatorami również było szkodliwe: komórki gromadziły nadmiar wapnia, wytwarzały szkodliwe reaktywne molekuły i miały mniejszą zdolność do osadzenia się. Wyniki sugerowały, że komórki potrzebują krótkotrwałej, dobrze wyregulowanej mechanicznej aktywacji Piezo1, a nie stałego chemicznego pobudzania.
Wykorzystanie maleńkich kulek do dotknięcia czujnika
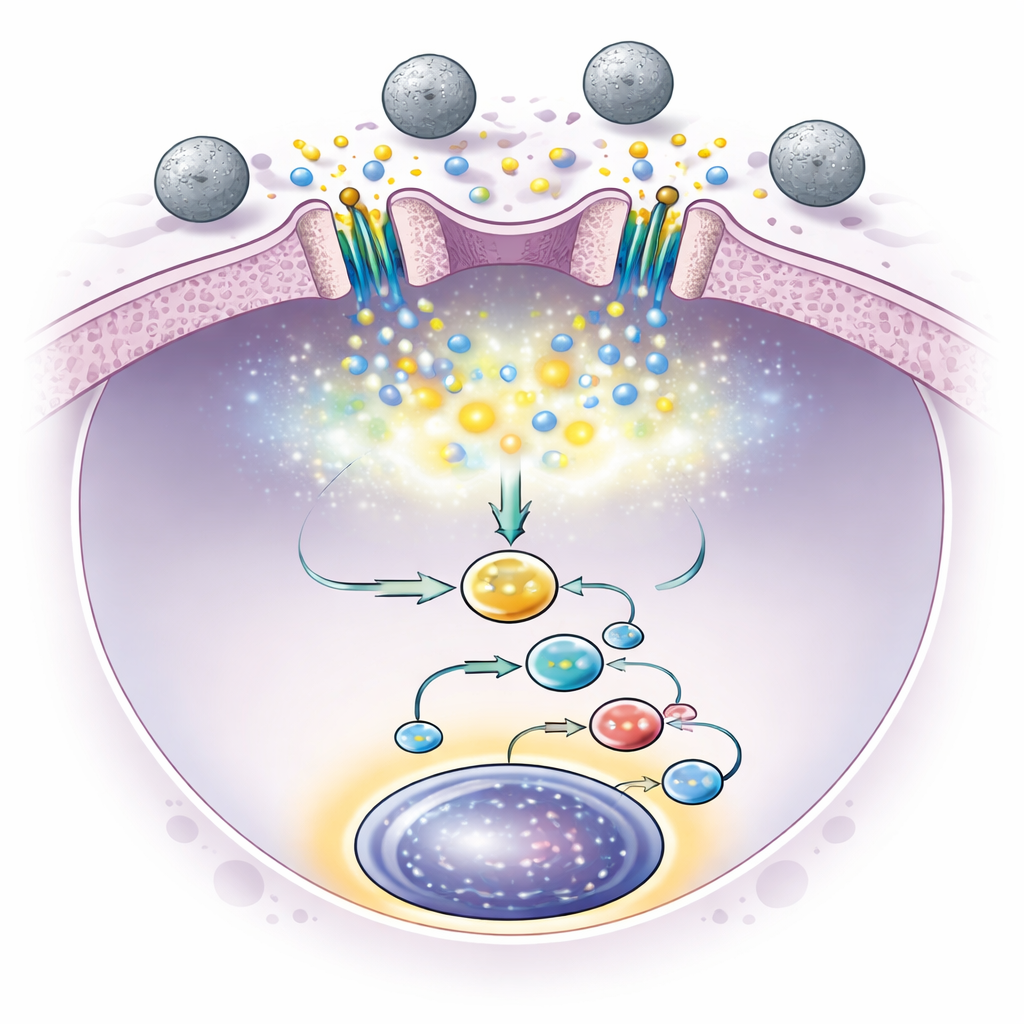
Aby dostarczyć właśnie odpowiednie mechaniczne pchnięcie, zespół sięgnął po mikroskopijne sfery polimerowe, w istocie gładkie plastikowe kulki, które mogły stykać się z komórkami macierzystymi w hodowli. Testowali kulki o różnych rozmiarach i sztywności i odkryli, że 500-nanometrowe sfery polistyrenowe — określane jako PS500 — były wyjątkowo skuteczne. Kiedy mysie komórki szpiku kostnego hodowano razem z tymi kulkami, liczba komórek macierzystych znacznie wzrosła, a komórki te zachowały silną zdolność długoterminowej odbudowy w kolejnych przeszczepieniach między pokoleniami myszy. Dokładne obrazowanie i pomiary mechaniczne wykazały, że kulki wielokrotnie powodowały niewielkie odkształcenia błony komórkowej, z siłami wystarczającymi do otwarcia kanałów Piezo1 w krótkich impulsach, nie przytłaczając komórek.
Od mechanicznego dotyku do sygnałów wzrostu
Krótki epizod otwarcia kanałów Piezo1 wywoływał niewielkie pule wapnia w komórkach macierzystych. To z kolei uruchamiało wewnętrzne szlaki prowadzące do produkcji pewnych białek sygnałowych, w szczególności czynnika wzrostu interleukiny-6. Interleukina-6 następnie działała zwrotnie na komórki macierzyste i aktywowała białko Stat3 w ich jądrach, znane z wspierania przeżycia komórek macierzystych i samoodnawiania. Gdy badacze zablokowali ten szlak Stat3, korzystny efekt kulek zniknął, potwierdzając, że łańcuch zdarzeń — mechaniczny dotyk, puls wapnia, uwolnienie interleukiny-6 i aktywacja Stat3 — był kluczowy dla ekspansji. Co ważne, po tylko krótkim okresie ekspozycji na kulki sygnalizacja pozostała aktywna, a liczba komórek macierzystych nadal rosła, podkreślając, że stała stymulacja nie była konieczna.
Obietnica dla ludzkich przeszczepów
Zespół następnie zastosował tę samą metodę do ludzkich hematopoetycznych komórek macierzystych pobranych z krwi pępowinowej, powszechnego, lecz często ograniczonego źródła do przeszczepów. Dzięki kulkom PS500 te ludzkie komórki rozszerzały się kilka razy bardziej niż przy najlepszych metodach opartych wyłącznie na małych molekułach, zachowując jednocześnie zdolność do trwałej odbudowy krwi u myszy immunodeficyentnych. Badania bezpieczeństwa na myszach sugerowały, że kulki nie wnikają do komórek macierzystych, można je skutecznie usunąć prostą wirowaniem lub filtracją i nie powodują oczywistych uszkodzeń narządów ani nieprawidłowości we krwi przy testowanych dawkach. To stawia system oparty na kulkach jako praktyczną i potencjalnie skalowalną technologię dla banków krwi i centrów transplantacyjnych.
Co to może znaczyć dla pacjentów
W istocie badanie pokazuje, że delikatny bodziec mechaniczny — dostarczony przez dryfujące nanoskali kuleczki — może skłonić komórki krwiotwórcze do podziałów przy zachowaniu ich potencjału, poprzez krótkotrwałą aktywację wbudowanego czujnika ciśnienia zamiast jego przeciążania. Jeśli metoda zostanie przełożona na praktykę kliniczną, może ułatwić uzyskanie wystarczającej liczby wysokiej jakości komórek macierzystych z niewielkiej jednostki krwi pępowinowej lub od częściowego dawcy, poszerzając dostęp do leczniczych przeszczepów dla znacznie większej liczby osób. Podkreśla też, że zwracanie uwagi nie tylko na chemiczne „zupy” otaczające komórki, lecz także na fizyczne doznania, jakie odczuwają, może otworzyć nowe sposoby kontrolowania losów komórek.
Cytowanie: Wang, Q., Zeng, X., Yang, H. et al. Transient mechanical activation of the Piezo1 channel facilitates ex vivo expansion of hematopoietic stem cells. Cell Res 36, 272–285 (2026). https://doi.org/10.1038/s41422-025-01209-1
Słowa kluczowe: hematopoetyczne komórki macierzyste, mechanoczułe kanały jonowe, Piezo1, mikrosfery polistyrenowe, przeszczepienie komórek macierzystych