Clear Sky Science · pl
Bilirubina bezpośrednio aktywuje RIPK3, wywołując nieklasyczny nekroptoza
Kiedy pomocna cząsteczka staje się szkodliwa
Bilirubina jest najbardziej znana jako żółty barwnik stojący za żółtaczką noworodków i powszechnym kolorem siniaków. W niskich stężeniach rzeczywiście pomaga chronić komórki przed uszkodzeniem. Jednak gdy bilirubina gromadzi się w organizmie i przedostaje do mózgu, może powodować trwałe uszkodzenia, szczególnie u noworodków i osób z ciężką chorobą wątroby. Badanie to odkrywa zaskakujący mechanizm, dzięki któremu nadmiar bilirubiny może bezpośrednio uruchomić molekularny „wyłącznik śmierci” w komórkach nerwowych, wywołując destrukcyjny rodzaj śmierci komórkowej i wskazując nowe cele terapeutyczne.
Z barwnika krwi w zagrożenie dla mózgu
Bilirubina powstaje podczas recyclingu czerwonych krwinek. Normalnie wątroba modyfikuje i usuwa ją, utrzymując niskie i stosunkowo bezpieczne stężenia. W pewnych stanach — takich jak żółtaczka noworodków, ciężkie infekcje czy niewydolność wątroby — nieprzetworzona bilirubina może się kumulować. Ponieważ dobrze rozpuszcza się w tłuszczach, ta „wolna” forma może przekraczać barierę krew–mózg, zwłaszcza gdy bariera ta jest osłabiona przez chorobę lub stan zapalny. Po dostaniu się do mózgu bilirubina jest znana jako toksyczna, ale dokładne kroki, poprzez które uszkadza komórki nerwowe, pozostawały niejasne.
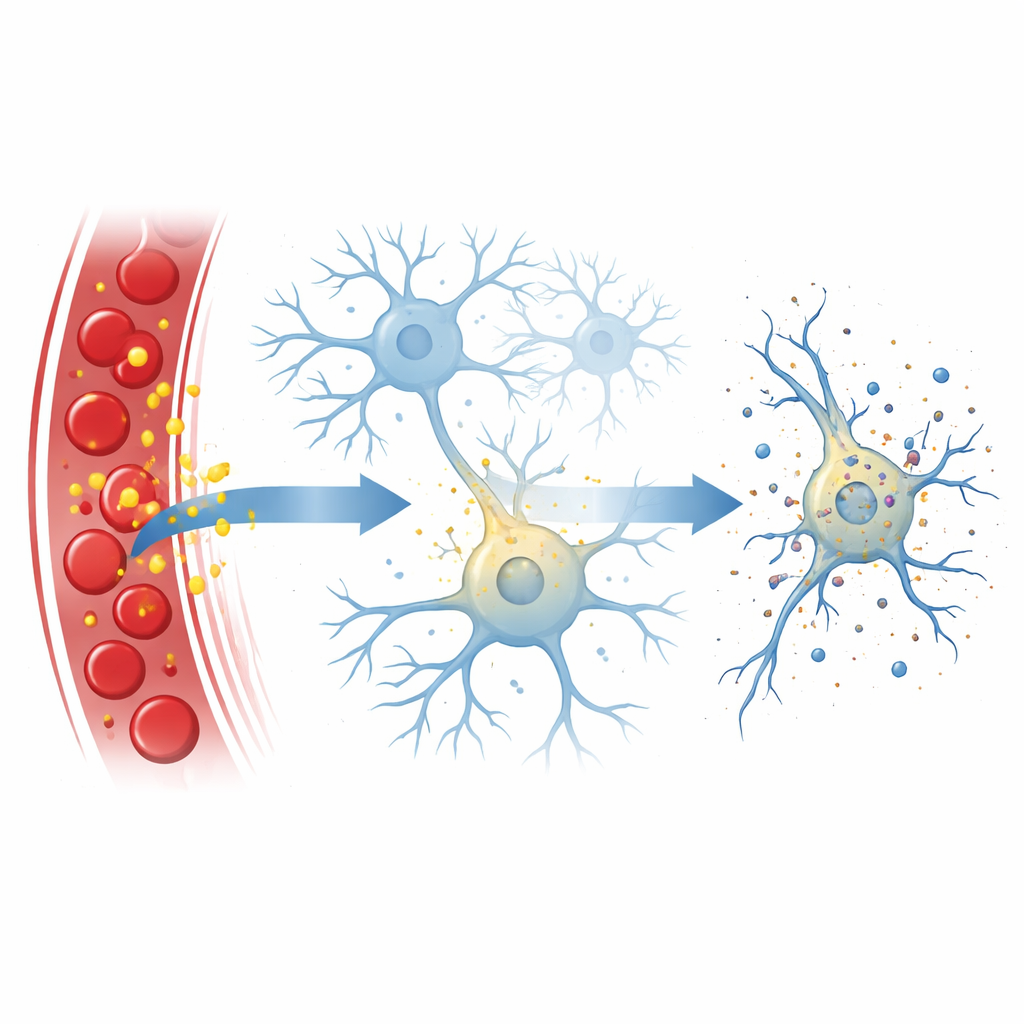
Sterowana eksplozja komórkowa
Naukowcy skupili się na nekroptozie — regulowanej formie śmierci komórkowej przypominającej drobną eksplozję: komórka puchnie, jej błona zewnętrzna pęka, a zawartość wypływa, często wywołując stan zapalny. Proces ten jest zwykle napędzany łańcuchem białek, z RIPK3 jako centralnym węzłem i MLKL, który tworzy dziury w błonie komórkowej. W klasycznych ścieżkach RIPK3 aktywowany jest przez białka partnerskie rozpoznające sygnały zagrożenia, takie jak cząsteczki zapalne czy materiał wirusowy. Zespół odkrył jednak, że bilirubina może ominąć tych zwykłych partnerów i mimo to uruchomić nekroptozę w komórkach nerwowych.
Bilirubina chwyta molekularny wyłącznik śmierci
Na hodowlach neuronów, w plasterkach mózgu i w modelach mysich naukowcy wykazali, że bilirubina selektywnie aktywuje RIPK3 i jego dalszego partnera MLKL w komórkach nerwowych, przy czym typowe białka nadrzędne pozostają w dużej mierze niezmienione. Eksperymenty genetyczne pokazały, że po usunięciu RIPK3 lub MLKL bilirubina nie była w stanie skutecznie zabijać neuronów. Testy biochemiczne poszły dalej: bilirubina fizycznie wiązała się z RIPK3 w dwóch konkretnych miejscach w jego aktywnym rdzeniu, sprzyjała skupianiu się cząsteczek RIPK3 i zwiększała ich aktywność kinazową — funkcję chemiczną uruchamiającą szlak śmierci. To bezpośrednie przyłączenie do RIPK3 nie zależało od typowej powierzchni interakcji białka (domena RHIM) ani od innych białek adaptorowych, wyznaczając nieklasyczną drogę do nekroptozy.
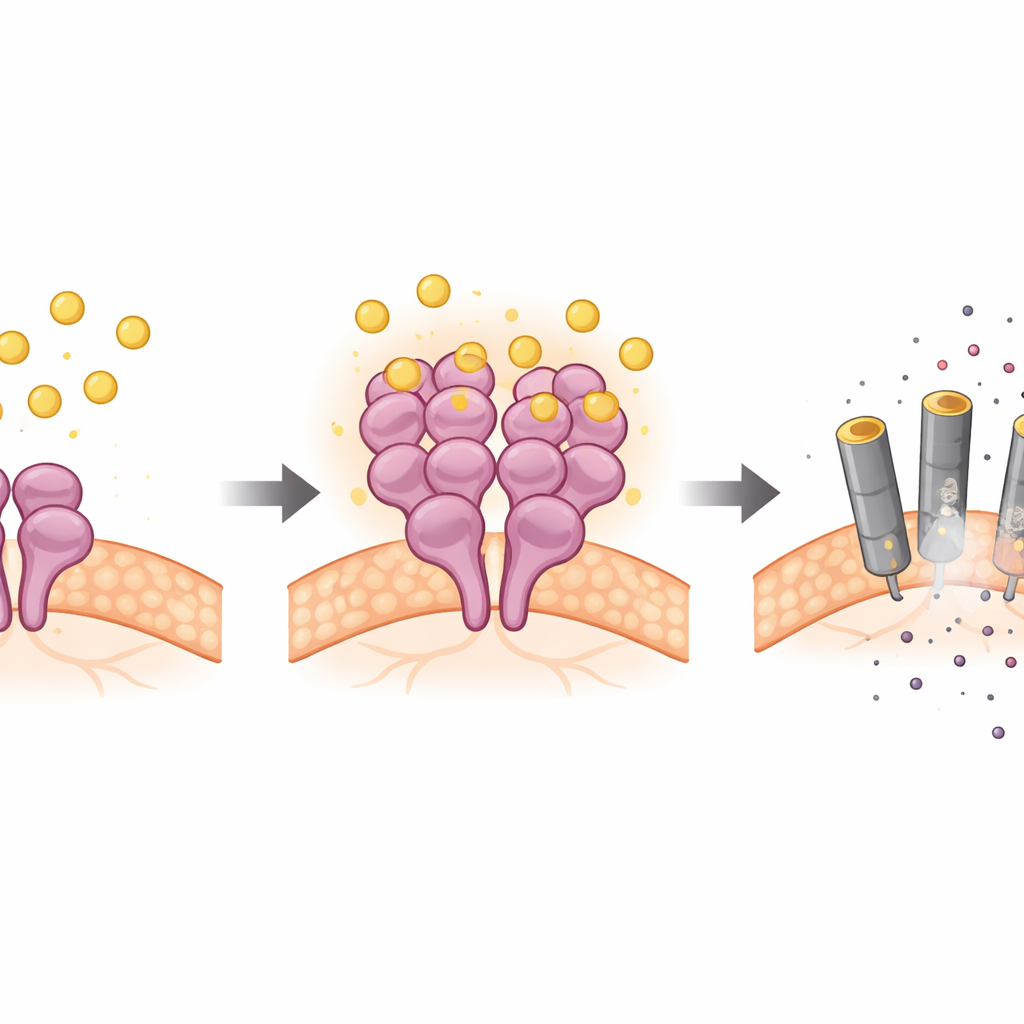
Dowody z żywego mózgu
Aby sprawdzić, czy ten mechanizm ma znaczenie w całym organizmie, zespół podniósł poziom bilirubiny u myszy poprzez wstrzyknięcie jej do mózgu lub wywołanie uszkodzenia wątroby i stanu zapalnego, tak by bilirubina naturalnie przedostała się do mózgu. U normalnych myszy doprowadziło to do silnej aktywacji RIPK3 i MLKL w wrażliwych obszarach mózgu, wzrostu markerów śmierci komórkowej i widocznej utraty zdrowych neuronów. Myszy zmodyfikowane genetycznie tak, by brakowało im RIPK3, były chronione: ich neurony wykazywały znacznie mniejsze uszkodzenia, mniej sygnałów śmierci i osłabione reakcje zapalne, mimo że poziomy bilirubiny były tak samo wysokie. Co ważne, przetworzona, rozpuszczalna w wodzie forma bilirubiny, uważana zwykle za nieszkodliwą, ani nie aktywowała RIPK3, ani nie powodowała podobnego uszkodzenia mózgu, podkreślając, że to niezmodyfikowana, rozpuszczalna w tłuszczach forma jest prawdziwym sprawcą.
Co to oznacza dla pacjentów
Praca ta ujawnia, że nadmiar niezestryfikowanej bilirubiny może bezpośrednio aktywować RIPK3, wywołując sterowany, lecz destrukcyjny rozpad komórek mózgowych poprzez nekroptozę. Zamiast działać jedynie jako ogólny toksyn lub źródło stresu oksydacyjnego, bilirubina zachowuje się jak mała cząsteczka aktywująca specyficzny program śmierci w neuronach i komórkach odpornościowych mózgu. Dla pacjentów z ciężką żółtaczką lub niewydolnością wątroby sugeruje to, że blokowanie RIPK3 lub MLKL — zwłaszcza lekami zdolnymi przeniknąć do mózgu — mogłoby kiedyś pomóc ograniczyć uszkodzenia neurologiczne. W prostych słowach badanie pokazuje, jak zwykle pomocny barwnik może stać się precyzyjnym molekularnym zabójcą i wskazuje nowe sposoby unieszkodliwienia go bez zakłócania jego codziennych ochronnych ról.
Cytowanie: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Słowa kluczowe: neurotoksyczność bilirubiny, nekroptoza, RIPK3, niewydolność wątroby i uszkodzenie mózgu, szlaki śmierci komórkowej