Clear Sky Science · pl
Integracyjny pipeline profilowania przestrzennego do określania architektury mikrośrodowiska guza w archiwalnych próbkach klinicznych przy użyciu technologii CmTSA superplex
Dlaczego ukryty krajobraz wokół guzów ma znaczenie
Nowotwory nie rosną w izolacji. Otacza je tętniąca życiem okolica złożona z komórek układu odpornościowego, komórek wspierających, naczyń krwionośnych i tkanki bliznowatej, które razem tworzą „mikrośrodowisko” guza. W artykule przedstawiono praktyczną metodę szczegółowego mapowania tego ukrytego krajobrazu przy użyciu standardowych szpitalnych próbek tkankowych. Dzięki ujawnieniu, jakie typy komórek sąsiadują ze sobą i jak organizują się w sprzyjające lub szkodliwe sąsiedztwa, metoda może pomóc lekarzom lepiej przewidywać zachowanie nowotworu u pacjenta oraz wybierać najskuteczniejsze terapie.
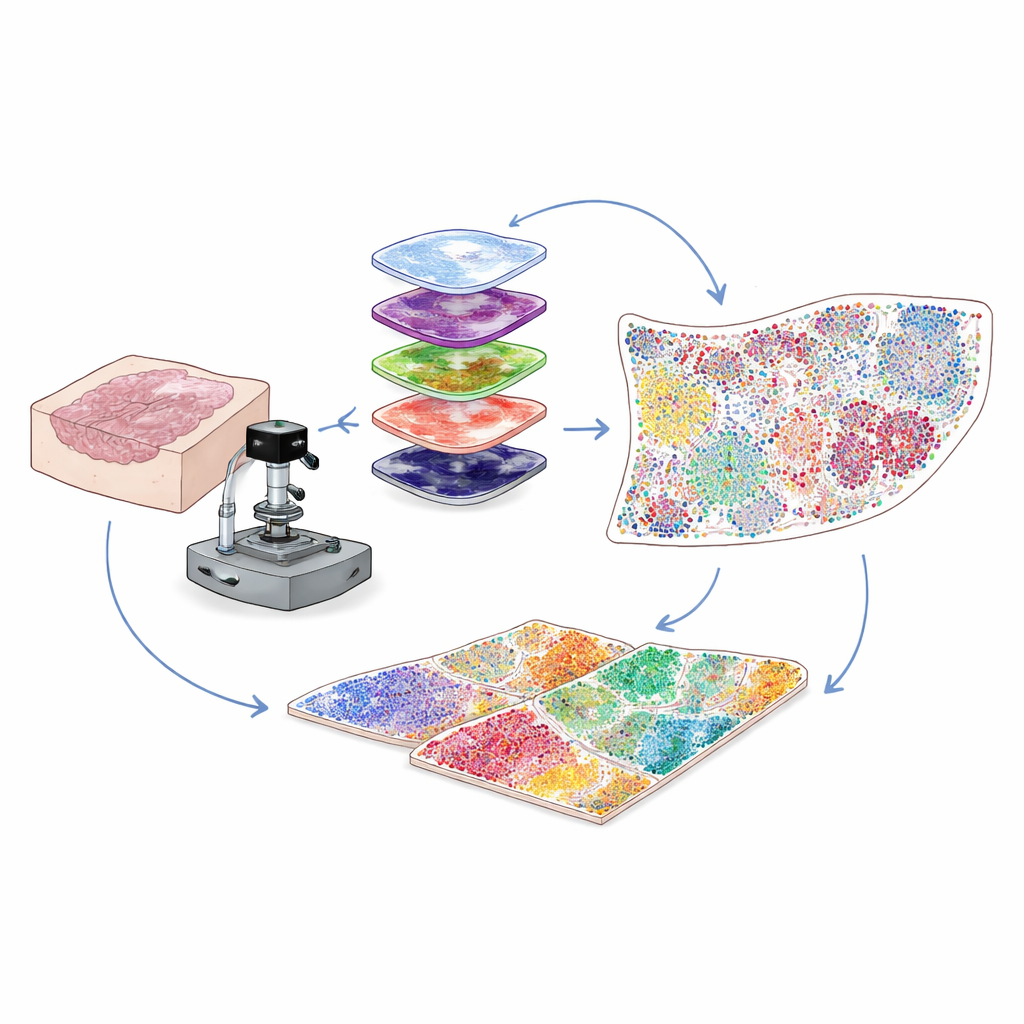
Więcej informacji z codziennych szpitalnych próbek
Większość klinicznych próbek nowotworowych jest utrwalana jako cienkie plasterki tkanki zatopionej w wosku, znane jako bloki FFPE, które mogą być przechowywane przez lata. To kopalnia danych dla badań, ale problem techniczny ograniczał naukowców: takie próbki wykazują naturalną fluorescencję tła, która zagłusza słabe sygnały wielu ważnych białek. Autorzy rozwiązali ten problem, łącząc intensywne, precyzyjnie dostrojone światło z łagodnym leczeniem chemicznym, by selektywnie zetrzeć to tło bez uszkadzania tkanki ani celów białkowych. Ten hybrydowy optyczno-chemiczny etap „wybielania” znacznie poprawia klarowność obrazów, umożliwiając wykrycie słabych sygnałów białkowych, które w przeciwnym razie byłyby utracone.
Oznaczanie dziesiątek znaczników białkowych na tej samej płatce
Aby ustalić, jakie komórki są obecne i co robią, naukowcy barwią tkanki przeciwciałami wiążącymi się z określonymi białkami. Tradycyjne metody multipleksowe albo borykają się z niską siłą sygnału dla rzadkich białek, albo pozwalają jednocześnie śledzić ograniczoną liczbę markerów. W przedstawionej pracy zespół stosuje metodę nazwaną cykliczną amplifikacją sygnału tyramidą (cyclic tyramide signal amplification). W każdej rundzie barwiony jest niewielki zestaw markerów, które są enzymatycznie „rozwijane” w jasne, trwale przytwierdzone plamki fluorescencyjne. Następnie przeciwciała są delikatnie usuwane, podczas gdy sygnał pozostaje, tło jest ponownie wybielane, i dodawany jest następny zestaw markerów. Powtarzając ten cykl wiele razy i wyrównując obrazy przy użyciu stałego sygnału z jąder komórkowych, można wiarygodnie wizualizować 30–60 różnych białek na jednej płytce tkankowej, na całej szkiełku, z rozdzielczością pojedynczej komórki.
Przekształcanie kolorowych obrazów w atlas komórka po komórce
Obrazy o wysokim poziomie multipleksu zawierają miliony pikseli — znacznie więcej, niż człowiek mógłby przeanalizować wzrokowo. Autorzy zbudowali więc pipeline przetwarzania obrazu oparty na wizji komputerowej, który najpierw znajduje i obrysowuje każde jądro komórkowe przy użyciu narzędzi głębokiego uczenia pierwotnie opracowanych do ogólnej segmentacji komórek. Następnie, na podstawie tego, gdzie pojawia się fluorescencja każdego białka — na błonie, w cytoplazmie lub w jądrze — oraz na podstawie zestawów reguł logicznych, każdej komórce przypisywany jest typ lub podtyp, taki jak komórka nowotworowa, pomocnicza komórka T, zabójcza komórka T, komórka B, fibroblast i inne. Wynikiem jest cyfrowa tabela wymieniająca dla każdej komórki na szkiełku jej tożsamość i dokładne współrzędne. To przekształca złożony obraz w ilościową mapę tego, kto i gdzie występuje w mikrośrodowisku guza.
Ujawnianie sąsiedztw komórkowych kształtujących wynik
Komórki rzadko działają w pojedynkę; ważne jest to, jacy mają sąsiadów. Aby to uchwycić, badacze przetestowali różne sposoby definiowania lokalnych sąsiedztw wokół każdej komórki i zdecydowali się na podejście sieciowe oparte na promieniu. Wyobraźmy sobie narysowanie małego kółka — o grubości zbliżonej do ludzkiego włosa — wokół każdej komórki i spisanie, kto w nim mieszka. Grupując komórki, których otaczające kółka mają podobne mieszanki sąsiadów, metoda identyfikuje powtarzające się „funkcjonalne nisze”, takie jak strefy bogate w komórki odpornościowe, bariery bogate w fibroblasty czy obszary zdominowane przez guz. Zastosowanie tej strategii do tkanki jelita grubego pokazuje, że sąsiedztwa oparte na promieniu lepiej odpowiadają znanym strukturom anatomicznym niż alternatywne metody. W próbkach raka szyjki macicy od pacjentów z dobrym i złym rokowaniem zespół stwierdził, że u pacjentów lepiej rokujących nisze bogate w komórki odpornościowe skupiają się przy brzegu guza, podczas gdy u pacjentów z gorszym wynikiem występują grube strefy gęste w fibroblasty, które otaczają komórki nowotworowe i wydają się odgradzać atakujące komórki odpornościowe.
Od map przestrzennych do spersonalizowanego leczenia
Łącząc wysokiej jakości, przystępne barwienie wielu białek z solidną analizą obrazów, praca dostarcza kompleksowy pipeline, który można zastosować do dużej liczby standardowych szpitalnych próbek. Metoda przekształca utrwaloną tkankę w szczegółowe mapy tego, jak komórki nowotworowe, odpornościowe i zrębowe rozmieszczają się i wchodzą w interakcje. Dla czytelników niebędących specjalistami wniosek jest taki, że nie tylko rodzaje komórek, lecz także ich precyzyjne wzorce sąsiedztwa mają znaczenie dla zachowania nowotworu. Ta platforma może pomóc badaczom zlokalizować ochronne centra odpornościowe, zidentyfikować supresyjne bariery komórkowe i w efekcie wspierać dokładniejsze prognozy oraz lepiej dostrojone strategie immunoterapii.
Cytowanie: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Słowa kluczowe: mikrośrodowisko guza, proteomika przestrzenna, obrazowanie multipleksowe, immunologia nowotworów, analiza pojedynczych komórek