Clear Sky Science · pl
Kwas palmitynowy aktywuje c-Myc poprzez dwie szlaki zależne od palmitoilacji, promując raka jelita grubego
Dlaczego tłuszcz w naszej diecie ma znaczenie dla zdrowia jelita
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie, a liczne badania wiążą diety wysokotłuszczowe z większym ryzykiem jego rozwoju. Jak jednak konkretne tłuszcze zawarte w pożywieniu komunikują się z genami sprzyjającymi nowotworom w komórkach jelita, pozostawało niejasne. Artykuł ujawnia bezpośrednie powiązanie między kwasem palmitynowym — głównym tłuszczem obecnym w mięsie, produktach mlecznych i wielu przetworzonych produktach — a silnym genem promującym nowotwory, c-Myc. Praca pokazuje, jak ten powszechny tłuszcz pokarmowy może podsycać stan zapalny, przestawiać metabolizm komórkowy i uzależniać guzy jelita od kwasu palmitynowego.
Od codziennego tłuszczu do przewlekłego zapalenia jelit
Kwas palmitynowy to nasycony tłuszcz obfity w dietach wysokotłuszczowych. Badacze karmili myszy różnymi dietami: normalną paszą, dietami wzbogaconymi w kwas palmitynowy lub klasyczną dietą wysokotłuszczową, a następnie wywoływali zapalenie jelita grubego (colitis). Myszy na dietach bogatych w kwas palmitynowy lub na diecie wysokotłuszczowej rozwijały cięższe zapalenie jelit niż zwierzęta na diecie normalnej. Ich okrężnice były krótsze, bardziej uszkodzone w badaniu mikroskopowym i pełne komórek układu odpornościowego — oznaki nasilonego uszkodzenia zapalnego. Wzorce aktywności genów w tych zapalnych tkankach przypominały te obserwowane w dobrze znanym modelu zapalenia prowadzącego do raka jelita, co sugeruje, że kwas palmitynowy przesuwa środowisko jelitowe w kierunku sprzyjającym nowotworzeniu.
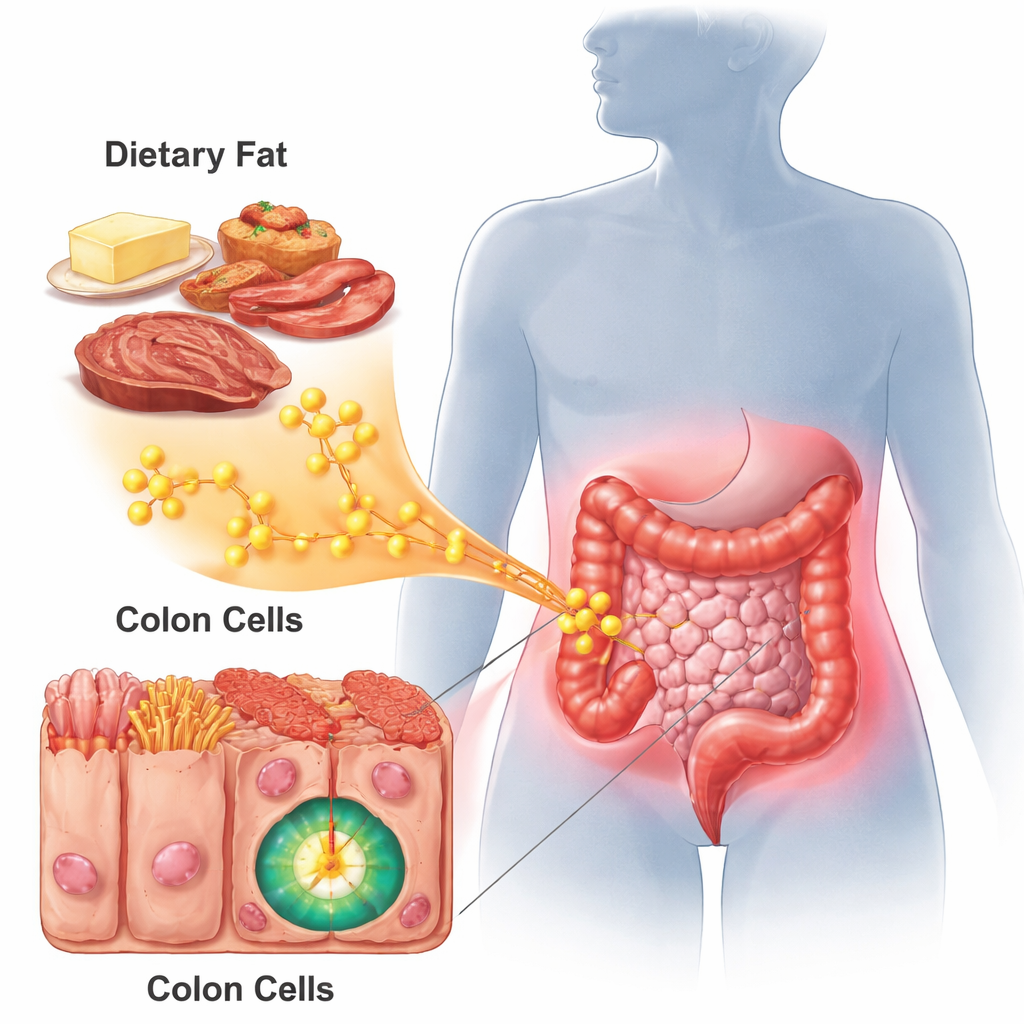
Przełącznik wyczuwający tłuszcz, który wzmacnia gen nowotworowy
Zespół skupił się na c-Myc, głównym genie kontrolnym napędzającym wzrost komórek, przeżycie i cechy przypominające komórki macierzyste w wielu nowotworach. Zarówno w tkankach mysich, jak i w próbkach ludzkiego raka jelita aktywność c-Myc — nie jego ilość — była nieprawidłowo wysoka. Porównując profile genowe myszy karmionych kwasem palmitynowym, we wczesnych guzach jelita i zaawansowanych nowotworach, naukowcy zidentyfikowali jeden kluczowy białkowy pomocnik: ZDHHC9. Ten enzym przyłącza łańcuchy kwasów tłuszczowych do innych białek w procesie zwanym palmitoilacją. Odkryli, że podczas zapalenia poziom IL-1β rośnie i zwiększa ekspresję ZDHHC9, który z kolei bezpośrednio modyfikuje c-Myc w określonym miejscu. Ten tłusty „znacznik” wzmacnia współpracę c-Myc z jego partnerem wiążącym MAX, czyniąc kompleks c-Myc bardziej aktywnym w włączaniu genów wzrostu i cech macierzystości, nawet bez zwiększenia ekspresji samego genu c-Myc.
Jak komórki nowotworowe stają się uzależnione od kwasu palmitynowego
W miarę postępu nowotworu relacja między c-Myc a kwasem palmitynowym zmienia się z jednokierunkowego napędu w samonapędzającą pętlę. Badanie pokazuje, że c-Myc bezpośrednio włącza FATP2, transporter wprowadzający długołańcuchowe kwasy tłuszczowe, takie jak kwas palmitynowy, do komórek raka jelita. Guzy o wyższej aktywności c-Myc miały więcej FATP2 i silniejsze sygnatury metabolizmu kwasów tłuszczowych. W hodowlach komórkowych i w przeszczepach guzów mysich dodatek kwasu palmitynowego przyspieszał wzrost komórek nowotworowych i zwiększał palmitoilację c-Myc, dodatkowo wzmacniając jego aktywność. Powstaje w ten sposób błędne koło: zapalenie i dieta podnoszą poziom kwasu palmitynowego, który aktywuje c-Myc; c-Myc zwiększa następnie FATP2, ściągając jeszcze więcej kwasu palmitynowego i utrzymując „silnik wzrostu” w stanie podwyższonej aktywności.
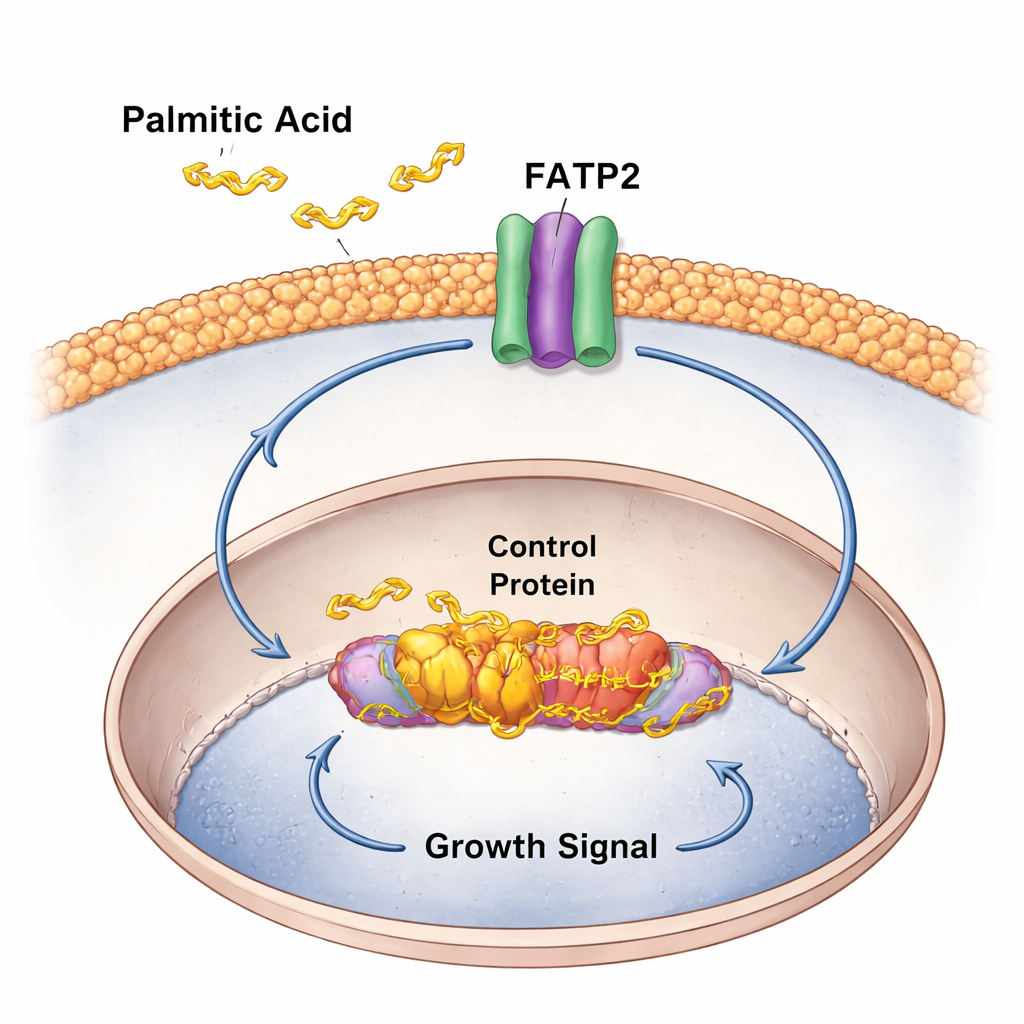
Przekształcenie słabości metabolicznej w możliwość terapeutyczną
Ponieważ guzy jelita w tym modelu stają się zależne od kwasu palmitynowego oraz osi ZDHHC9–FATP2–c-Myc, autorzy sprawdzili, czy przerwanie tego obwodu może spowolnić nowotwór. Użycie narzędzi genetycznych wyłączających ZDHHC9 lub FATP2 w komórkach nowotworowych drastycznie zmniejszyło wzrost guzów u myszy karmionych dietą bogatą w kwas palmitynowy. Połączenie obu wyciszeń było jeszcze bardziej skuteczne. Następnie zastosowali inhibitory o charakterze lekopodobnym: 2BP, który szeroko hamuje enzymy palmitoilujące, oraz Lipofermatę, blokującą FATP2. Każde leczenie zmniejszało rozmiar guza i aktywność genów docelowych c-Myc, a łącznie zmniejszyły guzy o ponad 80 procent, bez oczywistej toksyczności u myszy. To sugeruje, że ukierunkowanie sposobu, w jaki komórki nowotworowe przetwarzają kwas palmitynowy, może pośrednio ujarzmić inaczej „nieuleczalny” gen, taki jak c-Myc.
Co to znaczy dla diety i przyszłych terapii
Mówiąc prosto, badanie ujawnia, że powszechny tłuszcz w diecie może działać jako sygnał, który włącza c-Myc na wyższe obroty — najpierw pogarszając zapalenie jelit, a potem uzależniając dojrzałe guzy od większych ilości kwasu palmitynowego. Kwas palmitynowy przestaje być tylko paliwem; staje się elementem sieci komunikacji między dietą, układem odpornościowym i genami napędzającymi nowotwór. Praca wskazuje dwa główne wnioski: ograniczenie pokarmów bogatych w kwas palmitynowy może pomóc zmniejszyć ryzyko raka jelita, szczególnie u osób z przewlekłym zapaleniem jelit, oraz że nowe terapie blokujące ZDHHC9 lub FATP2 mogłyby wykorzystać uzależnienie guza od tego tłuszczu, aby spowolnić lub zatrzymać chorobę.
Cytowanie: Du, W., Zhang, J., Wang, Y. et al. Palmitic acid activates c-Myc via dual palmitoylation-dependent pathways to promote colon cancer. Cell Discov 12, 12 (2026). https://doi.org/10.1038/s41421-026-00869-6
Słowa kluczowe: rak jelita, dieta wysokotłuszczowa, kwas palmitynowy, c-Myc, uzależnienie metaboliczne