Clear Sky Science · pl
Chronobiologia wirusów neurotropowych: rytmiczne wejście wirusa i arytmiczne zegary gospodarza
Dlaczego czas ma znaczenie w zakażeniach mózgu
Wiele groźnych wirusów, w tym wirus wścieklizny i wirusy opryszczki, ma zdolność infekowania mózgu i nerwów. Badanie stawia pozornie proste, lecz istotne pytanie: czy pora dnia wpływa na to, jak łatwo te „neurotropowe” wirusy dostają się do naszego układu nerwowego, a czy same wirusy mogą z kolei zachwiać naszymi wewnętrznymi zegarami? Zrozumienie tej dwukierunkowej komunikacji między zegarami biologicznymi a wirusami może otworzyć nowe możliwości czasowania szczepień, leków przeciwwirusowych, a nawet organizacji pracy zmianowej w celu zmniejszenia ryzyka.
Dobowe zegary i wirusowe wejścia
Prawie każda komórka w organizmie ma wbudowany system odmierzający 24 godziny, zwykle nazywany zegarem okołodobowym. Steruje nim zestaw podstawowych białek zegarowych, w tym BMAL1 i REV-ERBα, które rytmicznie włączają i wyłączają tysiące genów. Autorzy skupili się na „klamkach” używanych przez wirusy do wnikania do komórek – białkach receptorowych na powierzchni komórek – dla kilkudziesięciu wirusów atakujących mózg lub wnikających do układu nerwowego. Badając organoidy o cechach mózgowych hodowane ze stem cells, linie komórkowe pochodzące od nerwów oraz tkanki myszy, odkryli, że większość tych receptorów wirusowych wykazuje dobowe wahania. Rytmy te ściśle korelowały z aktywnością komponentów zegara, co sugeruje, że nasz system dobowy dyskretnie kontroluje, ile miejsc wejścia dla wirusów jest dostępnych o danej porze.
Czynnik cyklu komórkowego jako posłaniec zegara
Pogłębiając analizę, badacze sprawdzili, jak białko zwykle związane z kontrolą podziału komórek, zwane E2F8, wpisuje się w tę sieć czasową. Odkryli, że E2F8 jest samo pod kontrolą okołodobową i działa jak łącznik między zegarem a przynajmniej jednym kluczowym receptorem wścieklizny, p75NTR. Gdy aktywny jest białkowy element zegara REV-ERBα, tłumi on E2F8. W rezultacie niski poziom E2F8 usuwa hamulec dla genu p75NTR, co pozwala na większą produkcję tego receptora i czyni komórki bardziej podatnymi na wirusa wścieklizny. Co istotne, E2F8 oddziałuje też zwrotnie na zegar: może wiązać się bezpośrednio z regionami kontrolnymi podstawowych genów zegarowych, takich jak REV-ERBα i PER2, tłumiąc ich aktywność. Tworzy to pętlę sprzężenia zwrotnego, w której regulator cyklu komórkowego pomaga kształtować dobowe rytmy i przez to wpływa na podatność komórek nerwowych na zakażenie.
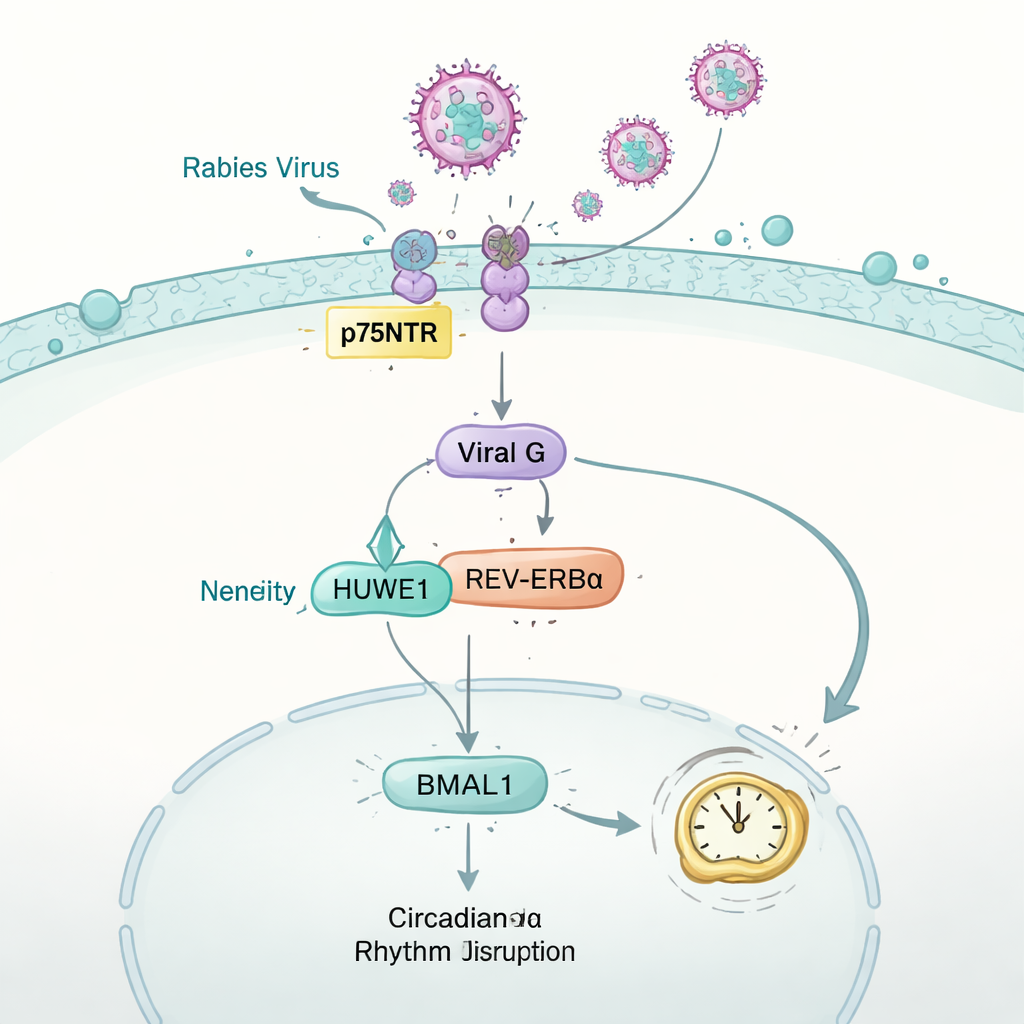
Jak wirus wścieklizny wyprowadza zegar z równowagi
Następnie badanie odwróciło pytanie: czy wirus może oddziaływać na zegar gospodarza? Na myszach zakażonych wirusem wścieklizny zespół monitorował aktywność ruchową, metabolizm i parametry oddechowe. Pomimo normalnego pobierania pokarmu we wczesnym okresie zakażenia, zwierzęta stopniowo traciły regularne wzorce dzień‑noc typowe dla zdrowych myszy. W mózgu i kilku innych narządach poziomy kluczowego białka zegarowego BMAL1 gwałtownie spadły. W komórkach o cechach nerwowych ten efekt dało się przypisać glikoproteinie „G” wirusa wścieklizny, białku powierzchniowemu, które normalnie ułatwia fuzję wirusa z komórką. G przejęła funkcję gospodarczego enzymu nazwanego HUWE1, który zwykle pomaga znakować inne białko zegarowe, REV-ERBα, do degradacji. Konkurując o HUWE1, wirusowe białko G stabilizowało REV-ERBα, co prowadziło do dodatkowego tłumienia BMAL1 i w efekcie zaburzenia mechanizmu zegara utrzymującego fizjologię w 24‑godzinnym rytmie.
Czasowanie, jet lag i ciężkość zakażenia
Aby sprawdzić, czy te molekularne zmiany mają znaczenie dla całego organizmu, zespół zakażał myszy wirusem wścieklizny o różnych porach dnia, przy standardowych warunkach światło‑ciemność, w chronicznych warunkach „jet lagu” oraz u zwierząt genetycznie pozbawionych REV-ERBα. Myszy zakażone na początku fazy aktywnej (nocnej), gdy receptor p75NTR osiąga szczyt, szybciej traciły na wadze, miały większe ładunki wirusa w wielu obszarach mózgu, silniejszy stan zapalny mózgu i umierały szybciej niż myszy zakażone na początku fazy odpoczynku. Myszy narażone na powtarzane przesunięcia fazy, naśladujące pracę zmianową, utraciły normalne rytmy zegarowe w mózgu, wykazywały stale wyższe poziomy p75NTR, słabsze podstawowe sygnały przeciwwirusowe i przechodziły cięższe choroby. Natomiast myszy pozbawione REV-ERBα miały niższe poziomy p75NTR, mniejsze ładunki wirusa i dłużej przeżywały po zakażeniu, co wskazuje, że ten składnik zegara jest istotnym strażnikiem stopnia ciężkości wścieklizny.
Co to oznacza dla ludzi
Mówiąc prosto, badanie pokazuje, że nasze wewnętrzne zegary nie tylko ustalają porę snu; otwierają i zamykają też molekularne drzwi, których używają wirusy atakujące mózg, a te same wirusy potrafią odwdzięczyć się, rozregulowując zegar. Jedno białko, REV-ERBα, stoi w kluczowym punkcie: wraz z E2F8 kształtuje zarówno poziomy receptorów, jak i dobowe ustawienia, podczas gdy wirus wścieklizny manipuluje nim na swoją korzyść. Te spostrzeżenia sugerują praktyczne kierunki działań. Szczepionki czy leki przeciwwirusowe mogą działać lepiej o określonych porach dnia, gdy receptory są niskie lub odpowiedź odpornościowa silniejsza. Ludzie z przewlekle zaburzonymi rytmami — na przykład pracownicy zmianowi czy częstymi podróżnymi — mogą być bardziej narażeni na pewne infekcje neurotropowe. Celowanie w REV-ERBα lub powiązane ścieżki mogłoby pomóc przechylić szalę na stronę gospodarza, łagodząc przebieg choroby i poprawiając wyniki leczenia.
Cytowanie: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Słowa kluczowe: zegar okołodobowy, wirusy neurotropowe, wścieklizna, receptory wirusowe, chronoterapia