Clear Sky Science · pl
Dynamiczne zmiany mikrośrodowiska immunologicznego w raku jajnika po chemioterapii neoadiuwantowej
Dlaczego to badanie ma znaczenie dla kobiet z rakiem jajnika
Zaawansowany rak jajnika często jest leczony silną chemioterapią przed lub po operacji, a mimo to u wielu kobiet choroba nawraca i przestaje odpowiadać na leki. Badanie stawia palące pytanie: w jaki sposób chemioterapia po cichu przekształca własne mechanizmy obronne organizmu wokół guza i czy możemy modyfikować tę reakcję, aby leczenie działało dłużej? Analizując pojedyncze komórki i testując nowe połączenia leków na myszach, badacze ujawniają ukrytą rolę lipidopochodnych hormonów zwanych prostaglandynami w ułatwianiu guzom unikania nadzoru immunologicznego po chemioterapii.
Zmieniające się pole bitwy wokół guza
Guzy jajnika nie rosną w izolacji: znajdują się w zatłoczonym „sąsiedztwie” komórek układu odpornościowego, tkanki łącznej i płynu w jamie brzusznej. Przed leczeniem to środowisko jest już przesunięte na korzyść nowotworu, z niewielką liczbą agresywnych limfocytów T zabójców i wieloma komórkami tłumiącymi atak immunologiczny. Zespół przeanalizował wcześniej opublikowane dane sekwencjonowania RNA pojedynczych komórek od kobiet z wysokozróżnicowanym rakiem surowiczym jajnika, porównując próbki pobrane przed i po chemioterapii neoadiuwantowej (podanej przed operacją). Stwierdzili, że chemioterapia nie tylko zabija komórki nowotworowe; czasowo pobudza też aktywność immunologiczną, zwiększając sygnały związane ze stymulacją komórek T i zapaleniem, jednocześnie redukując niektóre regulatory T, które zwykle tłumią odpowiedź immunologiczną.
Kiedy pomocne zmiany stają się szkodliwe
Pomimo tego krótkotrwałego wzmocnienia większość pacjentek i tak doświadcza nawrotu i rozwija oporność na leki platynowe, takie jak cisplatyna. Aby zrozumieć, dlaczego tak się dzieje, badacze zagłębiali się w to, jak różne typy komórek komunikują się po leczeniu. Odkryli, że chemioterapia silnie zwiększa ekspresję genów zaangażowanych w syntezę prostaglandyn w makrofagach związanych z guzem i fibroblastach oraz wzmacnia komunikację między tymi komórkami a limfocytami T. Zastosowawszy zaawansowane narzędzia matematyczne, wykazali, że ogólne środowisko przesunęło się ku stanowi prozapalnemu, ale ostatecznie supresyjnemu, z rosnącymi poziomami chemoatraktantów przyciągających komórki mieloidalne oraz nasilonymi ścieżkami, które z czasem mogą wyczerpywać limfocyty T. To sugeruje, że prostaglandyny mogą działać jako molekularny włącznik, przekształcający początkowo korzystny napływ odporności w długotrwaczny hamulec przeciwko immunologii przeciwnowotworowej.
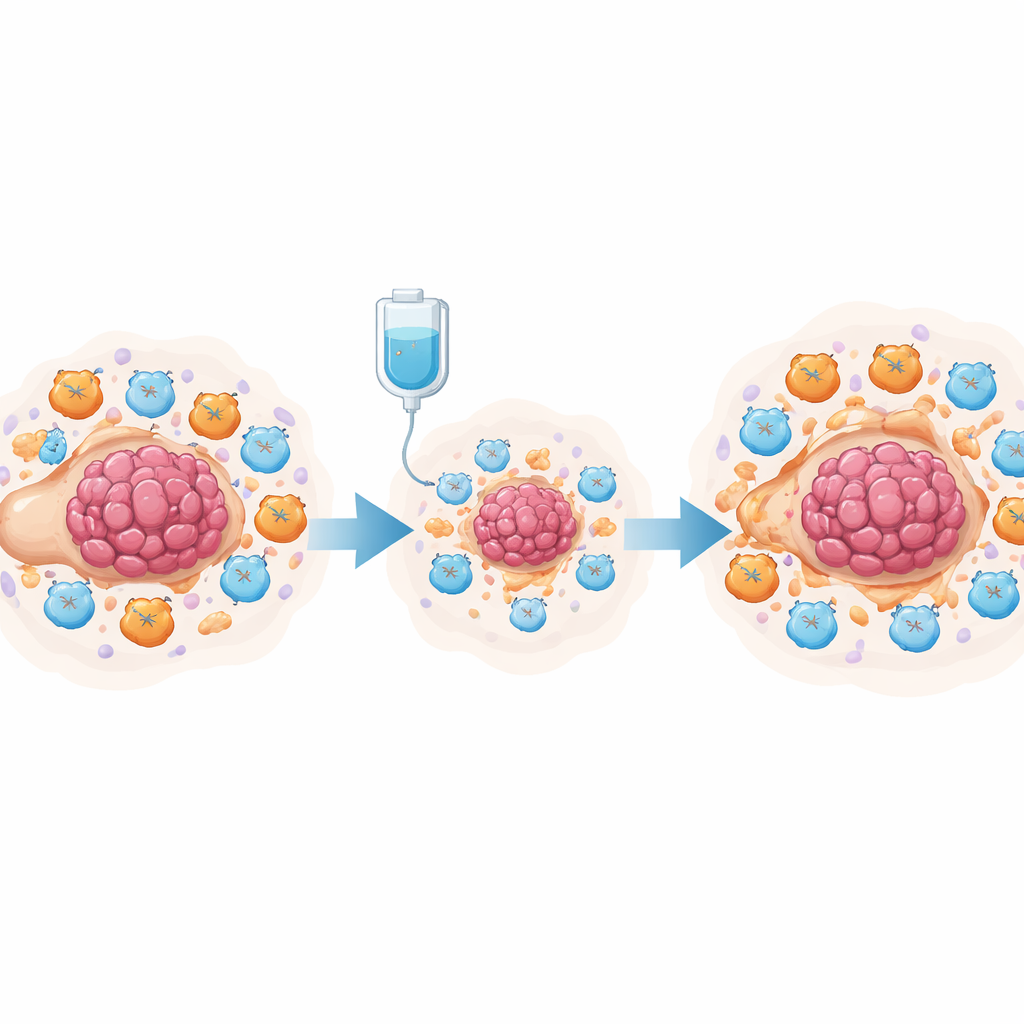
Chemioterapia, prostaglandyny i uśpione limfocyty T
Aby przetestować tę hipotezę eksperymentalnie, zespół użył modelu mysiego raka jajnika leczonego cisplatyną. Analiza pojedynczych komórek dziesiątek tysięcy komórek z jamy brzusznej wykazała, że cisplatyna zmniejszyła liczebność komórek nowotworowych i zwiększyła ogólną liczbę limfocytów T, ale jednocześnie wyraźnie rozszerzyła populacje mieloidalnych komórek supresorowych (MDSC) oraz wyczerpanych limfocytów T zabójców. Zarówno komórki nowotworowe, jak i te komórki supresorowe wykazywały wysoką ekspresję enzymów produkujących prostaglandyny. W hodowlach współkulturowych komórki nowotworowe traktowane cisplatyną nakłaniały komórki szpiku kostnego do przyjęcia fenotypu podobnego do MDSC i osłabiały aktywność oraz proliferację limfocytów CD8+ zabójców. Badacze powiązali ten efekt ze szlakiem sygnałowym NF-κB w komórkach nowotworowych, który uruchamiał gen PTGES — kluczowy etap w produkcji prostaglandyny E2. Zablokowanie tego szlaku obniżało poziomy PTGES i produkcję prostaglandyn.
Odwrócenie trendu dzięki terapii skojarzonej
Najważniejsze praktyczne pytanie brzmiało, czy blokowanie prostaglandyn może poprawić skuteczność chemioterapii. U myszy naukowcy wykorzystali genetyczne usunięcie Ptges w komórkach nowotworowych, przeciwciała neutralizujące prostaglandynę E2 oraz małocząsteczkowe inhibitory syntazy prostaglandyny E. Wszystkie te podejścia obniżały poziomy prostaglandyn, zmniejszały gromadzenie się MDSC i przywracały zdolność zabijania oraz odporność „podatnych na odnowę” limfocytów CD8+. W połączeniu z cisplatyną lub standardowym schematem cisplatyna‑paklitaksel inhibitory prostaglandyn hamowały wzrost i rozsiew guza skuteczniej niż sama chemioterapia. Dane wskazują, że immunosupresja napędzana przez prostaglandyny nie jest błahym zjawiskiem, lecz kluczową przyczyną ucieczki guza po początkowej odpowiedzi.
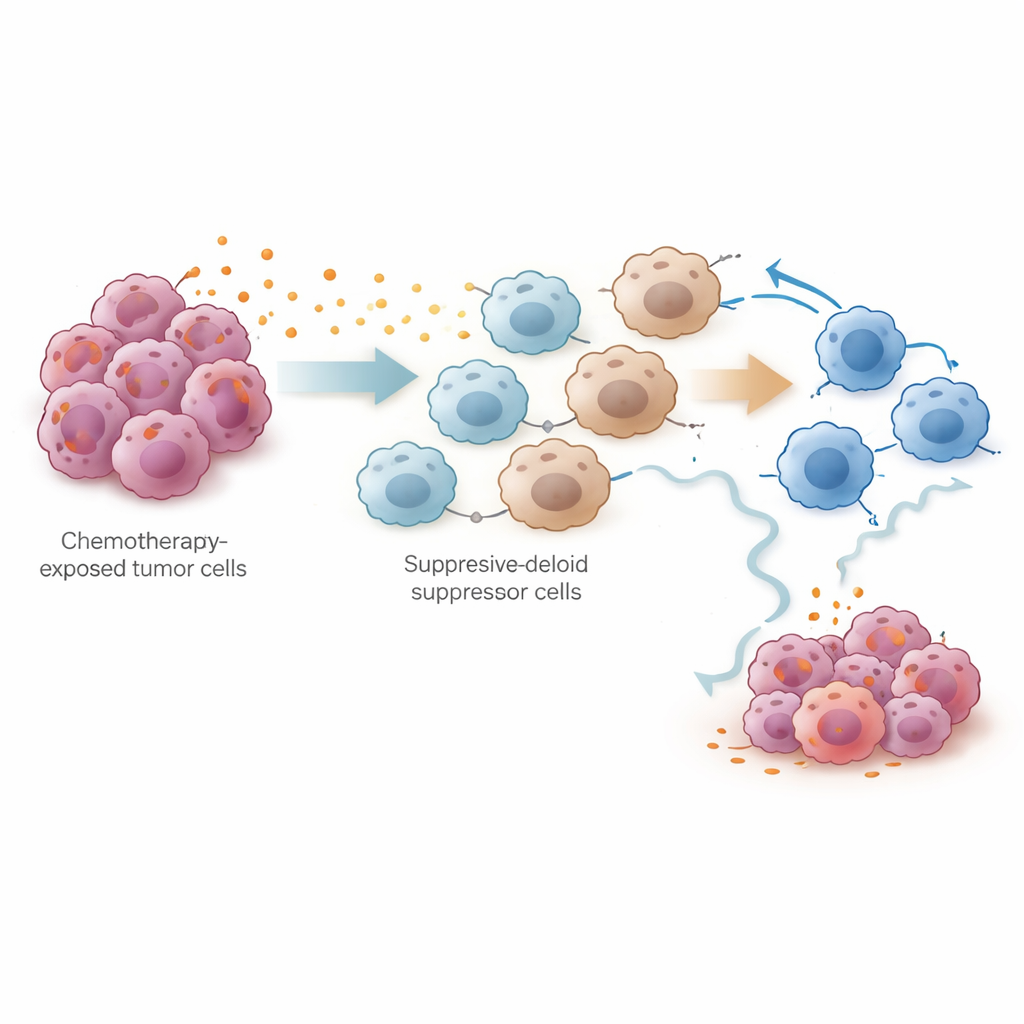
Nowe spojrzenie na utrzymanie skuteczności leczenia
Mówiąc prostymi słowami, praca ta sugeruje, że chemioterapia zmienia otoczenie guza w dwóch fazach: najpierw osłabia nowotwór i krótko mobilizuje układ odpornościowy, ale potem wywołuje falę prostaglandyn, które przyciągają komórki supresyjne i wyczerpują naturalne siły zabijające guz. Identyfikując produkcję prostaglandyn napędzaną przez PTGES jako kluczowego sprawcę, badanie wskazuje namacalną strategię: łączenie standardowej chemioterapii platynowej z lekami blokującymi szlaki prostaglandynowe może pomóc utrzymać silny atak immunologiczny i opóźnić lub zapobiec nawrotowi raka jajnika. Chociaż konieczne są badania kliniczne, podejście skojarzone oferuje obiecujący kierunek przedłużania korzyści z istniejących terapii.
Cytowanie: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Słowa kluczowe: rak jajnika, mikrośrodowisko guza, oporność na chemioterapię, prostaglandyny, immunoterapia