Clear Sky Science · pl
Wykorzystanie pyroptozy w terapii raka piersi: mechanizmy immunologiczne i nowe strategie biomateriałowe
Przekształcanie śmierci komórki w nową broń przeciw rakowi piersi
Rak piersi pozostaje jednym z najczęstszych i najbardziej opornych nowotworów na świecie. Wiele guzów ostatecznie unika działania zabiegów chirurgicznych, chemioterapii, a nawet nowoczesnych immunoterapii. Niniejszy przegląd bada pojawiający się pomysł: celowe wywoływanie „ognistej” formy śmierci komórki, zwanej pyroptozą, wewnątrz guzów piersi. Wywołując kontrolowane pęknięcie komórek nowotworowych w sposób zapalny, naukowcy mają nadzieję zarówno bezpośrednio zabić guz, jak i pobudzić układ odpornościowy do dołączenia do ataku.
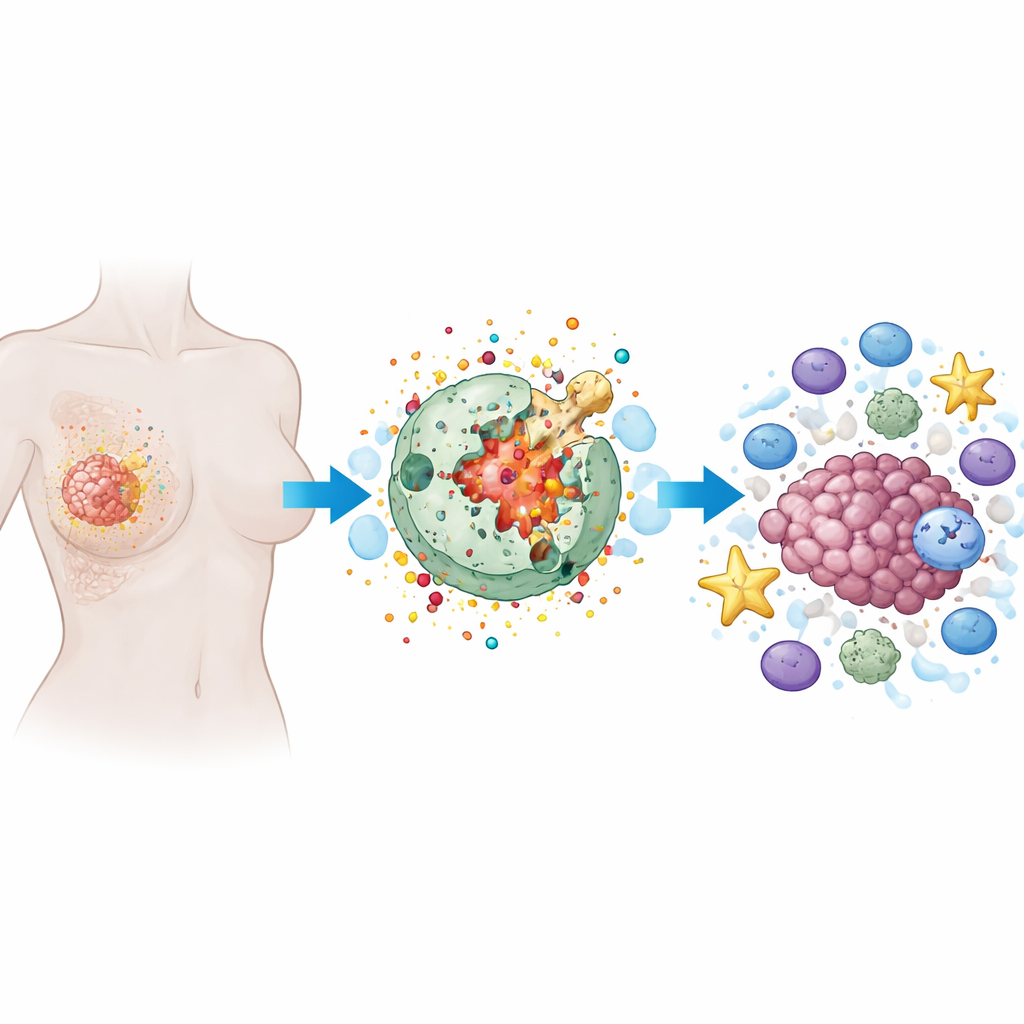
Jak działa „ognista” forma śmierci komórki
Pyroptoza to zaprogramowana forma śmierci komórki, w której komórka pęcznieje, jej błona zewnętrzna zostaje pełna porów, a w końcu pęka, uwalniając zawartość. W przeciwieństwie do cichej, uporządkowanej śmierci komórki obserwowanej przy wielu terapiach, pyroptoza jest głośna i zapalna. Specjalistyczne białka, zwłaszcza rodzina nazywana gasderminami, działają jak małe ładunki wyburzeniowe. Po przecięciu przez wewnętrzne enzymy gasderminy drążą otwory w błonie komórkowej. To nie tylko niszczy komórkę nowotworową, ale także uwalnia sygnały alarmowe i cząsteczki zapalne, które mogą przyciągać i aktywować komórki odpornościowe.
Dlaczego guzy piersi stanowią szczególne wyzwanie
Rak piersi nie jest jedną chorobą, lecz zbiorem podtypów o różnych zachowaniach. Niektóre, takie jak rak potrójnie ujemny, nie mają powszechnych celów terapeutycznych i często wykazują oporność na leczenie. Wiele guzów piersi uważa się za „immunologicznie zimne”, co oznacza, że zawierają niewiele aktywnych komórek odpornościowych wewnątrz. Przegląd wyjaśnia, jak cechy mikrośrodowiska guza piersi — w tym komórki zrębu, komórki immunosupresyjne oraz lokalne niedobory tlenu — mogą zarówno sprzyjać wywołaniu pyroptozy, jak i, jeśli są źle kontrolowane, zamieniać jej zapalenie w paliwo dla wzrostu i rozsiewu guza. Ta dwubiegunowość sprawia, że precyzja jest szczególnie istotna.
Wewnętrzne „przełączniki” gasdermin w komórkach nowotworowych
Centralnym motywem artykułu jest to, jak różne białka gasdermin działają jako molekularne przełączniki wewnątrz komórek raka piersi. Formy takie jak GSDMD i GSDME mogą przekształcać sygnały z chemioterapii, radioterapii lub atakujących komórek odpornościowych w pełnoobjawową pyroptozę. Inne, jak GSDMC i niektóre formy GSDMB, występują częściej w agresywnych guzach i mogą zarówno promować, jak i hamować chorobę w zależności od sposobu ich aktywacji. Wiele raków piersi chemicznie wycisza GSDME, tłumiąc pyroptozę i aktywację immunologiczną. Przywrócenie lub selektywne uruchomienie właściwych gasdermin może zadecydować o tym, czy terapia zabiła tylko kilka komórek, czy zamieniła cały guz w miejsce „w miejscu” szczepionki, które alarmuje układ odpornościowy.
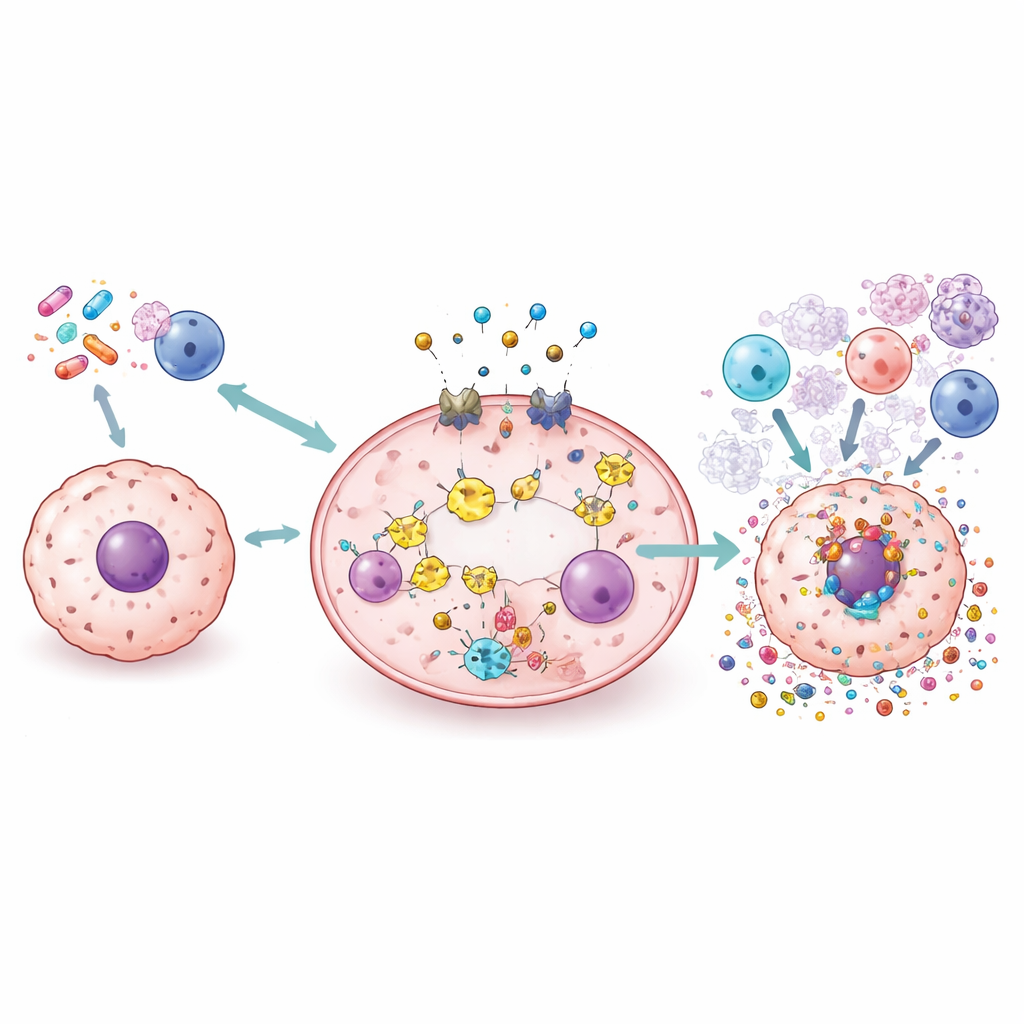
Nowe narzędzia: leki, nanocząstki, wirusy i radioterapia
Przegląd przedstawia szeroki wachlarz strategii badanych pod kątem bezpiecznego wykorzystania pyroptozy. Standardowe leki, takie jak cisplatyna i doksorubicyna, można przekierować lub przeformułować, aby skłaniały komórki nowotworowe do pękania napędzanego przez gasderminy zamiast cichej śmierci. Małe cząsteczki mogą wzmacniać lub blokować części szlaku, by precyzyjnie regulować zapalenie. Nanocząstki i biomimetyczne nośniki są projektowane do dostarczania chemioterapii, jonów miedzi lub cząsteczek aktywowanych światłem bezpośrednio do guzów, gdzie wywołują pyroptozę, oszczędzając tkanki zdrowe. Wirusy onkolityczne i radioterapia mogą być także zaprojektowane lub łączone z innymi środkami, by wywoływać pyroptozę i przekształcać immunologiczny krajobraz guza, potencjalnie zwiększając skuteczność leków hamujących punkty kontrolne odporności.
Równoważenie silnych korzyści z realnym ryzykiem
Ze względu na silny charakter zapalny pyroptozy te same reakcje, które pomagają układowi odpornościowemu zwalczać raka, mogą także uszkadzać normalne tkanki, a nawet sprzyjać wzrostowi guza, jeśli staną się przewlekłe. Autorzy podkreślają wczesne biomarkery — takie jak sygnatury genowe, wzorce metylacji, fragmenty białek gasdermin we krwi i profile cytokin — które mogą pomóc zidentyfikować pacjentów najbardziej prawdopodobnych do skorzystania i tych, u których istnieje wyższe ryzyko niebezpiecznych „burz cytokinowych”. Zaawansowane projekty nanomedyczne, starannie dobrane kombinacje leków oraz monitorowanie w czasie rzeczywistym markerów zapalnych są badane, aby utrzymać odpowiedź o ostrym, lecz kontrolowanym przebiegu.
Co to może oznaczać dla przyszłych pacjentów
Mówiąc wprost, przegląd argumentuje, że sprawienie, by komórki nowotworowe „umierały głośno”, może zmienić opiekę nad rakiem piersi. Poprzez precyzyjne wywołanie pyroptozy w wybranej podsieci komórek guza lekarze mogą zarówno zmniejszyć masę guza, jak i obudzić silną, długotrwałą odpowiedź immunologiczną, przemieniając guzy zimne w gorące i bardziej wrażliwe na nowoczesne immunoterapie. Jednak pyroptoza jest zmiennym sojusznikiem: jeśli zostanie uwolniona zbyt szeroko lub zbyt długo, może pogorszyć stan zapalny lub sprzyjać rozwojowi opornych komórek. Przyszłe badania skupią się na mapowaniu, kto skorzysta, doskonaleniu systemów celowanego dostarczania oraz prowadzeniu badań klinicznych łączących podejścia wywołujące pyroptozę z lekami immunologicznymi. Jeśli te wyzwania zostaną rozwiązane, wykorzystanie pyroptozy może dodać silny nowy wymiar do leczenia raka piersi.
Cytowanie: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Słowa kluczowe: pyroptoza, rak piersi, gasdermina, mikrośrodowisko guza, nanomedycyna