Clear Sky Science · pl
Absolutna dynamika i względna statyka: związek między glikolizą a OXPHOS w rozwoju nowotworu
Dlaczego wybory energetyczne raka mają znaczenie
Komórki nowotworowe przypominają ekstremalnych wytrzymałościowców: muszą nieustannie się zasilać, by rosnąć, szerzyć się i unikać terapii. Ten przegląd wyjaśnia, jak komórki guzowe korzystają z dwóch głównych systemów energetycznych — jednego szybkiego i jednego wydajnego — oraz, co ważniejsze, jak je mieszają i przełączają między nimi. Zrozumienie tych zmieniających się strategii energetycznych daje nowe spojrzenie na diagnozowanie i leczenie raka w całym przebiegu choroby.
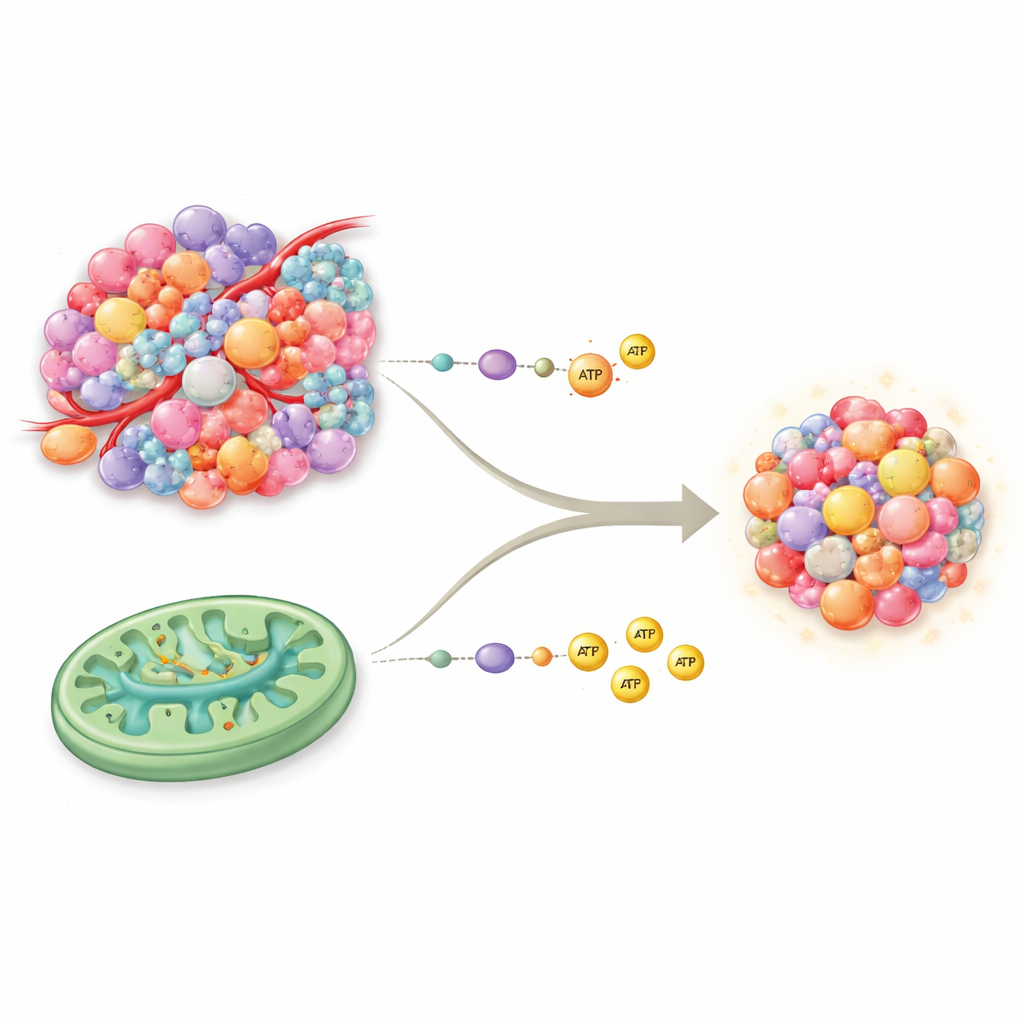
Dwie główne drogi produkcji paliwa przez komórki
Nasze komórki zwykle pozyskują energię dwiema podstawowymi drogami. Glikoliza to szybki, „gotówkowy” system, który szybko rozkłada cukry, ale daje stosunkowo mało energii na jednostkę. Fosforylacja oksydacyjna, czyli OXPHOS, zachodzi w mitochondriach i działa jak wysoko wydajna elektrownia — produkuje znacznie więcej energii, ale wymaga dobrej dostępności tlenu i substancji odżywczych. Przez dekady uważano, że rak polega niemal wyłącznie na glikolizie, nawet przy obecności tlenu — to wzorzec znany jako efekt Warburga. Nowe dowody obalają ten prosty pogląd: wiele guzów ma w pełni funkcjonalne mitochondria i potrafi wykorzystywać OXPHOS oraz cykl kwasu trójkarboksylowego (TCA) obok glikolizy, co zapewnia im bogatszy i bardziej elastyczny zestaw energetyczny niż wcześniej sądzono.
Wiele typów komórek, wiele wyborów paliwowych
Guz nie jest jednorodną masą. To mały ekosystem zawierający komórki nowotworowe, komórki wspomagające, naczynia krwionośne i komórki układu odpornościowego, z których każda ma odrębne potrzeby energetyczne. Niektóre komórki nowotworowe żyją blisko naczyń krwionośnych i mają dużo tlenu oraz składników odżywczych; inne są zanurzone głęboko w obszarach z ubogim zaopatrzeniem. W rezultacie komórki w tym samym guzie mogą preferować glikolizę, opierać się głównie na OXPHOS lub używać obu dróg jednocześnie. Ta metaboliczna różnorodność — zwana heterogennością — wynika z różnic w przepływie krwi, poziomach składników odżywczych, typie komórek i sygnałach ze środowiska otaczającego. Na to nakłada się często symbioza metaboliczna: komórki glikolityczne eksportują laktozat jako produkt „odpadkowy”, który sąsiednie komórki zależne od OXPHOS importują i spalają jako wartościowe paliwo. Podobne współdzielenie laktozatu zachodzi między komórkami nowotworowymi a komórkami wspomagającymi, takimi jak fibroblasty, komórki naczyniowe i komórki tłumiące odpowiedź immunologiczną, wspólnie pomagając guzowi przetrwać i opierać się terapii.
Nieustanne zmiany: jak energia guza przesuwa się w czasie
Metabolizm guza nie jest tylko zróżnicowany w danym momencie; jest też wysoce dynamiczny. W miarę wzrostu guza napotyka on zmieniające się warunki, takie jak niski poziom tlenu, nagromadzenie kwasu, brak składników odżywczych i zmiany sztywności tkanki. W surowych, niskotlenowych warunkach wiele komórek nowotworowych przełącza się w stronę glikolizy. Przy nagromadzeniu kwasów lub głodzie cukrowym mogą z kolei przesunąć się ku większemu wykorzystaniu OXPHOS. Ta sama elastyczność pojawia się podczas kluczowych etapów biologicznych. Komórki szybko dzielące się polegają na glikolizie, by generować elementy budulcowe do nowego DNA, lipidów i błon. Komórki odpoczywające lub krążące we krwi często bardziej polegają na OXPHOS. Podczas inwazji i przerzutów komórki nowotworowe wielokrotnie dostosowują wybór paliwa: niektóre etapy sprzyjają glikolizie, inne OXPHOS, a komórki przerzutowe kolonizujące nowe narządy dopasowują swój metabolizm do „gleby” docelowej tkanki.
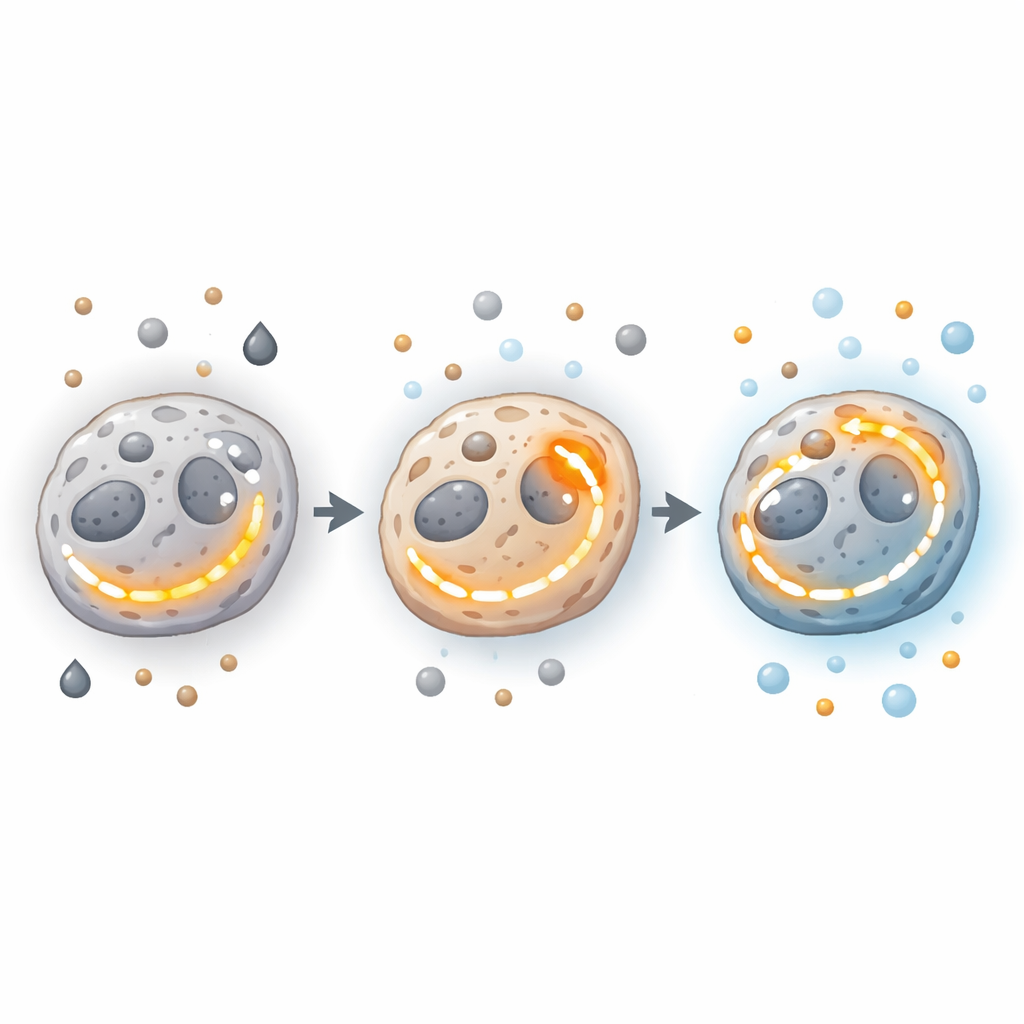
Geny, enzymy i „elektrownie” stojące za przełączaniem
Głębiej w maszynerii komórkowej geny i enzymy kierują tymi decyzjami energetycznymi. Onkogeny i geny supresorowe mogą pchać komórki ku glikolizie lub OXPHOS, albo umożliwiać jednoczesne zwiększenie obu dróg. Mutacje lub zmiany w kluczowych enzymach TCA, takich jak te obsługujące cytrynian, bursztynian czy izocytrynian, mogą przechylić równowagę, czasem napędzając sygnały sprzyjające nowotworowi, takie jak tworzenie naczyń krwionośnych i inwazja. Enzymy stojące na kluczowych rozdrożach — na przykład kinaza pirogronianowa M2, która pomaga zdecydować, czy węgiel pochodzący z cukru zostanie wykorzystany jako energia czy materiał budulcowy — łączą glikolizę z funkcją mitochondrialną. Równocześnie różnice w liczbie, strukturze i wydajności mitochondriów w różnych obszarach guza jeszcze bardziej poszerzają spektrum możliwych stanów energetycznych.
Ponowne przemyślenie terapii przez zmieniający się cel energetyczny
Ponieważ komórki guza potrafią przełączać się między glikolizą a OXPHOS, samo zablokowanie jednej ścieżki często nie wystarcza; nowotwór może przekierować wykorzystanie paliwa i przetrwać. Autorzy argumentują, że metabolizm energetyczny w raku jest tylko chwilowo stabilny i zasadniczo oraz nieustannie się zmienia. Proponują postrzeganie guzów przez „spectrum metabolizmu energetycznego”, które trzeba mierzyć w czasie, a nie tylko raz. W praktyce może to oznaczać śledzenie preferencji paliwowych guza na różnych etapach choroby i łączenie inhibitorów glikolizy i OXPHOS w dostosowanych kombinacjach. Takie dynamiczne strategie ukierunkowane na metabolizm mogą skuteczniej odciąć dopływ energii do guza, ograniczyć jego zdolność do adaptacji i poprawić długoterminową kontrolę choroby.
Cytowanie: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Słowa kluczowe: metabolizm nowotworu, glikoliza, fosforylacja oksydacyjna, mikrośrodowisko guza, plastyczność metaboliczna