Clear Sky Science · pl
Przejście śródbłonkowo-mezenchymalne indukowane przez APOA2 i przeprogramowanie metabolizmu lipidów w nowotworze nadają oporność na leki antyangiogenne poprzez TGF-β
Dlaczego to odkrycie ma znaczenie dla pacjentów
Lekarze coraz częściej stosują leki, które „głodzą” guzy wątroby, odcinając ich dopływ krwi, lecz u wielu pacjentów po początkowej poprawie choroba przestaje reagować na terapię. W tym badaniu zadano pilne pytanie: dlaczego niektóre raki wątroby stają się oporne na leczenie blokujące naczynia krwionośne i jak można im przeciwdziałać? Naukowcy odkryli ukrytą współpracę między białkiem transportującym tłuszcze we krwi a silnym sygnałem wzrostu, która pozwala nowotworom przesterować zarówno naczynia krwionośne, jak i sposób wykorzystania energii, wskazując na alternatywną strategię leczenia trudnej do wyleczenia choroby.
Guz, który uczy się żyć bez dotychczasowego „liniowego zasilania”
Rak wątrobowokomórkowy, najczęstsza postać raka wątroby, silnie zależy od powstawania nowych naczyń krwionośnych. Standardowe leki w zaawansowanej chorobie mają zablokować kluczową ścieżkę wzrostu naczyń opartą na VEGF i jego receptorze VEGFR2. Mimo to u wielu pacjentów guzy dalej rosną pomimo terapii. Porównując próbki guzów od pacjentów reagujących i niereagujących na lek antyangiogenny apatinib, autorzy zaobserwowali, że jeden gen, APOA2, wyróżniał się. Guzy od pacjentów opornych miały znacznie wyższy poziom APOA2 — białka znanego przede wszystkim z roli w transporcie tłuszczów we krwi. Zasugerowało to, że APOA2 może pomagać nowotworom unikać leków celujących naczynia.
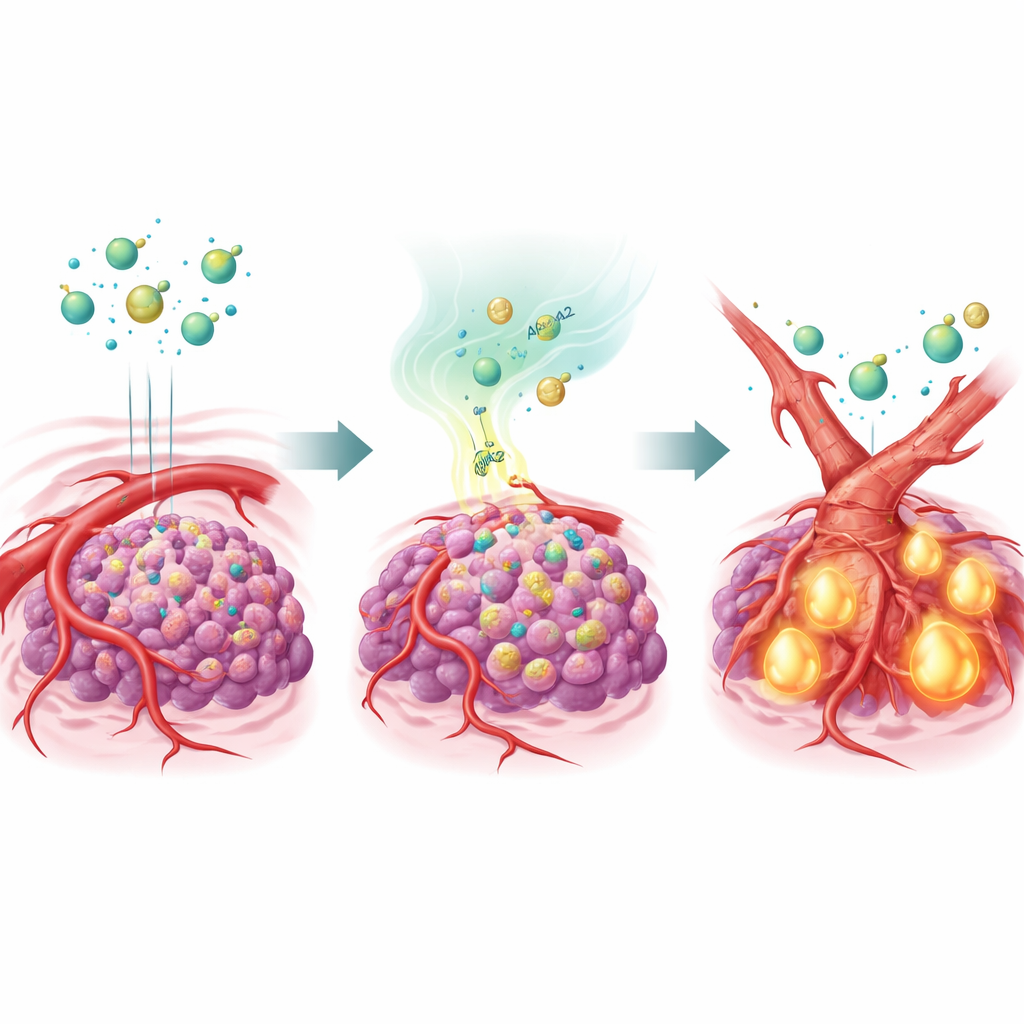
Białko transportujące tłuszcze, które przekształca naczynia krwionośne
Aby sprawdzić tę hipotezę, zespół genetycznie zmodyfikował komórki raka wątroby tak, by nadprodukowały APOA2, i wszczepił je myszom. Po leczeniu kilkoma różnymi lekami antyangiogennymi guzy bogate w APOA2 w dużej mierze ignorowały terapię: ich naczynia utrzymywały się, a nowotwory nadal rosły. Szczegółowa analiza wykazała silną aktywację sygnału nadrzędnego zwanego TGF-β w tych guzach, a jego poziomy były podwyższone zarówno w mikrośrodowisku guza, jak i we krwi zwierząt. TGF-β działał na komórki wyściełające naczynia, skłaniając je do zmiany tożsamości w procesie zwanym przejściem śródbłonkowo-mezenchymalnym. W miarę przechodzenia w bardziej bliznowaty, mezenchymalny stan, te komórki utraciły dużą część VEGFR2 — właśnie tego celu, do którego adresowane są leki antyangiogenne. W efekcie naczynia przebudowały się w formę, której leki nie były już w stanie skutecznie rozpoznać ani zaatakować.
Metaboliczne obejście, które utrzymuje komórki nowotworowe przy życiu
Historia nie kończy się na ścianie naczynia. Ten sam sygnał TGF-β napędzany przez APOA2 przeprogramował także sposób zasilania komórek nowotworowych. Zamiast polegać głównie na rozkładzie cukrów, komórki z wysokim poziomem APOA2 zaczęły pobierać więcej wolnych kwasów tłuszczowych ze środowiska i utleniać je w mitochondriach poprzez oksydację kwasów tłuszczowych. Pomiary wykorzystania składników odżywczych i zużycia tlenu wykazały, że komórki te stały się bardziej zależne od tłuszczu jako źródła energii i wytwarzały więcej ATP. Ta zmiana pozwoliła komórkom guza utrzymywać szybkie podziały i unikać śmierci komórkowej, nawet gdy podaż krwi była ograniczana przez terapię antyangiogenną.
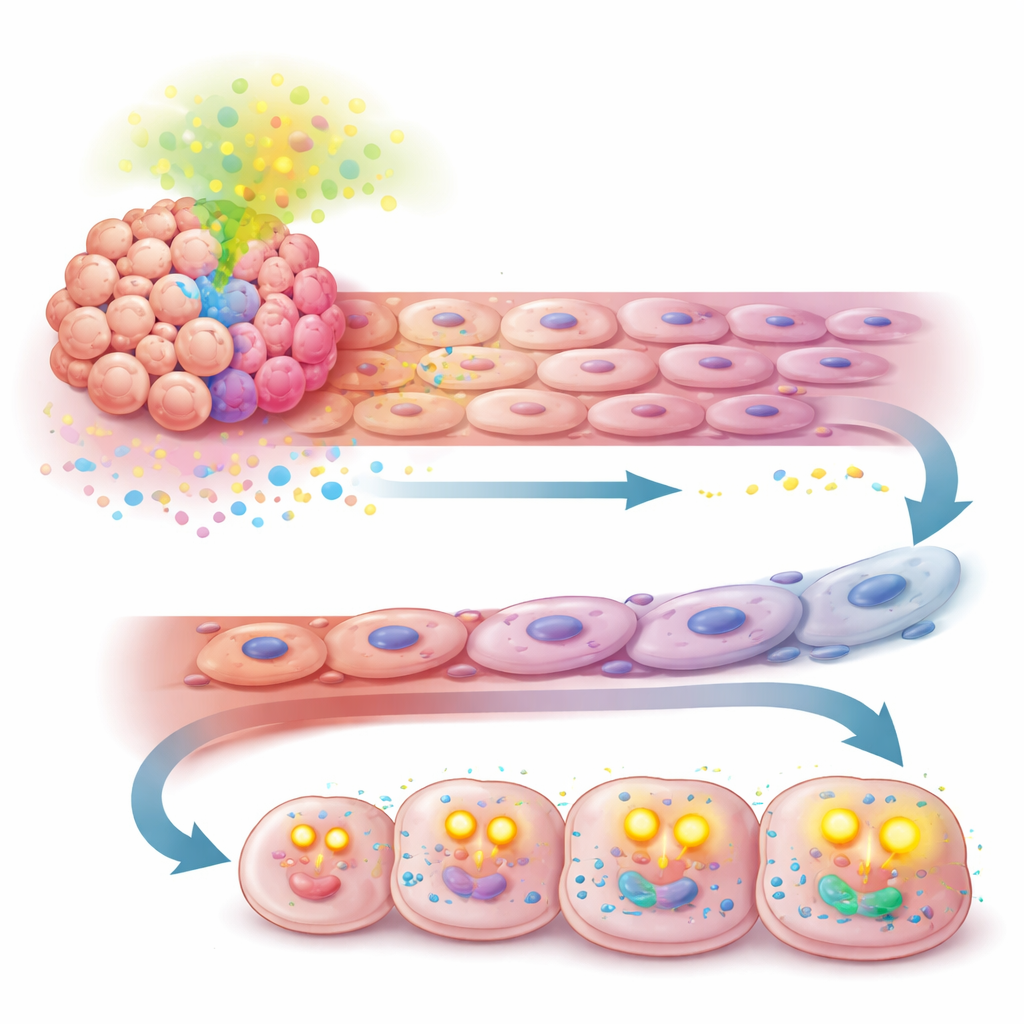
Wykorzystanie słabości jako nowego celu terapeutycznego
Co istotne, gdy badacze zablokowali TGF-β, korzyści wynikające z wysokiego poziomu APOA2 zniknęły. Hamowanie tego sygnału w modelach mysich zmniejszyło nieprawidłowe zmiany naczyniowe, przywróciło wrażliwość na terapię i spowolniło wzrost guza. Jeszcze bardziej obiecujące było to, że przeciwciało dwufunkcyjne jednocześnie blokujące TGF-β i punkt kontrolny immunologiczny PD-1 działało lepiej niż każdy z tych zabiegów osobno w guzach z wysokim APOA2. Wyniki sugerują, że w podgrupie raków wątroby oznaczonych wysokim APOA2 choroba cicho przestawiła swoją zależność z klasycznej ścieżki VEGF na trasę zdominowaną przez TGF-β, która podtrzymuje zarówno naczynia, jak i metabolizm guza.
Co to oznacza dla przyszłej opieki nad rakiem wątroby
Dla osoby nieznającej tematu kluczowa wiadomość brzmi: niektóre guzy wątroby unikają działania obecnych leków naczyniowych przez przesterowanie zarówno „instalacji” naczyniowej, jak i źródła energii. Białko związane z tłuszczami, APOA2, nasila sygnał TGF-β, który z kolei maskuje naczynia tak, że istniejące leki ich nie rozpoznają, i uczy komórki nowotworowe życia z tłuszczów zamiast cukru. Badanie sugeruje, że oznaczanie guzów pod kątem APOA2 mogłoby wskazać pacjentów, którzy prawdopodobnie nie odniosą korzyści z standardowych leków antyangiogennych, ale mogą odpowiedzieć na leki blokujące TGF-β, zwłaszcza w połączeniu z nowoczesną immunoterapią. Krótko mówiąc, ujawniając mechanizmy adaptacji guzów, praca ta wskazuje na bardziej spersonalizowaną strategię ataku zarówno na naczynia, jak i na źródło energii, od których zależą te odporne nowotwory.
Cytowanie: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Słowa kluczowe: rak wątrobowokomórkowy, oporność na leki antyangiogenne, APOA2, sygnalizacja TGF-beta, metabolizm lipidów nowotworu