Clear Sky Science · pl
KCTD1 stabilizuje c-Myc, aby zwiększyć ekspresję PD-L1 i tłumić odpowiedź przeciwnowotworową w raku wątrobowokomórkowym
Dlaczego to ma znaczenie dla przyszłej opieki onkologicznej
Wiele osób z rakiem wątroby nie odnosi korzyści z najnowszych, obiecujących immunoterapii, których celem jest uwolnienie własnych komórek T organizmu do walki z guzem. Badanie to analizuje, dlaczego główny typ raka wątroby — rak wątrobowokomórkowy — potrafi nadal ukrywać się przed atakiem immunologicznym nawet podczas leczenia, i identyfikuje nowy molekularny przełącznik, nazwany KCTD1, który mógłby zwiększyć skuteczność istniejących leków immunoterapeutycznych.
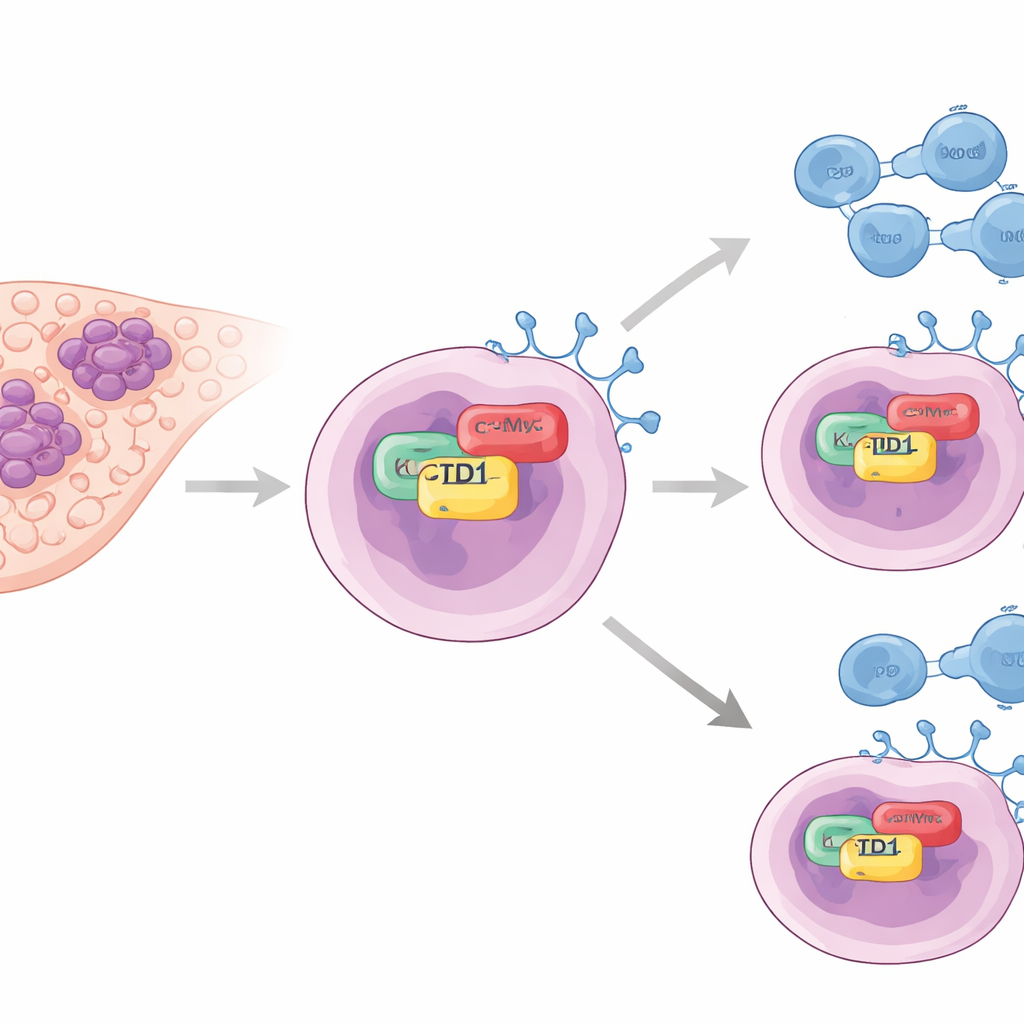
Ukryty pomocnik guzowych „wyłączników”
Autorzy skupili się na białku o nazwie KCTD1, wcześniej powiązanym ze wzrostem guzów wątroby, lecz słabo zbadanym w kontekście ucieczki przed układem odpornościowym. W próbkach nowotworowych od pacjentów stwierdzili, że poziom KCTD1 był wyraźnie wyższy w tkance nowotworowej w porównaniu z prawidłową wątrobą. Co istotne, guzy bogate w KCTD1 miały również wysoki poziom PD-L1 — białka powierzchniowego na komórkach nowotworowych, które łączy się z PD-1 na komórkach T i skutecznie nakazuje układowi odpornościowemu odpuścić. Pacjenci, których guzy wykazywały niższy poziom KCTD1, mieli tendencję do dłuższego przeżycia, co sugeruje związek tego białka z ciężkością choroby i siłą immunologicznej ochrony guza.
Łączenie molekularnych kropek wewnątrz komórek nowotworowych
Aby zrozumieć, jak KCTD1 zwiększa PD-L1, zespół wykorzystał linie komórkowe raka wątroby hodowane w laboratorium. Gdy zmniejszano poziom KCTD1, spadał poziom białka PD-L1, a pozostający PD-L1 ulegał szybszemu rozpadowi, co wskazuje, że KCTD1 pomaga stabilizować PD-L1, a nie jedynie włącza transkrypcję jego genu. Dzięki biochemicznym eksperymentom pull-down i mikroskopii fluorescencyjnej wykazano, że KCTD1 fizycznie wiąże się z innym kluczowym czynnikiem nowotworowym — onkoproteiną c-Myc — w jądrze komórkowym. Interakcja ta zachodzi poprzez specyficzne obszary kontaktu na obu białkach i prowadzi do stabilizacji c-Myc, co z kolei zwiększa produkcję PD-L1. Gdy obniżano tylko c-Myc, PD-L1 malał nawet przy obfitym KCTD1, co stawia c-Myc jako kluczowe ogniwo pośrednie w łańcuchu KCTD1–c-Myc–PD-L1.
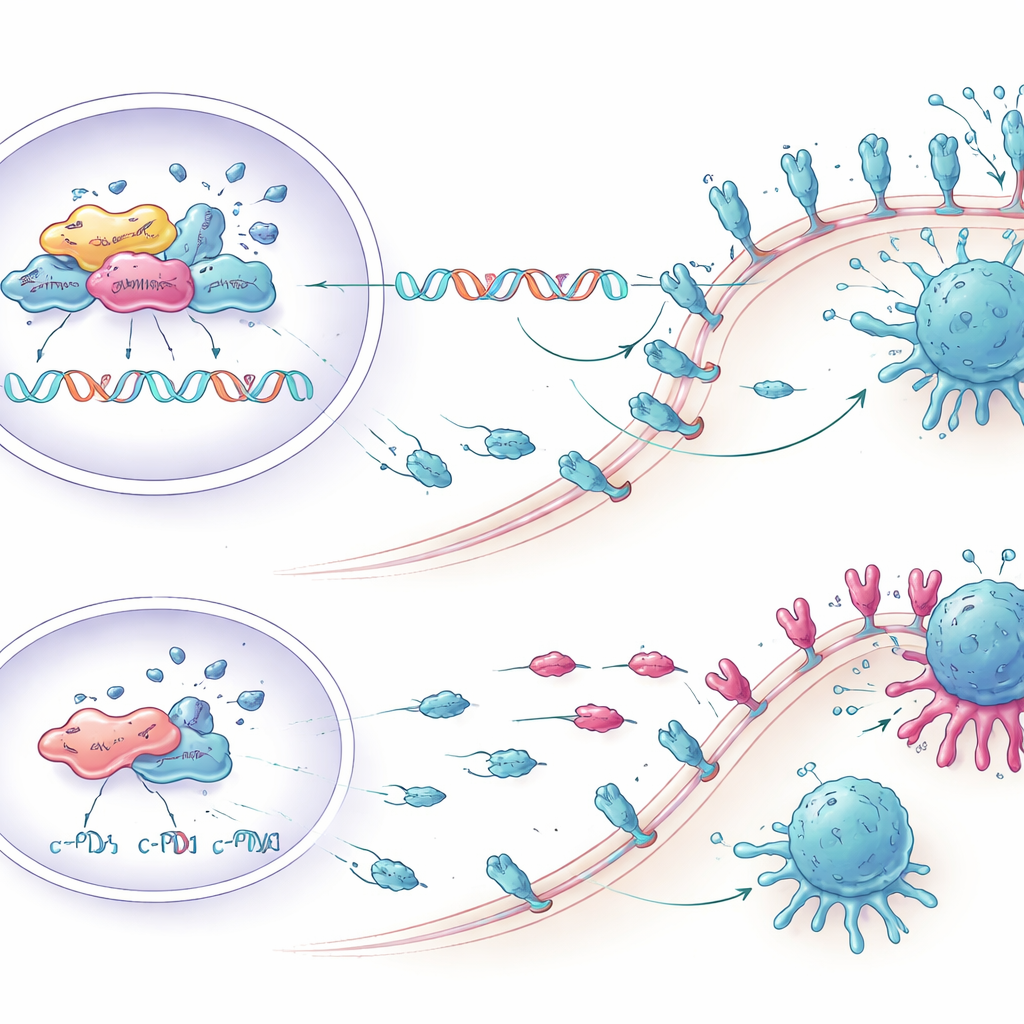
Przywracanie aktywności komórek T w laboratorium
Naukowcy zapytali następnie, czy obniżenie KCTD1 rzeczywiście może wzmocnić atak immunologiczny. Wspólhodowali ludzkie komórki raka wątroby z komórkami odpornościowymi pobranymi od dawców krwi. Komórki nowotworowe zmodyfikowane w celu obniżenia KCTD1, a przez to także PD-L1, wywoływały silniejszą odpowiedź limfocytów CD8 — głównych zabójców komórek nowotworowych. Więcej tych komórek T produkowało prozapalne molekuły, takie jak TNF-α i interferon gamma, wykazywało wyższe markery wzrostu i aktywacji oraz miało mniej oznak wyczerpania. W konsekwencji, więcej komórek nowotworowych przeszło programowaną śmierć komórkową po stłumieniu KCTD1, dowodząc, że zmiany molekularne przekładają się na rzeczywisty wzrost skuteczności zabijania przez układ odpornościowy.
Testowanie mechanizmu na myszach
Aby sprawdzić, czy ten sam wzorzec występuje in vivo, zespół wszczepił do wątrób myszy komórki raka wątroby pozbawione KCTD1. Guzy z obniżonym KCTD1 formowały mniej i mniejsze guzki, wykazywały wolniejszy podział komórek i większy odsetek komórek nowotworowych poddających się śmierci. Te guzy także wykazywały niższą ekspresję c-Myc i PD-L1. Usunięcie limfocytów CD8 z myszy znacznie zniwelowało te korzyści, co wskazuje, że spowolnienie wzrostu guza zależało w dużej mierze od aktywności komórek T. Wreszcie, połączenie wyciszenia KCTD1 z przeciwciałem anty–PD-1 — istniejącym lekiem blokującym punkt kontrolny immunologiczny — doprowadziło u myszy do najmniejszego obciążenia nowotworem i największego napływu limfocytów CD4 i CD8 do guza.
Co to może znaczyć dla pacjentów
Podsumowując, praca identyfikuje KCTD1 jako centralnego koordynatora, który stabilizuje c-Myc, zwiększa poziom PD-L1 na komórkach raka wątroby i osłabia atak limfocytów CD8. Zakłócenie tej ścieżki sprawia, że guzy stają się bardziej podatne na układ odpornościowy i bardziej wrażliwe na leki blokujące PD-1 u myszy. Dla pacjentów sugeruje to, że leki celujące w KCTD1 lub jego powierzchnię kontaktową z c-Myc mogłyby w przyszłości być łączone z aktualnymi immunoterapiami, by więcej osób z rakiem wątroby odniosło trwałą korzyść z kontroli immunologicznej choroby.
Cytowanie: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Słowa kluczowe: rak wątrobowokomórkowy, immunoterapia nowotworów, ścieżka PD-1 PD-L1, sygnalizacja c-Myc, odporność komórek T przeciw nowotworom