Clear Sky Science · pl
Ochronne zwiększenie ekspresji metalotioneiny-2A w zwyrodnieniu dysku międzykręgowego hamuje ferroptozę komórek jądra miażdżystego poprzez aktywację szlaku PI3K/AKT/mTOR
Dlaczego ten problem z kręgosłupem ma znaczenie
Ból dolnej części pleców dotyka setek milionów ludzi na całym świecie i jest jedną z głównych przyczyn niepełnosprawności. Jednym z istotnych winowajców jest stopniowe zużywanie się poduszek między kręgami, zwanych dyskami międzykręgowymi. W tym badaniu pojawia się pytanie z nadzieją: czy własne ochronne cząsteczki organizmu mogą zabezpieczać te dyski przed uszkodzeniem, a ich wzmocnienie otworzyłoby drogę do nowych terapii przewlekłego bólu pleców? 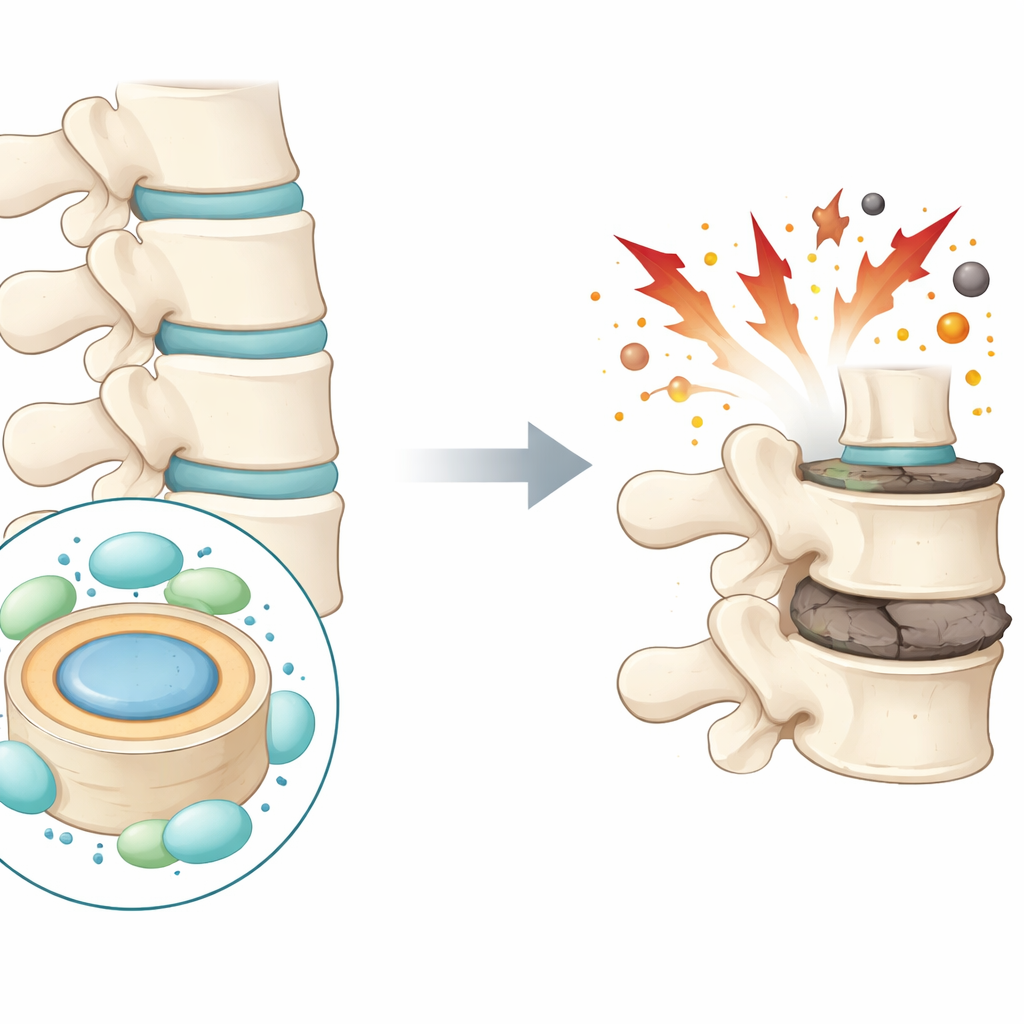
Poduszki wewnątrz kręgosłupa
Każdy dysk międzykręgowy ma miękkie, żelowe centrum zwane jądrem miażdżystym, otoczone twardszym pierścieniem. Struktury te działają jak amortyzatory kręgosłupa. W miarę zwyrodnienia dysków komórki w części centralnej obumierają, a wspierająca macierz białek i wody ulega degradacji. Dysk spłaszcza się i pęka, co może prowadzić do bólu i ograniczenia ruchomości. Autorzy koncentrują się na specyficznym typie obumierania komórek, który dopiero niedawno zyskał zainteresowanie w wielu schorzeniach: żelazozależnej, oksydacyjnej formie śmierci zwanej ferroptozą. Podejrzewają, że ten proces odgrywa kluczową rolę w rozkładzie dysku.
Gdy żelazo i utlenianie idą nie tak
Ferroptoza jest uruchamiana, gdy wolne żelazo i reaktywne cząsteczki tlenu gromadzą się w komórkach, uszkadzając lipidy błon komórkowych i w szczególności małe elektrownie komórkowe — mitochondria. Zespół przeanalizował dane z sekwencjonowania pojedynczych komórek z ludzkiej tkanki dyskowej i znalazł wyraźne ślady zmian w genach związanych z ferroptozą w dyskach ulegających zwyrodnieniu. W szczególności markery, które normalnie chronią komórki przed tego rodzaju uszkodzeniem, takie jak enzym GPX4, były zmniejszone w zużytych dyskach zarówno u pacjentów, jak i u szczurów. Jednocześnie wzrosły markery sprzyjające uszkodzeniu i zapaleniu, ukazując obraz komórek pod ostrzałem oksydacyjnym w miarę postępu zwyrodnienia dysku.
Wbudowany metal‑wiążący obrońca
Wśród wielu genów, które zmieniły się w chorych dyskach, jeden wyróżniał się szczególnie: metalotioneina‑2A (MT2A), małe białko wiążące metale, takie jak cynk, i neutralizujące szkodliwe reaktywne cząsteczki. Poziomy MT2A były wyraźnie wyższe w dyskach o cięższym stopniu zwyrodnienia u ludzi oraz w modelu urazu dysku u szczurów. Na pierwszy rzut oka wydaje się to paradoksem — dlaczego cząsteczka ochronna rośnie w uszkodzonym tkance? Badacze wysunęli hipotezę, że organizm uruchamia odpowiedź kompensacyjną, próbując przeciwdziałać wzrostowi stresu wywołanego żelazem. W hodowlach komórkowych, gdy komórki dyskowe wystawiono na działanie związku naśladującego stres oksydacyjny, poziomy MT2A wzrastały wraz ze spadkiem kondycji komórek, co wzmacniało przekonanie, że jest on włączany jako mechanizm obronny.
Wyłączanie i wzmacnianie ochrony
Aby sprawdzić, czy MT2A jest rzeczywiście ochronny, a nie szkodliwy, zespół ostrożnie zmniejszał lub zwiększał jego poziomy w ludzkich komórkach dyskowych. Gdy zablokowano produkcję MT2A, stres oksydacyjny powodował znacznie większe obumieranie komórek, większe gromadzenie żelaza, silniejsze uszkodzenie lipidów i poważne uszkodzenie mitochondriów. Gdy natomiast podniesiono poziom MT2A lub potraktowano komórki znanym inhibitorem ferroptozy, wiele z tych problemów uległo złagodzeniu: spadły poziomy żelaza i reaktywnych cząsteczek, odnowiły się ochronne antyoksydanty, a mitochondria wyglądały zdrowiej. Zmiany te odzwierciedliły się także w lepszym zachowaniu białek macierzy podporowej komórek, które są kluczowe dla utrzymania dysków pulchnych i funkcjonalnych. 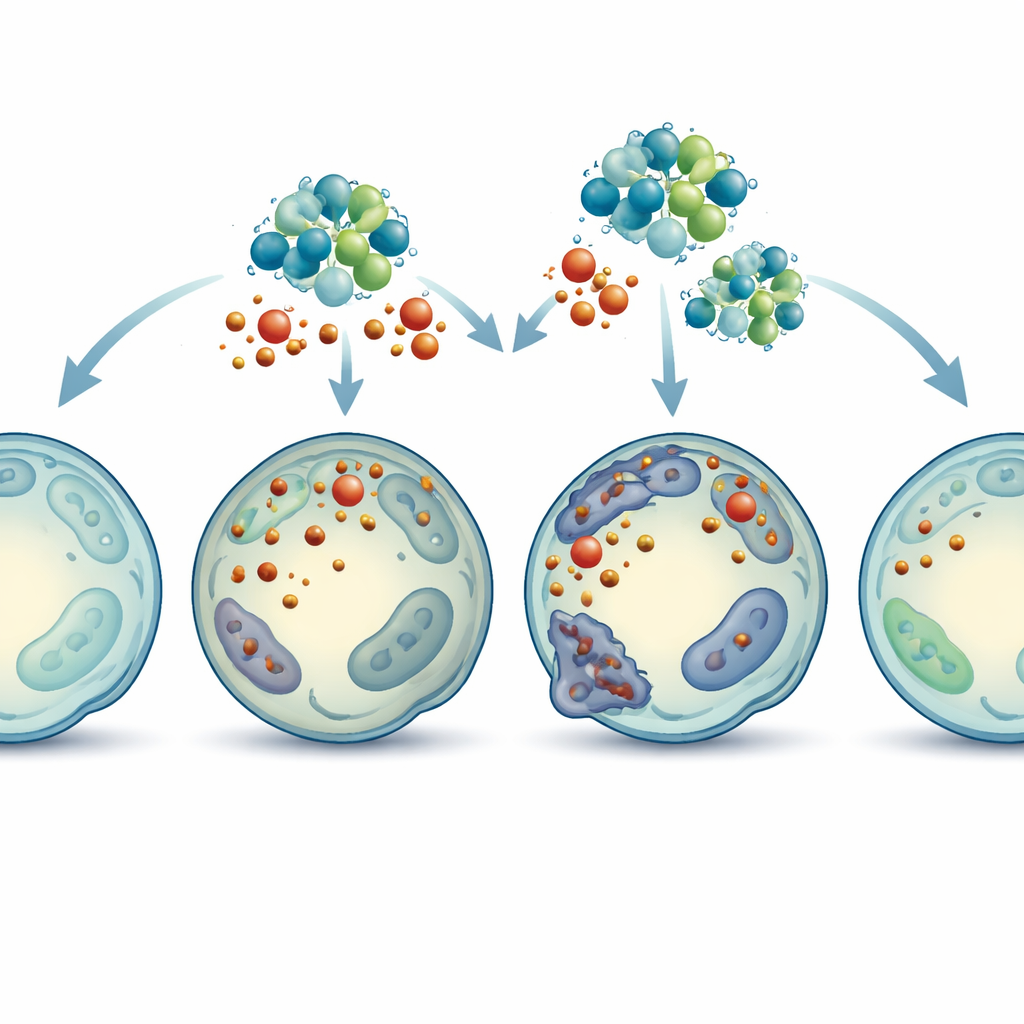
Kluczowa droga sygnałowa wewnątrz komórki
Pogłębiając analizę, naukowcy przyjrzeli się, jak MT2A przekazuje sygnały ochronne wewnątrz komórek. Sekwencjonowanie genów i pomiary białek wskazały na szlak PI3K/AKT/mTOR, dobrze znany system regulacyjny wpływający na wzrost, metabolizm i przeżycie. Obniżenie poziomu MT2A tłumiło aktywność tego szlaku, podczas gdy jego podniesienie włączało go. Gdy badacze zastosowali leki blokujące różne etapy tego szlaku, korzyści płynące z nadekspresji MT2A zniknęły: markery ferroptozy ponownie wzrosły, uszkodzenia oksydacyjne powróciły, a komórki dyskowe utraciły więcej swoich białek strukturalnych. Sugeruje to, że MT2A chroni komórki dysku przede wszystkim przez aktywację tej pro‑przeżyciowej drogi sygnałowej, która z kolei ogranicza ferroptozę.
Dowód koncepcji na zwierzętach
Na koniec zespół sprawdził, czy zwiększenie MT2A może rzeczywiście spowolnić zwyrodnienie dysku w żywym organizmie. U szczurów wywołali uszkodzenie dysku poprzez nakłucie igłą, a następnie dostarczyli wirusa zaprojektowanego do zwiększenia MT2A bezpośrednio do dysku. Tygodnie później obrazowanie i analiza tkankowa wykazały, że dyski z dodatkowymi poziomami MT2A zachowały większą wysokość, miały wyraźniejszą strukturę wewnętrzną i wykazywały mniejsze utraty kluczowych białek macierzy w porównaniu z nieleczonymi uszkodzonymi dyskami. Markery ferroptozy również były zmniejszone, co wspiera tezę, że MT2A pomaga chronić poduszkę dysku przed zapadaniem się pod wpływem stresu oksydacyjnego i żelazowego.
Co to oznacza dla przyszłej opieki nad bólem pleców
Podsumowując, praca sugeruje, że MT2A nie jest jedynie biernym obserwatorem, lecz wbudowanym czynnikiem bezpieczeństwa, który zwiększa się, gdy dyski zaczynają zawodzić, próbując bronić komórek przed szkodliwą, żelazozależną oksydacją. Poprzez aktywację wewnętrznej ścieżki przeżyciowej MT2A ogranicza specyficzną formę śmierci komórkowej, zachowuje strukturę dysku i spowalnia zwyrodnienie — przynajmniej w modelach zwierzęcych i hodowlach komórek. Dla pacjentów wskazuje to, że MT2A i jego partnerzy sygnałowi są obiecującymi celami dla leków lub terapii genowych mających na celu ochronę lub odnowę dysków kręgosłupa, co potencjalnie może zaoferować więcej niż tylko ulgę w bólu czy zabieg chirurgiczny w dłuższej perspektywie.
Cytowanie: Cai, H., Zheng, Hl., Chen, Qz. et al. The protective up-regulation of metallothionein-2A in intervertebral disc degeneration inhibits nucleus pulposus cell ferroptosis through activation of the PI3K/AKT/mTOR pathway. Cell Death Discov. 12, 111 (2026). https://doi.org/10.1038/s41420-026-02972-9
Słowa kluczowe: bół krzyża, zwyrodnienie dysku międzykręgowego, ferroptoza, metalotioneina-2A, szlak PI3K AKT mTOR