Clear Sky Science · pl
Multi-omika ujawnia heterogenność i funkcjonalne populacje progenitorów oligodendrocytów indukowanych przez ludzkie komórki macierzyste nerwowe
Dlaczego ochrona izolacji mózgu ma znaczenie
Połączenia w naszym mózgu zależą od tłustej powłoki zwanej mieliną, która owija włókna nerwowe jak izolacja na kablach elektrycznych. Gdy mielina ulega uszkodzeniu, jak w stwardnieniu rozsianym i innych chorobach, przekazywanie sygnałów zwalnia lub zawodzi, powodując problemy z ruchem, wzrokiem i myśleniem. W tym badaniu analizowano specjalną grupę ludzkich komórek zdolnych do odbudowy mieliny i postawiono praktyczne pytanie: które komórki będą najlepsze do przyszłych terapii komórkowych naprawiających tę kluczową izolację?
Od komórek początkowych do producentów mieliny
Naukowcy zaczęli od ludzkich nerwowych komórek macierzystych — wszechstronnych komórek początkowych pobranych z tkanki płodowej mózgu, które są już ukierunkowane na tworzenie komórek układu nerwowego. W laboratorium skierowali te komórki, by przekształciły się w progenitory oligodendrocytów, czyli hOPC, bezpośrednich prekursorów komórek wytwarzających mielinę. Pod mikroskopem komórki zmieniały kształt z prostych, okrągłych w bardziej złożone z licznymi wypustkami i włączały charakterystyczne białka oznaczające kolejne etapy dojrzewania w kierunku komórek produkujących mielinę. Zapewniło to wiarygodne, stosunkowo bezpieczne źródło ludzkich prekursorów budujących mielinę do szczegółowej analizy.
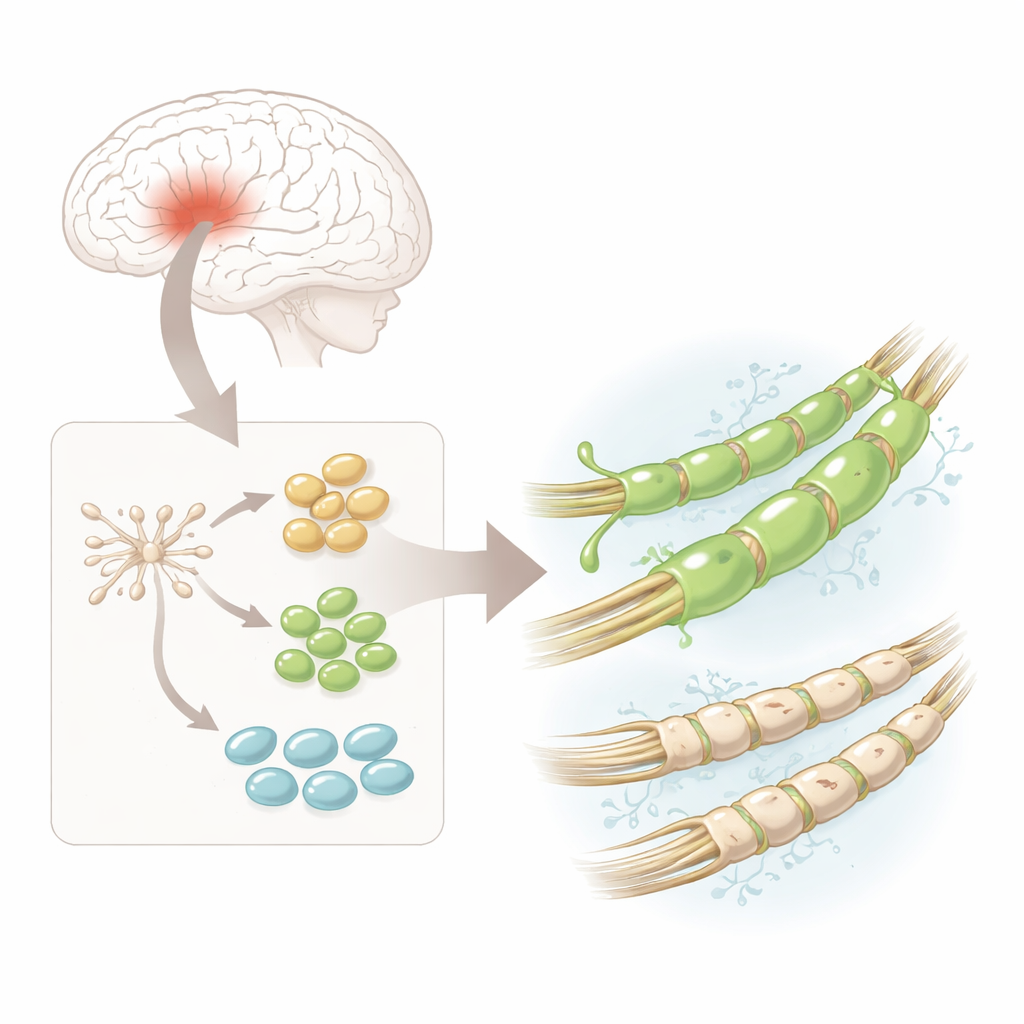
Jeden typ komórki, wiele ukrytych odmian
Wykorzystując sekwencjonowanie RNA pojedynczych komórek — metodę odczytującą, które geny są aktywne w tysiącach pojedynczych komórek — zespół odkrył, że hOPC nie były jednorodne. Zamiast tego pogrupowały się na trzy główne stadia: wczesne „pre-progenitory”, bardziej zaawansowane progenitory oraz komórki zbliżające się do pełnej tożsamości oligodendrocytu. We wszystkich tych stadiach wyróżniał się jeden gen: PDGFRA, kodujący receptor powierzchniowy komórki. Wysoce czuła metoda obrazowania RNA-Scope potwierdziła, że transkrypt i białko PDGFRA były bardziej obfite niż inne kluczowe markery na każdym etapie, co sugeruje, że ten receptor może definiować szczególnie zdolne komórki budujące mielinę.
Wyodrębnianie najsilniejszych komórek naprawczych
Aby to sprawdzić, naukowcy rozdzielili hOPC na dwie grupy w zależności od obecności receptora PDGFR-α na powierzchni. Porównali następnie komórki PDGFR-α dodatnie, PDGFR-α ujemne oraz nierozdzielone komórki w szeregu testów funkcjonalnych. Po przeszczepieniu do myszy „shiverer”, które nie mogą wytwarzać prawidłowej mieliny, komórki PDGFR-α dodatnie wytworzyły gęstszą, bardziej zwartą mielinę wokół włókien nerwowych niż inne grupy. Komórki te także migrowały dalej i szybciej się namnażały w testach laboratoryjnych. Innymi słowy, populacja PDGFR-α dodatnia była najwydajniejsza w przemieszczaniu się tam, gdzie była potrzebna, zwiększaniu liczebności i odbudowie izolacji.
Wewnętrzne sygnały napędzające wzrost i naprawę
Idąc dalej, zespół porównał aktywność genów między komórkami PDGFR-α dodatnimi i ujemnymi. Stwierdzili, że komórki dodatnie włączały sieci genów zaangażowanych w wzrost komórek glejowych i tworzenie mieliny oraz kilka kluczowych szlaków sygnałowych wewnątrzkomórkowych. Dwa szlaki szczególnie się wyróżniały: PI3K–AKT–mTOR, od dawna powiązany z wzrostem komórek i produkcją mieliny, oraz sygnalizacja TGF-β, która wpływa na wybory losu młodych komórek mózgowych. Dane sugerowały, że aktywacja PDGFR-α wpływa na PI3K–AKT–mTOR, które z kolei wzmacnia sygnały związane z TGF-β, razem skłaniając komórki ku stanie skutecznych producentów mieliny.
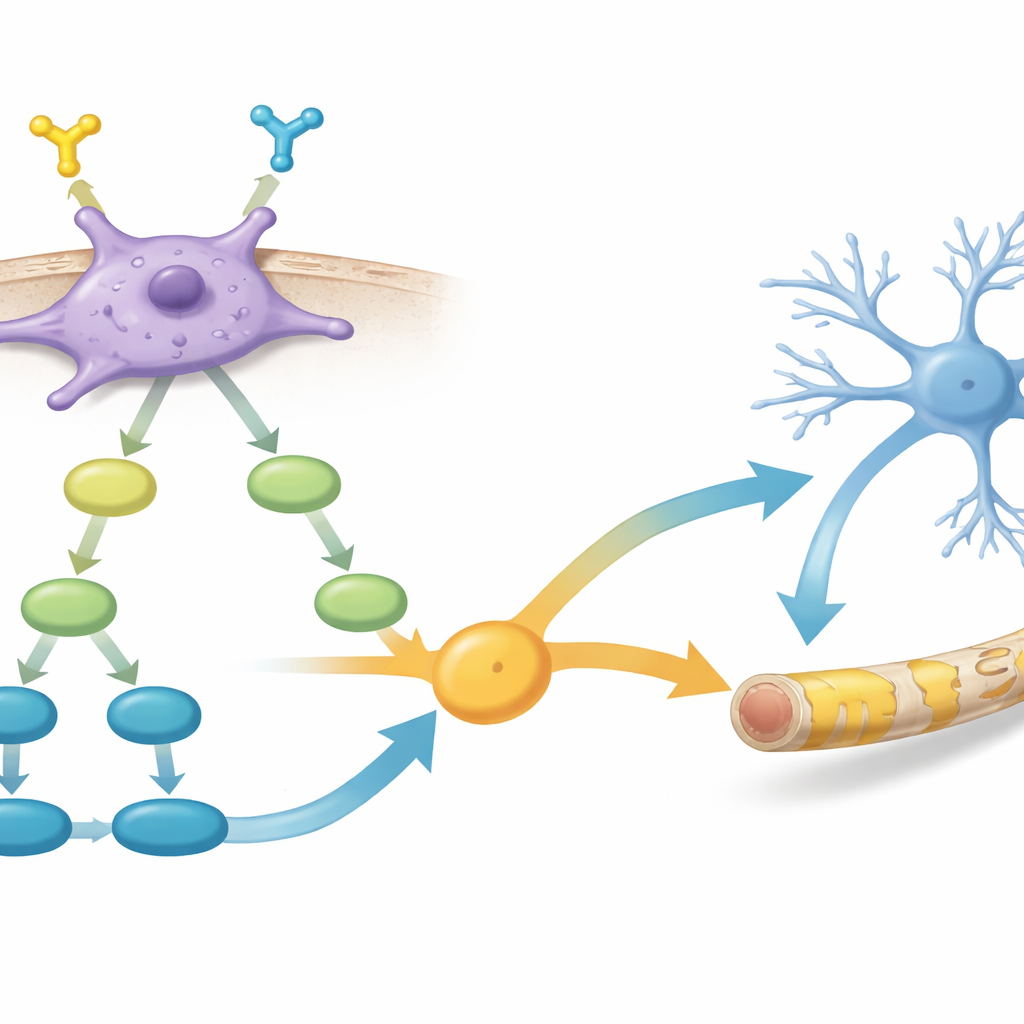
Wzmacnianie naprawy mieliny za pomocą chemicznego wsparcia
Naukowcy zapytali następnie, czy można dodatkowo ulepszyć te obiecujące komórki. Poddali PDGFR-α dodatnie hOPC działaniu małocząsteczkowego związku aktywującego szlak TGF-β i zbadali zarówno aktywność genów, jak i zachowanie komórek. Po leczeniu komórki wykazywały wyższe poziomy wielu genów związanych z mieliną i tworzyły grubsze, bardziej kompletne pochewki mielinowe po przeszczepieniu do myszy shiverer w porównaniu z nieleczonymi komórkami PDGFR-α dodatnimi. Wyniki te wspierają ideę, że precyzyjne dostrojenie sygnałów wewnątrzkomórkowych w już dobrze wyselekcjonowanych progenitorach może dodatkowo poprawić ich skuteczność jako żywych narzędzi naprawy mieliny.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy przekaz jest taki: nie wszystkie prekursory budujące mielinę są takie same. Dzięki połączeniu zaawansowanych narzędzi do odczytu genów i obrazowania to badanie wskazuje wyróżniającą się podgrupę — hOPC PDGFR-α dodatnie — które lepiej migrują, dzielą się częściej i skuteczniej odbudowują mielinę niż ich odpowiedniki. Wskazuje także wewnętrzne szlaki sygnałowe, które można chemicznie modulować, aby uczynić te komórki jeszcze wydajniejszymi. Razem te wnioski wytyczają mapę drogową dla projektowania bezpieczniejszych, bardziej efektywnych terapii komórkowych przywracających izolację mózgu w chorobach związanych z utratą mieliny.
Cytowanie: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Słowa kluczowe: naprawa mieliny, progenitory oligodendrocytów, komórki macierzyste nerwowe, terapia komórkowa, sekwencjonowanie RNA pojedynczych komórek