Clear Sky Science · pl
Axin1 stabilizuje S-opsynę i utrzymuje przeżycie fotoreceptorów czopkowych przez hamowanie aktywności GSK3β
Jak utrzymać nasze widzenie barwne
Za każdym razem, gdy wchodzimy w światło słoneczne lub spoglądamy na jasny ekran, drobne komórki w naszych oczach pracują intensywnie, zamieniając światło w widzenie. Te komórki, zwane fotoreceptorami, są delikatne i w wielu ślepiących chorobach mogą stopniowo obumierać. Badanie to ujawnia, jak mało znany „organizujący” białko, Axin1, pomaga chronić fotoreceptory czopkowe — komórki odpowiedzialne za widzenie w świetle dziennym i percepcję kolorów — poprzez utrzymywanie kluczowych cząsteczek światłoczułych we właściwym miejscu i łagodzenie niebezpiecznego stresu wewnątrz komórki.
Jak czopki widzą świat
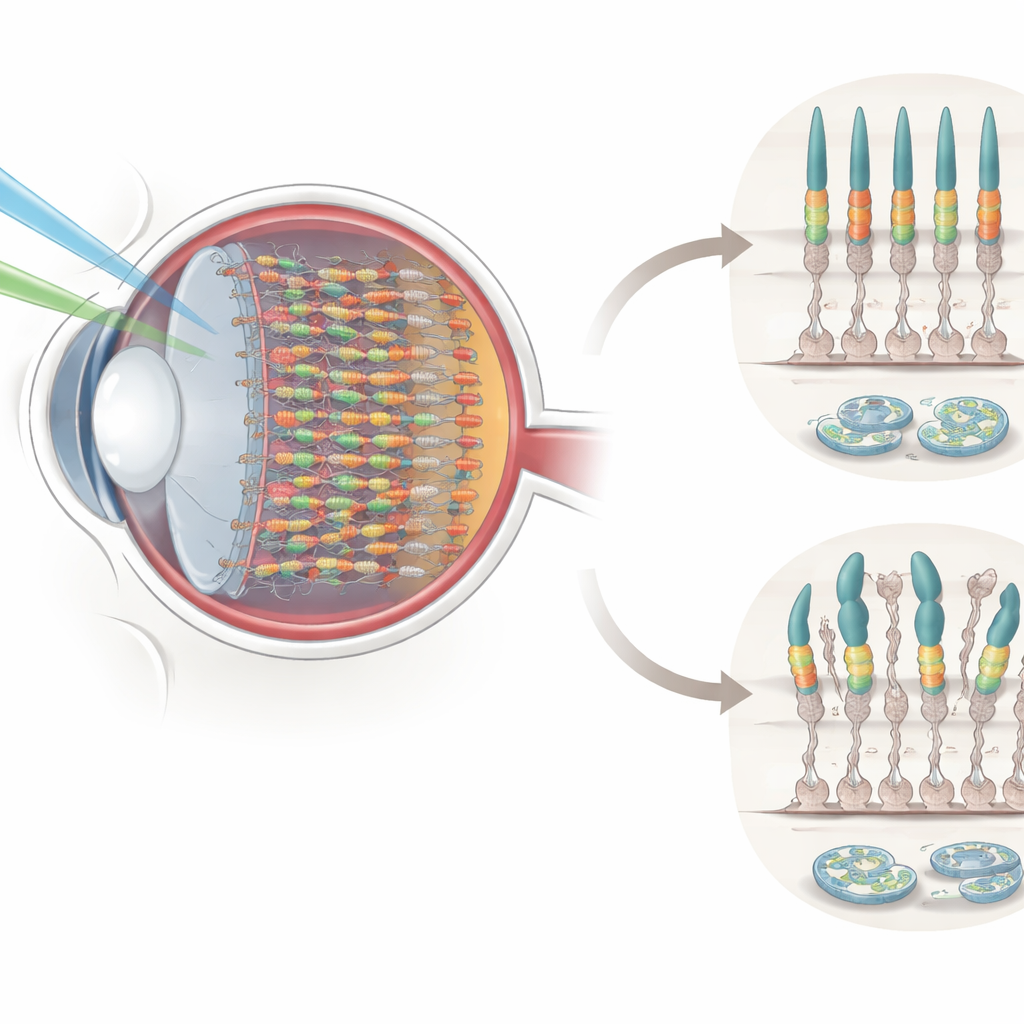
Nasza siatkówka zawiera dwa główne typy fotoreceptorów: pręciki do widzenia przy słabym świetle i bez barw oraz czopki do widzenia w jasnym świetle i rozróżniania barw. Czopki zawierają specjalne pigmenty, w tym S-opsynę, która jest najbardziej wrażliwa na krótkofalowe (niebieskie) światło. Pigmenty te znajdują się w wąskim, ułożonym w stosie obszarze na końcu każdego fotoreceptora zwanym segmentem zewnętrznym, gdzie padające światło jest przekształcane w sygnały elektryczne. Ponieważ ten obszar jest nieustannie bombardowany światłem i musi szybko się odnawiać, jest szczególnie podatny na uszkodzenia oraz na stres w „fabryce” fałdowania białek komórki — retikulum endoplazmatycznym (ER). Gdy ER zostaje przeciążone przez nieprawidłowo sfałdowane lub źle ulokowane białka, może to uruchomić śmierć komórki, przyczyniając się do degeneracji siatkówki i utraty wzroku.
Ukryty organizator w komórkach czopkowych
Naukowcy zwrócili uwagę na Axin1, białko-szablon znane przede wszystkim z organizowania szlaków sygnalizacyjnych w innych częściach organizmu. Dzięki barwieniu o wysokiej rozdzielczości w siatkówkach myszy odkryli, że Axin1 nie jest rozmieszczony równomiernie w oku. Zamiast tego występuje w nadmiarze w fotoreceptorach czopkowych, szczególnie w siatkówce brzusznej (dolnej), dokładnie tam, gdzie wiadomo, że S-opsyna jest najbardziej obfita. W obrębie każdego czopka Axin1 gromadzi się w segmencie zewnętrznym, ściśle pokrywając się z S-opsyną. W czasie dojrzewania Axin1 i S-opsyna pojawiają się razem, przechodząc od małych punktów do wydłużonych struktur przypominających pręciki, które oznaczają dojrzałe segmenty zewnętrzne czopków. To ścisłe dopasowanie przestrzenne i czasowe sugerowało, że Axin1 może być kluczowy dla utrzymania S-opsyny we właściwej pozycji, umożliwiającej efektywne wykrywanie światła.
Co się dzieje, gdy Axin1 zanika
Aby sprawdzić znaczenie Axin1, zespół selektywnie usunął go z komórek czopkowych myszy przy użyciu wirusowego podejścia do edycji genów. Zwierzęta pozbawione Axin1 wykazywały powolne zwężanie źrenicy pod wpływem niebieskiego lub zielonego światła oraz nieprawidłowe zachowanie w teście preferencji światło–ciemność, co wskazywało na upośledzone postrzeganie światła. Pod mikroskopem ich segmenty zewnętrzne czopków wyglądały na zdezorganizowane: poziomy S-opsyny spadły, a zamiast tworzyć gładkie, pręcikowate struktury, pigment rozpadł się na rozproszone punktowe skupiska. Otaczająca tkanka siatkówki również wykazywała wczesne oznaki problemów. Połączenia szczelne w warstwie barwnikowej wspierającej zostały zaburzone, markery synaptyczne między czopkami a neuronami dalszego rzędu były zredukowane, a komórki glejowe — zwykle ciche komórki wspierające — uległy aktywacji, co sądowe cechy trwającej degeneracji siatkówki.
Stres wewnątrz komórki i niebezpieczny przełącznik
Brak Axin1 nie tylko zmieniał strukturę; nasilał również stres biochemiczny. W siatkówkach myszy pozbawionych Axin1 markery stresu ER, takie jak białko CHOP, były silnie podwyższone w warstwach fotoreceptorów. W hodowanych komórkach pochodzenia czopkowego 661W zmniejszenie ekspresji Axin1 sprawiło, że ekspozycja na niebieskie światło i chemiczny induktor stresu ER, tunikamycyna, stały się znacznie bardziej toksyczne, zwiększając ekspresję genów związanych ze stresem ER oraz liczbę komórek przechodzących apoptozę. Badanie powiązało tę wrażliwość z kluczowym enzymem, GSK3β, który staje się bardziej aktywny, gdy poziomy Axin1 spadają. Nadaktywne GSK3β popychało komórki w stronę stresu ER i śmierci. Odwrotnie, stabilizowanie Axin1 za pomocą małocząsteczkowego leku lub bezpośrednie hamowanie GSK3β chlorkiem litu zmniejszało markery stresu, uspokajało aktywność GSK3β i ratowało wiele komórek przed apoptozą.
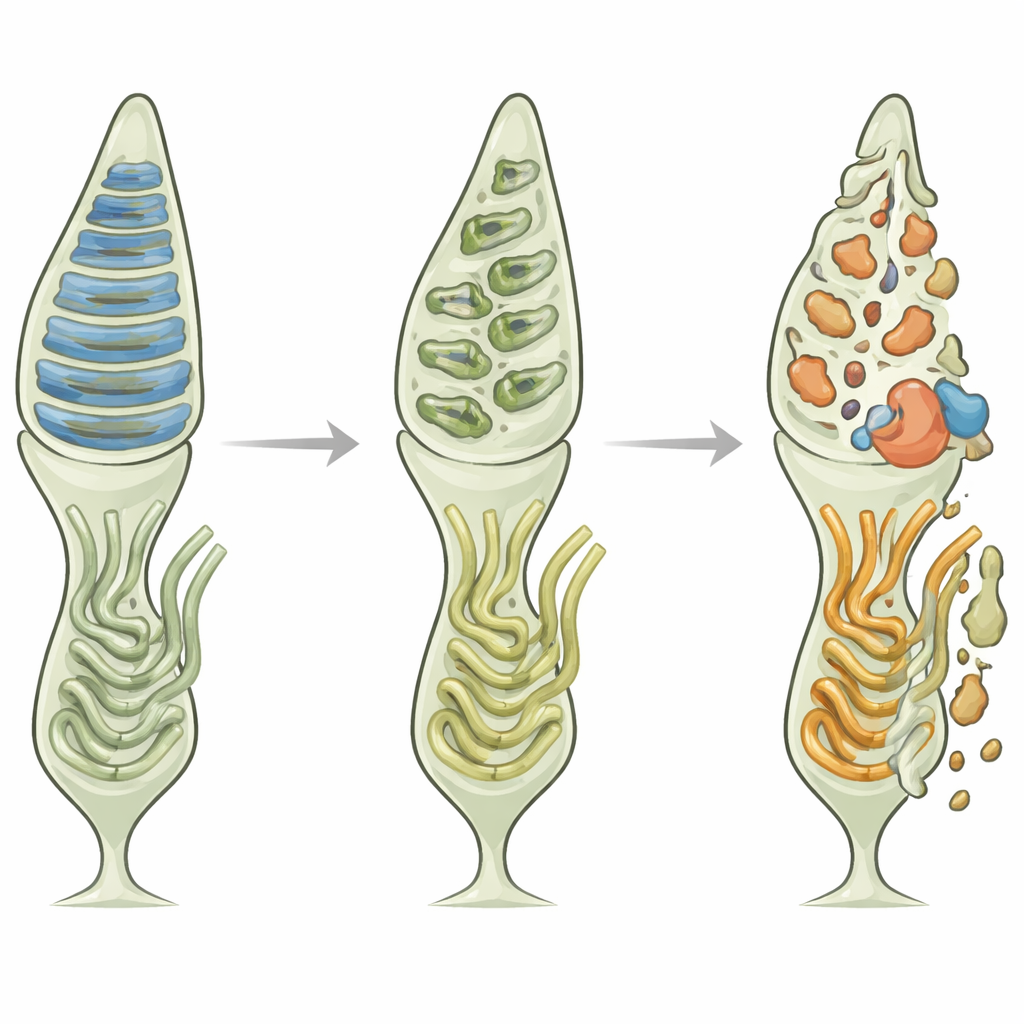
Przekształcanie ochrony w terapię
W sumie wyniki przedstawiają Axin1 jako centralnego strażnika fotoreceptorów czopkowych. Poprzez zakotwiczenie S-opsyny we właściwym miejscu w segmencie zewnętrznym i powstrzymywanie enzymu sprzyjającego stresowi, GSK3β, Axin1 pomaga czopkom radzić sobie z nieustającym obciążeniem wynikającym z jasnego i krótkofalowego światła. Gdy Axin1 jest nieobecny lub niestabilny, S-opsyna ulega złej lokalizacji, ER zostaje zalane problematycznymi białkami, szlaki stresowe zapalają się, a czopki są pchane w kierunku degeneracji. Ponieważ wiele ludzkich chorób prowadzących do ślepoty ostatecznie wiąże się z utratą czopków i śmiercią komórek indukowaną stresem ER, strategie zwiększające lub naśladujące funkcję Axin1 — albo bezpiecznie łagodzące aktywność GSK3β — mogą otworzyć nowe drogi do spowolnienia lub zapobiegania degeneracji siatkówki oraz zachowania naszego widzenia dziennego i barwnego.
Cytowanie: Xu, J., Man, J., Fan, Y. et al. Axin1 stabilizes S-opsin and maintains cone photoreceptor survival by inhibiting GSK3β activity. Cell Death Discov. 12, 109 (2026). https://doi.org/10.1038/s41420-026-02968-5
Słowa kluczowe: degeneracja siatkówki, fotoreceptory czopkowe, stres retikulum endoplazmatycznego, Axin1, GSK3 beta