Clear Sky Science · pl
Sprzężenie między bioenergetyką mitochondriów a SASP determinuje skuteczność senolityków w senescencji indukowanej terapią
Dlaczego eliminacja „zombie” komórek nowotworowych jest tak trudna
Wiele współczesnych leków przeciwnowotworowych nie zabija wszystkich komórek guza bezpośrednio. Zamiast tego część komórek przechodzi w przypominający limbo stan zwany senescencją: przestają się dzielić, ale pozostają przy życiu — niczym „zombie”. Komórki senescentne wywołane terapią mogą początkowo być pomocne, lecz jeśli utrzymują się zbyt długo, mogą napędzać nawrót choroby, oporność i działania niepożądane. Dlatego naukowcy testują senolityki — leki selektywnie zabijające komórki senescentne. Artykuł stawia pozornie proste pytanie: dlaczego niektóre senescentne komórki nowotworowe giną po ekspozycji na senolityki, a inne uporczywie przeżywają?
Elektrownie, które pamiętają swoją przeszłość
W centrum badań znalazły się mitochondria, maleńkie elektrownie wewnątrz komórek. Autorzy sprawdzili, czy sposób, w jaki mitochondria spalają różne paliwa — takie jak cukry, tłuszcze i aminokwasy — wpływa na wrażliwość senescentnych komórek nowotworowych na senolityki celujące w białko przetrwania BCL‑xL. Korzystając z testu wysokoprzepustowego (MitoPlate S‑1), funkcjonalnie „odciskali” aktywność mitochondriów w kilku liniach komórkowych przed i po wywołaniu senescencji różnymi terapiami (leki uszkadzające DNA, inhibitory mitozy, stres oksydacyjny lub inhibitory cyklu komórkowego). Okazało się, że senescencja indukowana terapią nie tworzy jednolitego stanu mitochondrialnego. Każdy lek pozostawiał odrębny „bioenergetyczny odcisk”, zmieniając zakres i intensywność, z jaką mitochondria mogły wykorzystać różne źródła energii. Kluczowe było to, że ta plastyczność była nakładana na wcześniejszą konfigurację: pierwotna budowa mitochondriów komórek rodzicielskich ustalała górną granicę — „sufit” — jak duża może być późniejsza odpowiedź na senolityk.
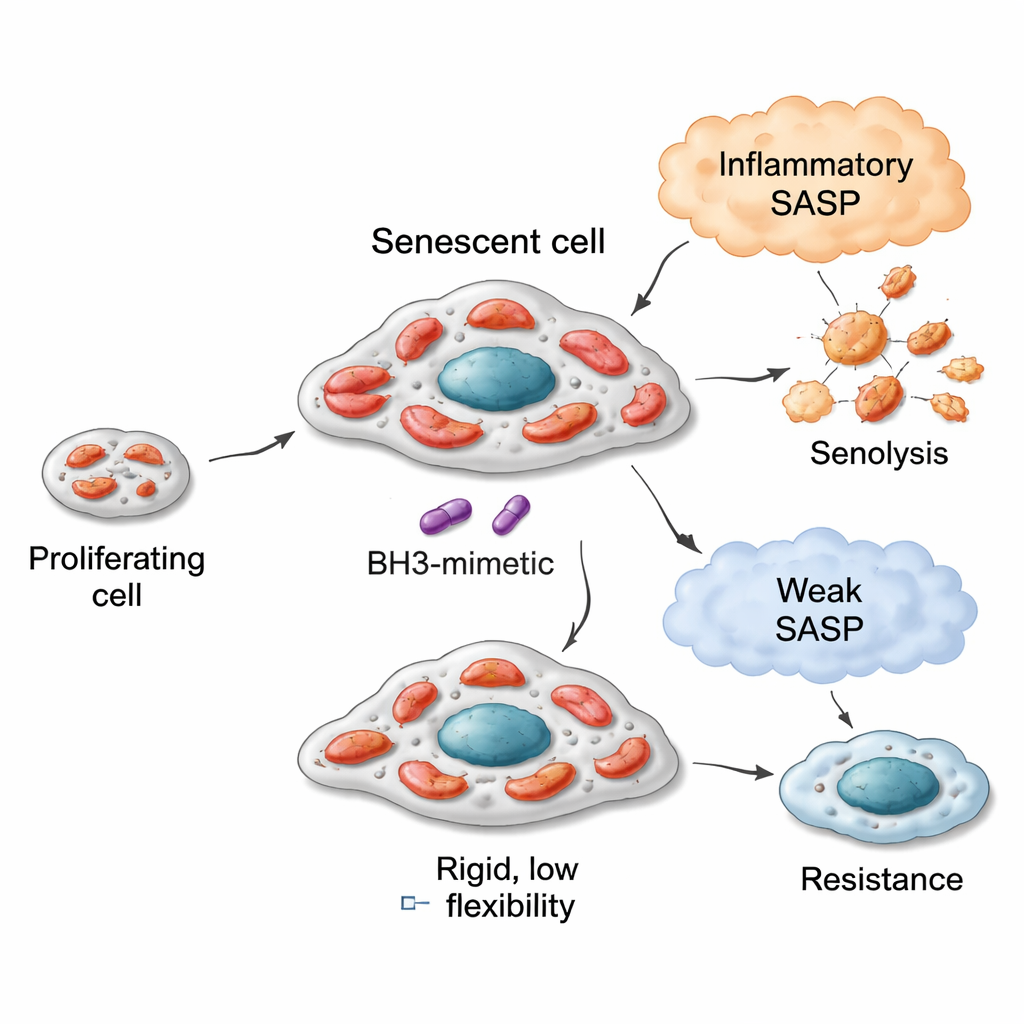
Elastyczne silniki, różne paliwa i wrażliwość na senolityki
W modelach raka płuca, piersi i jelita komórki senescentne z bardziej elastycznymi mitochondriami — zdolnymi do utleniania szerszego wachlarza paliw — wykazywały większą wrażliwość na senolityki celujące w BCL‑xL, takie jak navitoclax (ABT‑263) i A1331852. Na przykład w komórkach raka płuca wywołanych do senescencji przez bleomycyn mitochondria intensywnie wykorzystywały wiele substratów, szczególnie powiązanych z rozkładem kwasów tłuszczowych i niektórymi ścieżkami aminokwasowymi. Te komórki były wysoce wrażliwe na senolityki. Natomiast komórki wprowadzone w senescencję przez inhibitor CDK4/6 (palbociclib) miały węższe spektrum metaboliczne i słabo reagowały na te same środki. Związek ten miał jednak swoje ograniczenia: komórki raka piersi także mogły stać się metabolicznie elastyczne po senescencji, lecz ponieważ ich wyjściowe mitochondria były mniej „zaprzyjaźnione” z apoptozą, ich maksymalna odpowiedź na senolityk była umiarkowana. Komórki raka jelita z defektywnym mechanizmem apoptotycznym pozostawały oporne niezależnie od zmian metabolicznych. Jedna miara — jak dobrze komórki utleniały paliwo sukcynian na poziomie wyjściowym — okazała się prostym wskaźnikiem tej dziedziczonej zdolności mitochondrialnej.
Kiedy metabolizm rozmawia z zapaleniem
Komórki senescentne słyną z SASP, koktajlu wydzielanych czynników zapalnych i wzrostowych wpływających na okoliczne tkanki. Zespół zbadał, jak metabolizm mitochondrialny łączy się z tym zachowaniem sekrecyjnym, używając komórek z wbudowanym raportem dla miR‑146a, mikroRNA włączanego przez główny regulator zapalny NF‑κB. Stwierdzili, że chociaż ogólne profile SASP były w dużej mierze determinowane przez typ komórki, tylko niektóre stany senescentne aktywowały oś NF‑κB/miR‑146a. Były to te same stany, które dobrze odpowiadały na senolityki celujące w BCL‑xL. Co ważne, te „SASP‑pozytywne o zapalnym charakterze” komórki senescentne także wykazywały zwiększone wykorzystanie utleniania kwasów tłuszczowych oraz wzrost ekspresji genów przekazujących długołańcuchowe kwasy tłuszczowe do mitochondriów. Zablokowanie wejścia kwasów tłuszczowych lekiem etomoksirem osłabiło aktywację miR‑146a, nie odwracając jednak całkowicie senescencji, co sugeruje, że wybór paliwa mitochondrialnego pomaga „zezwolić” na zapalny, sprzyjający senolitykom SASP.
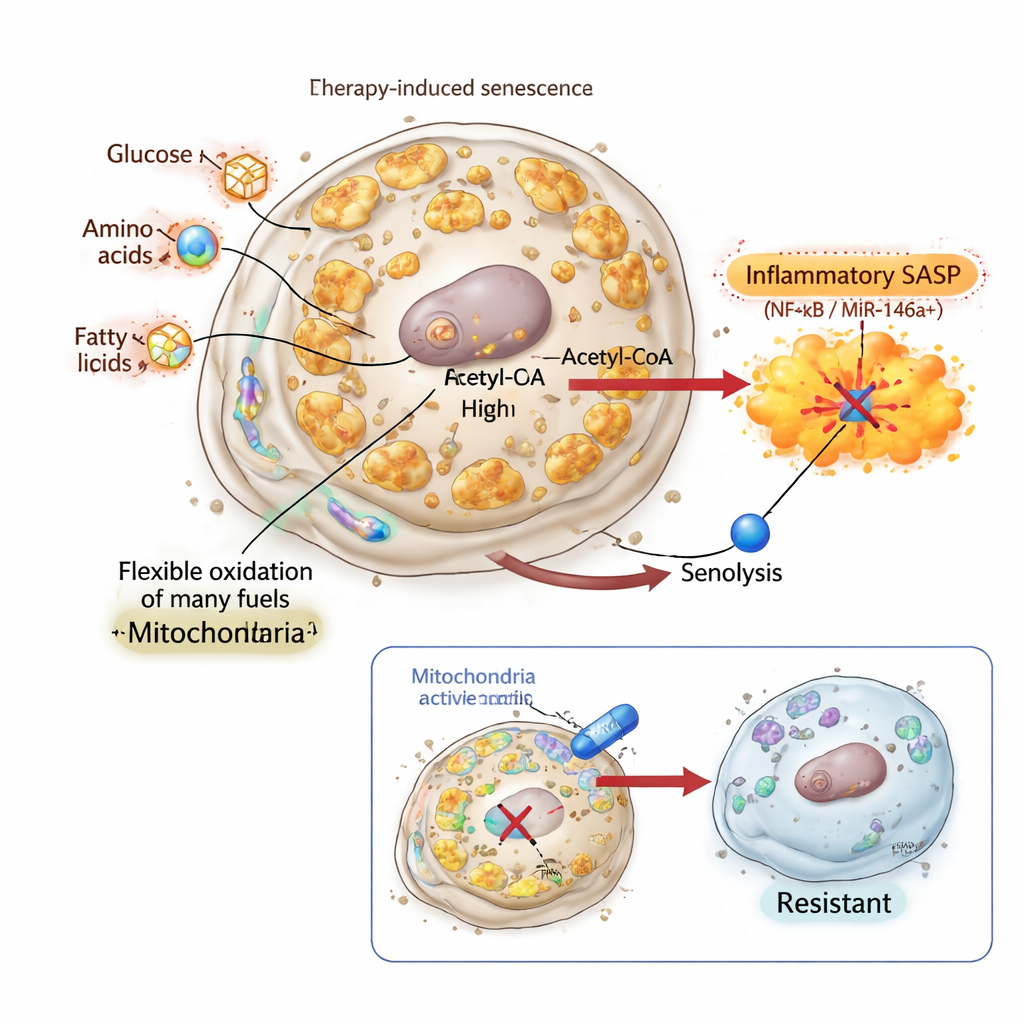
Wygaszanie sygnału i tworzenie nieusuwalnych komórek senescentnych
Aby sprawdzić, czy zapalny SASP jest rzeczywiście niezbędny do zabijania przez senolityki, badacze zastosowali inflachromen — związek wiążący białka chromatyny HMGB1 i HMGB2 i blokujący ich rolę w aktywacji genów SASP. W komórkach raka płuca i piersi inflachromen wywołał kanoniczny fenotyp senescentny: komórki stały się duże, przestały się dzielić i nagromadziły markery senescencji. Ich masa mitochondrialna i aktywność bioenergetyczna znacznie wzrosły, a wykorzystanie paliw uległo ewidentnej reorganizacji. Mimo to ich SASP był stłumiony, a reporter miR‑146a pozostał w dużej mierze nieaktywny. Co uderzające, te senescentne komórki pozbawione SASP były całkowicie odporne na senolityki celujące w BCL‑xL, pomimo aktywnych bioenergetycznie, przereprogramowanych mitochondriów i obniżonej ekspresji klasycznego genu antyapoptotycznego BCL2. Pokazało to, że same zmiany mitochondrialne nie wystarczają; bez mitochondriów napędzanego wyjścia zapalnego „drugi cios” senolityczny nie działa.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla czytelnika niebędącego specjalistą wniosek z badania jest taki, że eliminacja terapeutycznie wywołanych „zombie” komórek nowotworowych rządzi się złożonym, warstwowym obwodem. Po pierwsze, pierwotny stan i okablowanie mitochondriów komórki nowotworowej ustalają, jak daleko senolityki kiedykolwiek mogą zajść. Po drugie, konkretny zabieg wywołujący senescencję może przesunąć metabolizm mitochondrialny w kierunku większej lub mniejszej elastyczności, zbliżając lub oddalając komórki od progu apoptozy. Po trzecie — i najważniejsze — senolityki działają dobrze tylko wtedy, gdy przereprogramowanie metaboliczne skutecznie uruchamia zapalny program SASP, który oddziałuje z jądrem komórkowym. Bez tej zapalnej wymiany zdań komórki senescentne mogą stać się martwym końcem odpornym na leki. W praktyce sugeruje to, że przyszłe terapie warto optymalizować przez funkcjonalne badanie zarówno elastyczności mitochondriów, jak i zapalności SASP w guzach, a następnie dobierać kombinacje leków wywołujących senescencję i senolityków tak, by „zombie” komórki nie tylko były zamrożone, lecz także przygotowane do usunięcia.
Cytowanie: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Słowa kluczowe: senescencja komórkowa, mitochondria, senolityki, metabolizm nowotworowy, zapalny SASP