Clear Sky Science · pl
Ustęp SREBP1 wywołuje ferroptozę poprzez tłumienie osi Nrf2-XCT/GPX4 w raku jajnika
Obrócenie fabryki tłuszczu nowotworu przeciwko niemu samemu
Rak jajnika często wykrywany jest późno i bywa trudny do leczenia. W tym badaniu zbadano zaskakującą słabość tych guzów: ich zależność od syntezy tłuszczów. Naukowcy wykazali, że wyłączenie kluczowego przełącznika „fabryki tłuszczu” w komórkach nowotworowych może jednocześnie spowolnić ich wzrost i uruchomić specyficzny rodzaj śmierci komórkowej, a także ułatwić układowi odpornościowemu atak guza.
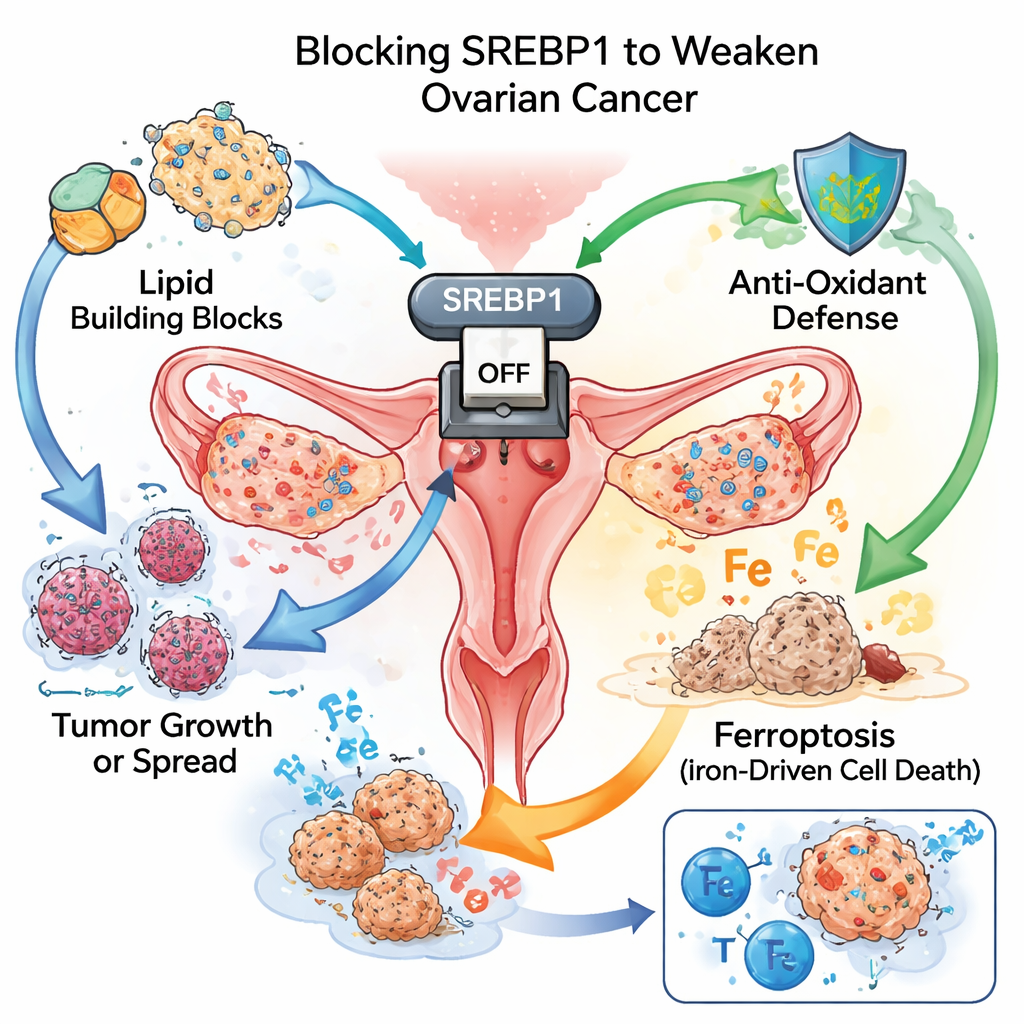
Główny przełącznik paliwa guza
Podobnie jak szybko rosnące chwasty, komórki nowotworowe potrzebują ogromnych ilości materiałów budulcowych i energii. Jednym ze sposobów zaspokojenia tych potrzeb jest przestawienie sposobu, w jaki wytwarzają i wykorzystują tłuszcze. Zespół skupił się na SREBP1, białku pełniącym rolę głównego przełącznika produkcji tłuszczów. W próbkach tkankowych od ponad stu pacjentów guzy jajnika wykazywały znacznie wyższe poziomy SREBP1 niż otaczająca normalna tkanka. Kobiety, których guzy miały silniejsze barwienie SREBP1, miały zwykle bardziej agresywną chorobę i krótsze przeżycie, co wskazuje na to białko zarówno jako czynnik napędzający progresję, jak i sygnał ostrzegawczy złego rokowania.
Spowolnienie wzrostu i rozprzestrzeniania przez odcięcie tłuszczu
W liniach komórkowych raka jajnika hodowanych w laboratorium obniżenie poziomu SREBP1 wyraźnie zmniejszyło zdolność komórek do mnożenia się i tworzenia kolonii. Komórki zablokowały się na określonych etapach cyklu komórkowego, co uniemożliwiało im efektywne dzielenie. Badacze zaobserwowali też mniej oznak ruchu i inwazji: testy zadrapania (scratch) i Transwell wykazały, że komórki z mniejszą ilością SREBP1 słabiej migrowały, a kluczowe markery procesu EMT przesunęły się z powrotem w kierunku bardziej „normalnego” stanu. Równocześnie spadły poziomy trójglicerydów i cholesterolu, a barwienia wykazały mniej kropli lipidowych wewnątrz komórek, potwierdzając, że wewnętrzny mechanizm syntezy tłuszczów został przytłumiony.
Wywołanie śmierci komórki napędzanej żelazem
Najbardziej uderzającym efektem blokady SREBP1 była aktywacja ferroptozy, niedawno rozpoznanego rodzaju śmierci komórkowej napędzanej przez żelazo oraz peroksydację błon komórkowych. Tylko bloker ferroptozy, a nie inhibitory innych szlaków śmierci, mógł uratować komórki z wyciszonym SREBP1, co wskazuje na ferroptozę jako główną przyczynę ich obumierania. Testy chemiczne wykazały więcej produktów uszkodzenia powstałych w wyniku utleniania tłuszczów, mniej antyoksydacyjnej glutationu i wyższe poziomy reaktywnych cząsteczek lipidowych. Dwa białka, które normalnie chronią komórki przed ferroptozą — xCT i GPX4 — były silnie zredukowane po wyciszeniu SREBP1, co pozbawiło komórki istotnej ochrony przed tym destrukcyjnym procesem.
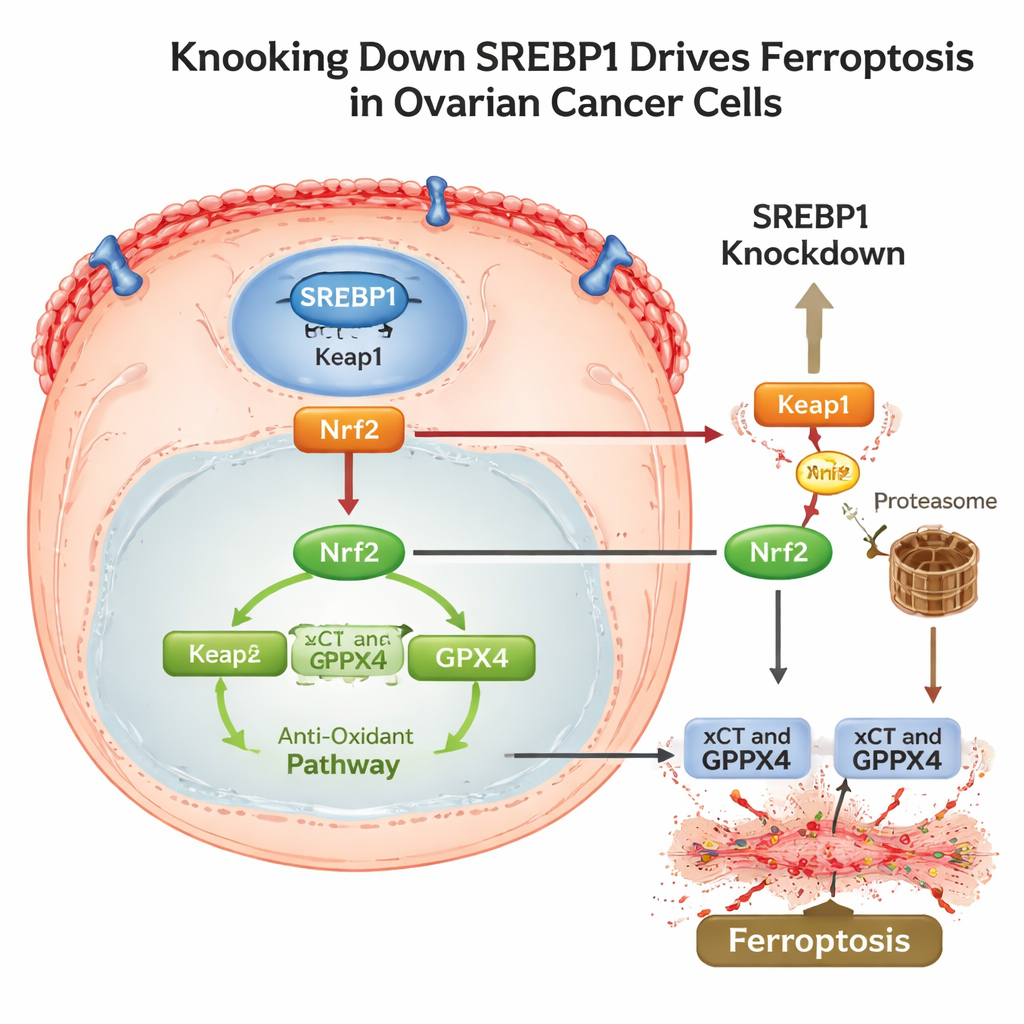
Rozbrajanie antyoksydacyjnej tarczy komórki i sztuczek ucieczki
Aby zrozumieć, jak SREBP1 łączy się z tym programem śmierci, naukowcy prześledzili szlak przez kolejne białko odpowiedzi na stres, Nrf2. W warunkach normalnych Nrf2 pomaga komórkom przetrwać, włączając geny antyoksydacyjne, w tym xCT i GPX4. Badanie wykazało, że obniżenie SREBP1 zwiększyło poziomy Keap1, białka oznaczającego Nrf2 do eliminacji, co prowadziło do zwiększonego rozkładu Nrf2 i mniejszej jego obecności w jądrze. W miarę spadku poziomów Nrf2 słabły jego obronne mechanizmy i następowała ferroptoza. Co ważne, guzy bogate w SREBP1 wykazywały też wyższe poziomy PD-L1, białka powierzchniowego pomagającego komórkom nowotworowym ukryć się przed atakującymi limfocytami T. Gdy SREBP1 został wyciszony w guzach mysz, nowotwory rosły wolniej, wykazywały więcej oznak uszkodzeń lipidów, mniej Nrf2 i GPX4 oraz niższe PD-L1, równocześnie z nasileniem aktywności immunologicznej.
Dlaczego to ma znaczenie dla przyszłych terapii
Mówiąc prosto, guzy jajnika wydają się używać SREBP1 jako narzędzia o podwójnym zastosowaniu: napędza ono ich wzrost przez zwiększanie produkcji lipidów, a jednocześnie uzbraja je w antyoksydacyjną tarczę i mechanizmy kamuflażu immunologicznego. Praca ta pokazuje, że wyłączenie SREBP1 może pozbawić guz lipidów, zdjąć jego ochronę przed uszkodzeniami napędzanymi żelazem i zmniejszyć zdolność unikania ataku immunologicznego. To czyni SREBP1 atrakcyjnym celem dla nowych leków i sugeruje, że łączenie inhibitorów SREBP1 z terapiami wywołującymi ferroptozę lub uwalniającymi układ odpornościowy może zapewnić pacjentom skuteczniejszą i trwalszą kontrolę choroby.
Cytowanie: Nie, R., Zhou, H., Chen, L. et al. SREBP1 knockdown triggers ferroptosis by suppressing the Nrf2-XCT/GPX4 axis in ovarian cancer. Cell Death Discov. 12, 101 (2026). https://doi.org/10.1038/s41420-026-02964-9
Słowa kluczowe: rak jajnika, metabolizm lipidów, ferroptoza, SREBP1, odporność przeciwnowotworowa