Clear Sky Science · pl
PDHA1 zwiększa odporność na ferroptoza w komórkach raka gruczołu krokowego odpornych na anoikę poprzez zwiększenie ekspresji AIFM2
Dlaczego niektóre komórki raka prostaty odmawiają śmierci
Kiedy komórki nowotworowe odrywają się od guza i trafiają do krwiobiegu, większość z nich powinna obumrzeć, zanim dotrze do nowego narządu. Mniejszość jednak przetrwa, przemieści się i zasiać przerzuty, które często są śmiertelne. W tym badaniu stawiono kluczowe pytanie: co pozwala pewnym komórkom raka prostaty opierać się formie śmierci komórkowej, która zwykle następuje po utracie kontaktu z tkanką macierzystą? Odkrywając ukryty obwód przetrwania w tych komórkach, badanie wskazuje nowe sposoby blokowania przerzutów u ich źródła.
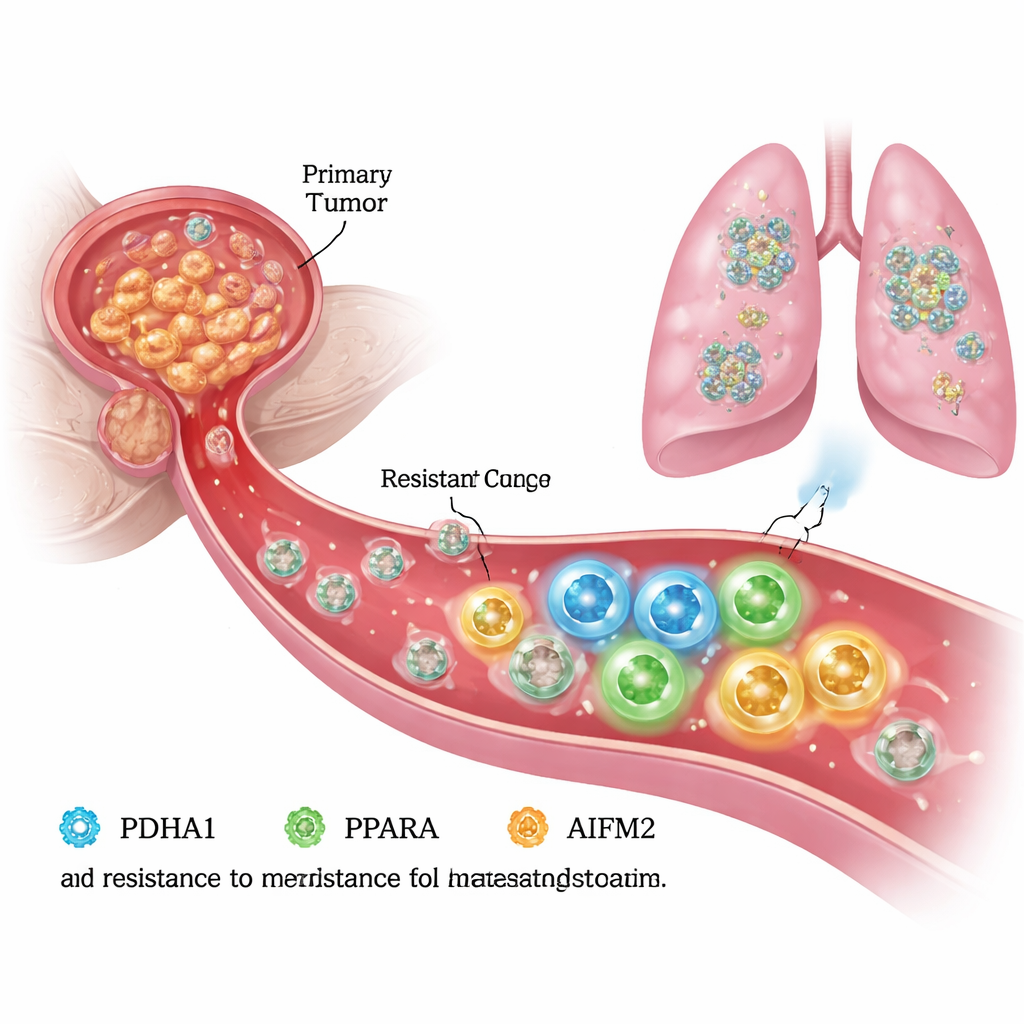
Ucieczka przed śmiercią w krwiobiegu
Aby się szerzyć, komórki raka prostaty muszą przetrwać życie bez wsparcia tkanki otaczającej, zwanej macierzą zewnątrzkomórkową. W tych „odłączonych” warunkach zdrowe komórki przechodzą zaprogramowaną śmierć zwaną anoiką, a wiele komórek nowotworowych jest także podatnych na powiązany proces śmierci napędzany żelazem, zwany ferroptozą. Autorzy wyhodowali w laboratorium komórki raka prostaty odporne na anoikę i porównali je z ich pierwotnymi „rodzicielskimi” komórkami. Stwierdzili, że komórki odporne nie tylko migrowały i inwazyjnie naciekały bardziej agresywnie, ale też lepiej przeżywały w warunkach odłączenia, co sugeruje, że przestawiły swoje wewnętrzne mechanizmy, by unikać ferroptozy i dalej się rozwijać.
Metaboliczny przełącznik z drugą rolą
Badając temat głębiej, zespół skupił się na enzymie metabolicznym o nazwie PDHA1, znanym głównie z udziału w przekształcaniu pirogronianu pochodzącego z cukrów w acetylo-CoA w mitochondriach, zasilającym produkcję energii. W komórkach odpornych na anoikę poziomy i aktywność PDHA1 były znacznie wyższe, a próbki od pacjentów wykazywały więcej PDHA1 w guzach pierwotnych u mężczyzn, u których rak prostaty rozsiał się do węzłów chłonnych lub odległych miejsc. Gdy badacze zmniejszyli poziom PDHA1, komórki odporne straciły dużą część swojej zdolności do przemieszczania się, inwazji i przeżycia. Co zaskakujące, znaczna część PDHA1 w tych komórkach nie była już ograniczona do mitochondriów; przeniknęła do jądra komórkowego, gdzie DNA jest upakowany z histonami, które można chemicznie modyfikować, by włączać lub wyłączać geny.
Przepisywanie aktywności genów, by zablokować ferroptozę
W jądrze PDHA1 wydawał się zasilać lokalną produkcję acetylo-CoA, kluczowego składnika dla acetylacji histonów. Autorzy pokazali, że nuklearny PDHA1 zwiększał specyficzne oznaczenie, acetylację H3K9, w obszarze kontrolnym genu PPARA. Ta zmiana działała jak poluzowanie „bębnów” chromatyny, ułatwiając włączenie PPARA. PPARA z kolei pełniła rolę głównego przełącznika, który zwiększał produkcję innego białka, AIFM2, wiążąc się z jego promotorem i podnosząc transkrypcję. Zamiast bezpośrednio regulować gen AIFM2, PDHA1 działał więc przez PPARA, ustanawiając wieloetapową ścieżkę od zmienionego metabolizmu do zmienionej regulacji genów.
Budowanie tarczy przeciwko uszkodzeniom spowodowanym żelazem
AIFM2 jest znany jako wewnętrzny hamulec ferroptozy: pomaga chronić lipidy w błonach komórkowych przed niszczącą oksydacją. W odpornych komórkach raka prostaty zwiększenie PDHA1 podwyższało poziomy AIFM2, podczas gdy zahamowanie PDHA1 je obniżało. Testy funkcjonalne pokazały, że zmniejszenie PDHA1 nasilało cechy charakterystyczne ferroptozy — więcej reaktywnych form tlenu, więcej uszkodzeń lipidów, niższy potencjał błony mitochondrialnej i typowe kurczenie się mitochondriów — zwłaszcza gdy komórki eksponowano na lek wywołujący ferroptozę, erastynę. Nadekspresja AIFM2 odwracała te efekty, ratując przeżywalność komórek na hodowlach i przywracając przerzuty do płuc u myszy, nawet gdy PDHA1 był stłumiony. To potwierdziło, że AIFM2 jest krytycznym efektorem zależnym od PDHA1, odpowiadającym za odporność na ferroptozę.
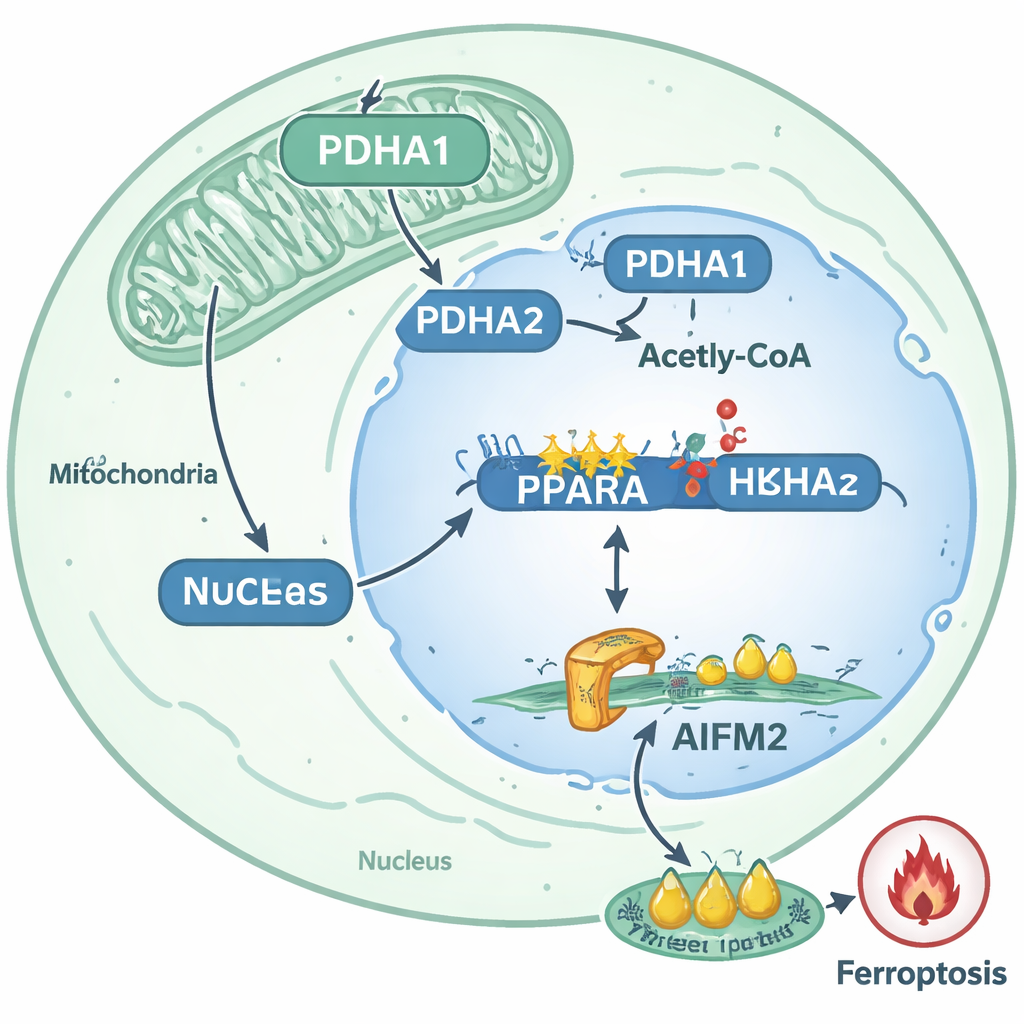
Od obwodu molekularnego do pomysłów na leczenie
Mapując te zdarzenia, badanie przedstawia jasną drogę, dzięki której odłączone komórki raka prostaty stają się trudniejsze do zabicia: PDHA1 przemieszcza się do jądra, zwiększa acetylację histonów przy genie PPARA, podnosi aktywność PPARA, a w konsekwencji podwyższa poziomy AIFM2, blokując ferroptozę. Ta ścieżka jest silnie związana z zachowaniami przerzutowymi w guzach pacjentów i modelach zwierzęcych. Dla czytelników niebędących specjalistami kluczowe wnioski są takie, że niektóre komórki nowotworowe przekształcają normalny enzym metaboliczny w narzędzie epigenetyczne, które przepisuje aktywność genów i buduje biochemiczną tarczę przeciwko potężnej formie śmierci komórkowej. Autorzy sugerują, że leki ukierunkowane na PDHA1, PPARA lub AIFM2 — lub terapie celowo wywołujące ferroptozę — mogłyby w przyszłości zostać połączone, aby pozbawić komórki raka prostaty przerzutów tej przewagi przetrwania i uczynić je znacznie bardziej wrażliwymi podczas ich najbardziej niebezpiecznej podróży: skoku z jednego narządu do drugiego.
Cytowanie: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Słowa kluczowe: przerzuty raka prostaty, ferroptoza, odporność na anoikę, PDHA1, AIFM2