Clear Sky Science · pl
Osteocytarna lipokalina-2 reguluje tworzenie kości lokalnie poprzez żelazo-zależną ferroptozę i hamowanie sygnalizacji Wnt
Gdy komórki kostne cicho kształtują zdrowie całego organizmu
Większość z nas myśli o kościach jak o sztywnej konstrukcji, jednak w rzeczywistości są one żywe — wypełnione komórkami, które nieustannie odbudowują i naprawiają nasz szkielet. To badanie ujawnia, jak jeden niewielki białkowy produkt komórek kostnych, lipokalina-2, może dyskretnie osłabiać kości od środka, zaburzając gospodarkę żelaza i energetykę komórkową. Zrozumienie tego ukrytego mechanizmu może wskazać nowe kierunki terapii osteoporozy i utraty masy kostnej związanej z wiekiem.
Białko-posłaniec o podwójnym życiu
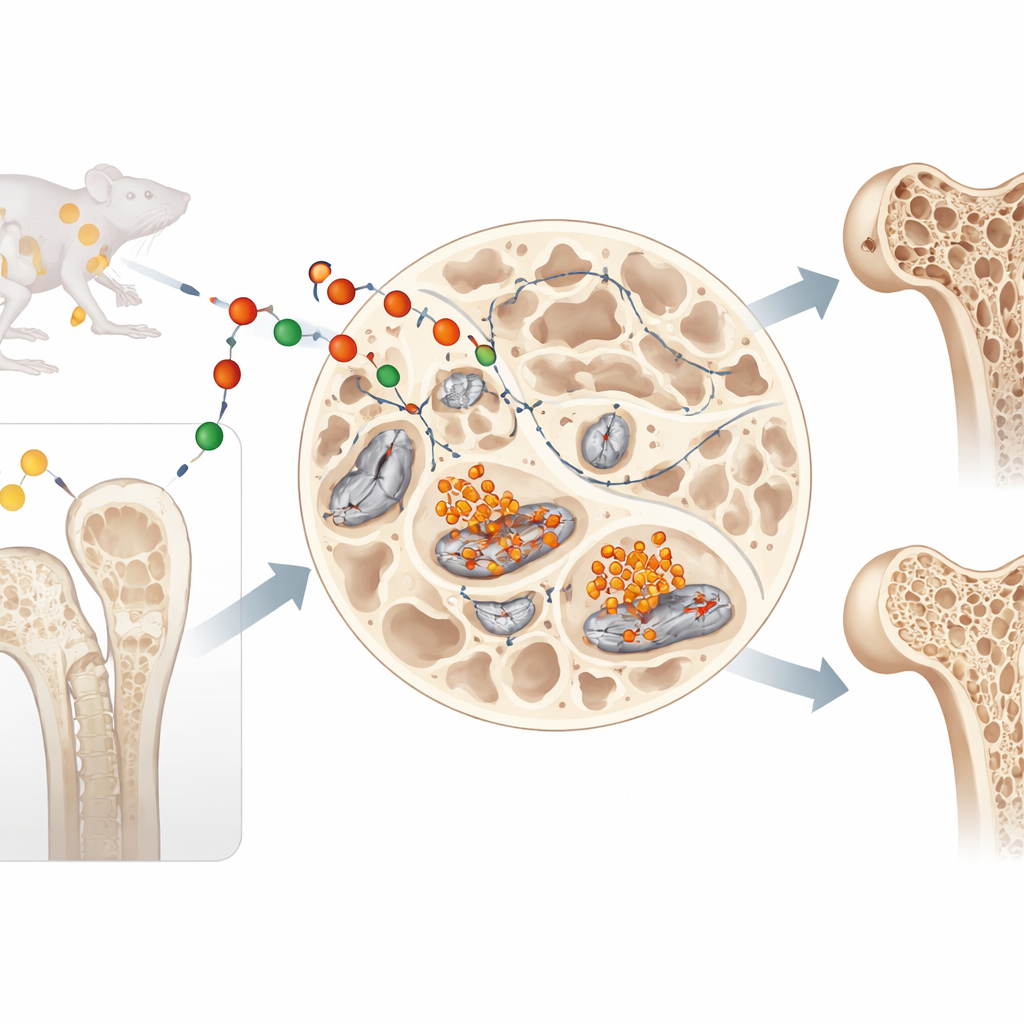
Lipokalina-2 była dotąd znana jako wędrujący hormon krążący we krwi, który pomaga regulować apetyt i masę ciała oraz chroni przed zakażeniami wiążąc żelazo. Autorzy tej pracy postawili jednak inne pytanie: co lipokalina-2 robi tam, gdzie jest wytwarzana — bezpośrednio w kości? Skoncentrowali się na osteocytach, długowiecznych komórkach zatopionych głęboko w tkance kostnej, które odczuwają siły mechaniczne i kierują przebudową kości. Zespół stwierdził, że osteocyty nie tylko nadal produkują lipokalinę-2 w miarę dojrzewania, lecz wręcz zwiększają jej syntezę, co sugeruje istotną lokalną rolę w obrębie szkieletu.
Nadmierne obciążenie żelazem i „rdzewiejący” rodzaj śmierci komórkowej
Ponieważ lipokalina-2 może transportować żelazo, badacze sprawdzili, czy powoduje ono gromadzenie żelaza w osteocytach. W hodowlach komórkowych dodanie lipokaliny-2 spowodowało akumulację żelaza wewnątrz komórek, wzrost szkodliwych reaktywnych form tlenu oraz intensywne uszkodzenie błon komórkowych bogatych w lipidy. To cechy charakterystyczne niedawno rozpoznanego typu śmierci komórkowej — ferroptozy, w której żelazo działa niczym rdza, wywołując destrukcyjne reakcje chemiczne. Zablokowanie żelaza za pomocą środka chelatującego całkowicie zapobiegło uszkodzeniom i śmierci komórek, potwierdzając, że proces jest zależny od żelaza.
Bramkowy receptor i upadek mitochondriów
Aby zrozumieć, jak lipokalina-2 dostarcza ładunek żelaza do osteocytów, zespół zwrócił uwagę na specyficzny receptor powierzchniowy SLC22A17. Gdy zredukowano ten receptor w komórkach podobnych do osteocytów, lipokalina-2 przestała napędzać wejście żelaza, stres oksydacyjny i śmierć ferroptotyczną, nawet przy nadmiarze żelaza. Badanie wykazało również, że lipokalina-2 osłabia „elektrownię” komórkową — mitochondria. Nadmiar lipokaliny-2 powodował utratę prawidłowego potencjału błon mitochondrialnych i zmniejszenie produkcji energii, podczas gdy usunięcie lipokaliny-2 przywracało funkcję mitochondriów. W kościach myszy pozbawionych lipokaliny-2 w osteocytach geny wspierające oddychanie mitochondrialne i kontrolę jakości mitochondriów były aktywowane, co sugeruje lepszą kondycję energetyczną tych komórek.
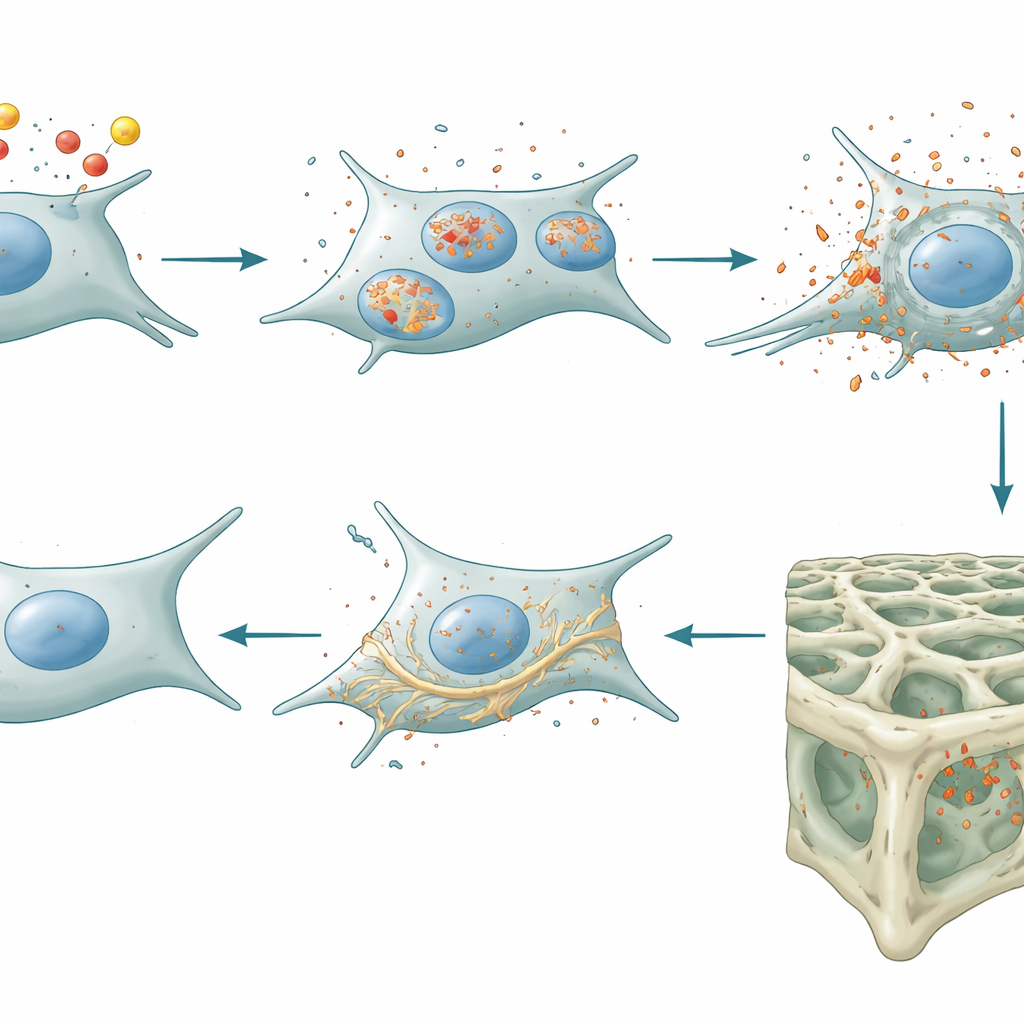
Od stresu komórkowego do słabszej kości — i jak zdjęcie hamulca pomaga
Następnie badacze przyjrzeli się intactnym myszom, u których genetycznie usunięto lipokalinę-2 specyficznie w późnych stadiach komórek tworzących kość oraz w osteocytach. Zwierzęta te gromadziły mniej żelaza w komórkach kostnych i wykazywały silniejsze mechanizmy antyoksydacyjne przeciwdziałające ferroptozie. Co istotne, produkowały też niższe poziomy dwóch kluczowych białek — sklerostyny i DKK1 — które zwykle działają jak hamulce ścieżki Wnt/β-katenina, będącej głównym motorem tworzenia kości. Gdy te hamulce zostały złagodzone, sygnalizacja pobudzająca osteoblasty budujące kość wzrosła. Badania mikrotomografii komputerowej i eksperymenty z znakowaniem kości potwierdziły rezultat: myszy bez osteocytarnej lipokaliny-2 budowały więcej i lepiej połączonej kości gąbczastej (beleczkowej), głównie poprzez zwiększenie tworzenia kości, a nie spowolnienie jej resorpcji. Mimo tych zmian szkieletowych ich masa ciała, kontrola poziomu glukozy we krwi, metabolizm i aktywność pozostały prawidłowe, co pokazuje, że efekt był lokalny dla tkanki kostnej, a nie ogólnym działaniem hormonalnym.
Co to oznacza dla utrzymania mocnych kości
Mówiąc wprost, praca ta pokazuje, że lipokalina-2 wewnątrz komórek kostnych działa jak lokalny przełącznik, który podnosi poziom żelaza, obciąża mitochondria, predysponuje komórki do uszkodzeń ferroptotycznych i tłumi kluczową ścieżkę wzrostu — razem ograniczając tworzenie nowej tkanki kostnej. Gdy ten wewnętrzny hamulec zostaje usunięty, osteocyty są zdrowsze, wysyłają więcej sygnałów sprzyjających budowie, a kość beleczkowa staje się gęstsza i lepiej połączona bez zaburzania ogólnego metabolizmu. Ponieważ poziomy lipokaliny-2 i zaburzenia równowagi żelaza rosną z wiekiem i przy przewlekłym zapaleniu, ukierunkowanie systemu lipokalina-2–receptor może zaoferować nowy sposób ochrony kości przed „rdzewieniem” od wewnątrz.
Cytowanie: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
Słowa kluczowe: zdrowie kości, osteocyty, metabolizm żelaza, ferroptoza, sygnalizacja Wnt