Clear Sky Science · pl
Polimeraza DNA kappa stabilizowana przez Ptbp2 wchodzi w interakcję z MRE11 i sprzyja niestabilności genomowej w białaczce
Jak komórki białaczkowe utrzymują połamane DNA i nadal przeżywają
Nasze DNA jest nieustannie atakowane, a zdrowe komórki zwykle świetnie radzą sobie z wykrywaniem i naprawą uszkodzeń. W białaczce jednak niektóre komórki uczą się żyć z połamanym, niestabilnym DNA — i nawet wykorzystują tę niestabilność jako przewagę przetrwania. W badaniu odkryto molekularne „porozumienie” między białkiem biorącym udział w składaniu RNA (Ptbp2), specjalną enzymatyczną kopiarką DNA (polimerazą DNA kappa, czyli Polk) i czynnikiem wyczuwającym uszkodzenia (MRE11), które pomaga komórkom białaczkowym naprawiać wystarczająco dużo uszkodzeń, by przetrwać, jednocześnie gromadząc genetyczny chaos napędzający postęp nowotworu.
Ukryty pomocnik w komórkach białaczkowych
Naukowcy skupili się na przewlekłej białaczce szpikowej (CML), nowotworze krwi zwykle wywoływanym przez gen fuzyjny BCR::ABL1. Choć nowoczesne leki blokujące BCR::ABL1 działają dobrze we wczesnym stadium choroby, wielu pacjentów w agresywnej fazie „blast crisis” słabo odpowiada na terapię. Wcześniejsze badania wykazały, że Ptbp2 — białko wiążące RNA i wpływające na jego przetwarzanie — jest wzmocnione przez BCR::ABL1 i zachowuje się jak onkogen w CML. Zespół odkrył, że Ptbp2 przyczepia się do końca ogonowego (3′ UTR) mRNA Polka i chroni go przed degradacją. W rezultacie komórki białaczkowe wytwarzają więcej białka Polk, gdy poziomy Ptbp2 są wysokie.
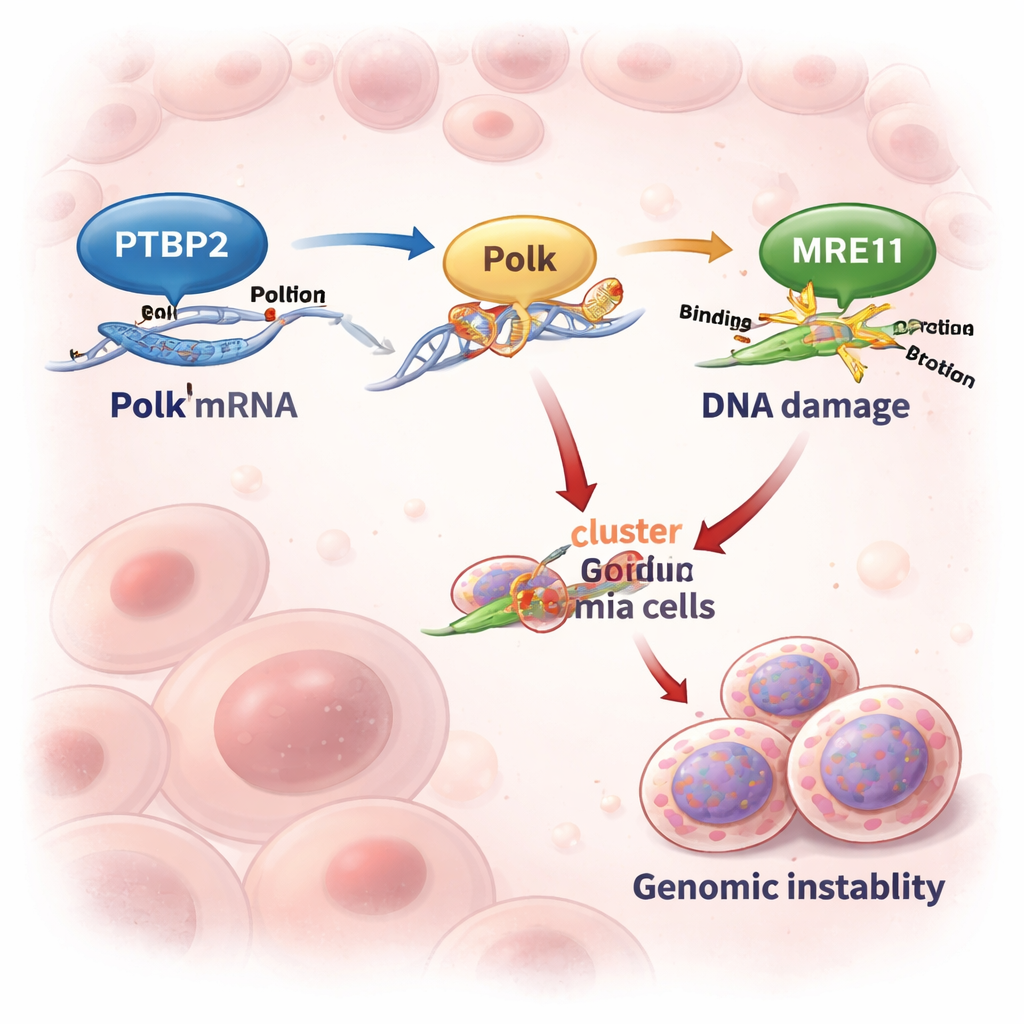
Włączenie podatnej na błędy maszyny kopiującej DNA
Polk to „zapasowa” polimeraza DNA, która potrafi przepisać uszkodzone fragmenty DNA, gdy zwykły aparat replikacyjny zatrzymuje się. Ta zdolność może uratować komórki pod stresem — kosztem jednak zwiększonej liczby błędów, ponieważ Polk jest podatny na wprowadzanie mutacji. W liniach komórkowych i próbkach pacjentów z zaawansowaną CML poziomy Ptbp2 i Polka zmieniały się równolegle. Gdy naukowcy wyłączyli Ptbp2 w komórkach białaczkowych, poziom Polka gwałtownie spadł, a jego RNA rozpadało się prawie dwa razy szybciej. Ponowne wprowadzenie Polka do komórek pozbawionych Ptbp2 przywróciło ich właściwości, co dowodzi, że główną rolą Ptbp2 jest tutaj utrzymanie Polka w dużej ilości i aktywności.
Naprawa uszkodzeń — ale nieperfekcyjna
Aby sprawdzić, jak ten duet wpływa na naprawę DNA, badacze potraktowali komórki hydroksyureą, lekiem hamującym replikację DNA, często stosowanym u pacjentów z CML. Komórki pozbawione Ptbp2 wykazywały znacznie więcej uszkodzeń DNA, widocznych jako długie „ogony komet” i jasne ogniska γH2AX — cechy charakterystyczne połamanych chromosomów. Tak uszkodzone komórki częściej obumierały. W przeciwieństwie do nich komórki z wysokim poziomem Ptbp2 i Polka lepiej tolerowały lek, efektywniej naprawiały uszkodzenia i przeżywały, mimo że naprawa była niedokładna. Nadekspresja Polka w komórkach z wyciętym Ptbp2 znosiła ich wrażliwość, potwierdzając, że partnerstwo Ptbp2–Polk pomaga komórkom białaczkowym przetrwać stres replikacyjny i unikać apoptozy.
Sieć reagowania na uszkodzenia DNA sprzyjająca niestabilności
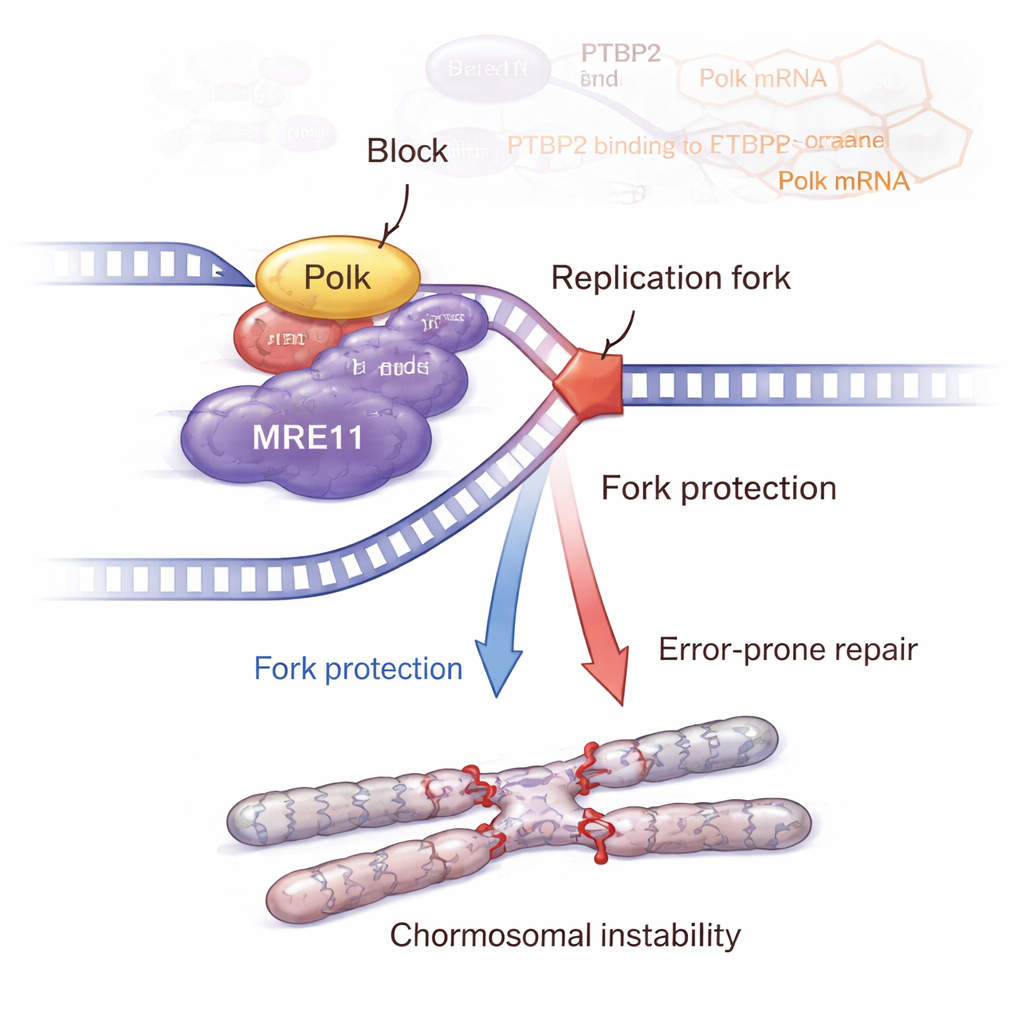
Historia nie kończy się na Polku. Zespół wykazał, że Polk fizycznie wchodzi w interakcję z MRE11, kluczowym składnikiem kompleksu MRN wyczuwającego pęknięcia DNA i aktywującego szlak ATM–CHK2. Gdy usunięto Ptbp2, poziom Polka spadł, poziomy i aktywność MRE11 zmniejszyły się, a sygnalizacja ATM–CHK2 osłabła. Przywrócenie Polka odtworzyło MRE11 i jego aktywację. Szczegółowe eksperymenty na włóknach DNA ujawniły, że Ptbp2 i Polk chronią zatrzymane widły replikacyjne przed cofnięciem, w dużej mierze dzięki MRE11. Zablokowanie MRE11 lekiem osłabiło tę ochronę wideł i zwiększyło uszkodzenia DNA. Paradoksalnie, komórki z aktywnym szlakiem Ptbp2–Polk–MRE11 gromadziły więcej nieprawidłowości chromosomalnych, takich jak wymiany chromatyd sióstr, pęknięcia, luki, wrzeciona z wieloma biegunami i olbrzymie komórki wielojądrowe — klasyczne znaki niestabilności genomowej, które mogą napędzać bardziej agresywny nowotwór.
Od myszy do potencjalnych nowych terapii
W modelach mysich komórki białaczkowe z niezmienionym Ptbp2 tworzyły większe, bardziej nieprawidłowe guzy niż komórki pozbawione Ptbp2. Tkanki z tych myszy wykazywały wyższe poziomy Ptbp2, Polka, markera proliferacji Ki-67 oraz zniekształcone struktury podziału komórkowego. W oddzielnym modelu mysim przypominającym CML napędzanym przez BCR::ABL1, dodatkowy Ptbp2 zwiększał poziom Polka oraz liczbę nietypowo dzielących się komórek i inwazyjnych skupisk białaczki w śledzionie i wątrobie, co wskazuje na szybszy postęp choroby. Razem wyniki te sugerują, że oś Ptbp2–Polk–MRE11–ATM–CHK2 pozwala komórkom białaczkowym przetrwać silny stres DNA, jednocześnie stopniowo gromadząc szkodliwe mutacje.
Dlaczego to ma znaczenie dla pacjentów
Dla laika kluczowy wniosek jest taki, że niektóre komórki białaczkowe wymykają się kontroli, stąpając po linie: naprawiają DNA wystarczająco, by przeżyć, ale na tyle niedokładnie, by pojawiać się mutacje. Ptbp2 stabilizuje Polka, który następnie współdziała z MRE11, by chronić zestresowane DNA i podtrzymywać sygnalizację uszkodzeń — ale ta naprawa jest niedoskonała i sprzyja chaosowi genetycznemu. Ponieważ zaawansowana CML i inne nowotwory wydają się polegać na tej kruchej równowadze, celowanie w Ptbp2 lub jego kontrolę nad Polkiem mogłoby przechylić bilans na niekorzyść komórek i skierować je na drogę samodestrukcji, oferując obiecujący nowy kierunek terapii, zwłaszcza w trudnym do leczenia stadium blast crisis.
Cytowanie: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Słowa kluczowe: przewlekła białaczka szpikowa, niestabilność genomu, naprawa DNA, polimeraza DNA kappa, PTBP2