Clear Sky Science · pl
Mitofagia w raku trzustki: wglądy mechanistyczne i implikacje dla nowych strategii terapeutycznych
Dlaczego elektrownie naszych komórek mają znaczenie w raku trzustki
Gruczolakorak przewodowy trzustki jest jednym z najbardziej śmiertelnych nowotworów, między innymi dlatego, że guzy szybko uczą się opierać niemal wszystkim terapiom stosowanym przez lekarzy. Niniejszy przegląd analizuje zaskakujący element tej oporności: mitofagię, wbudowany w komórkę system rozpoznawania i recyklingu zużytych mitochondriów — małych „elektrowni”, które wytwarzają energię. Zrozumienie, jak rak trzustki przejmuje ten proces porządkowania, może otworzyć nowe drogi do skuteczniejszych, trwalszych terapii.
Komórkowe ekipy porządkowe i sztuczki przeżyciowe raka
Mitochondria robią znacznie więcej niż tylko generowanie energii; pomagają regulować metabolizm, śmierć komórkową oraz neutralizację szkodliwych cząsteczek zwanych reaktywnymi formami tlenu. Gdy mitochondria są uszkodzone lub ich nadmiar, komórki wykorzystują mitofagię do oznaczania i usuwania ich. Dzieje się to dwiema głównymi drogami. Pierwsza, znana jako szlak PINK1/Parkin, opiera się na sensorze uszkodzeń (PINK1) i enzymie znakującym (Parkin), które oznaczają wadliwe mitochondria do zniszczenia. Druga wykorzystuje białkowe receptory, takie jak BNIP3, NIX i FUNDC1, umieszczone na powierzchni mitochondriów, które bezpośrednio łączą je z komórkowymi „workami” utylizacyjnymi, zwanymi autofagosomami, bez tej samej etykietującej fazy. Te szlaki często współdziałają, dając komórkom elastyczne sposoby dostosowania zapasów mitochondriów do stresu, takiego jak niedotlenienie czy ekspozycja na leki. 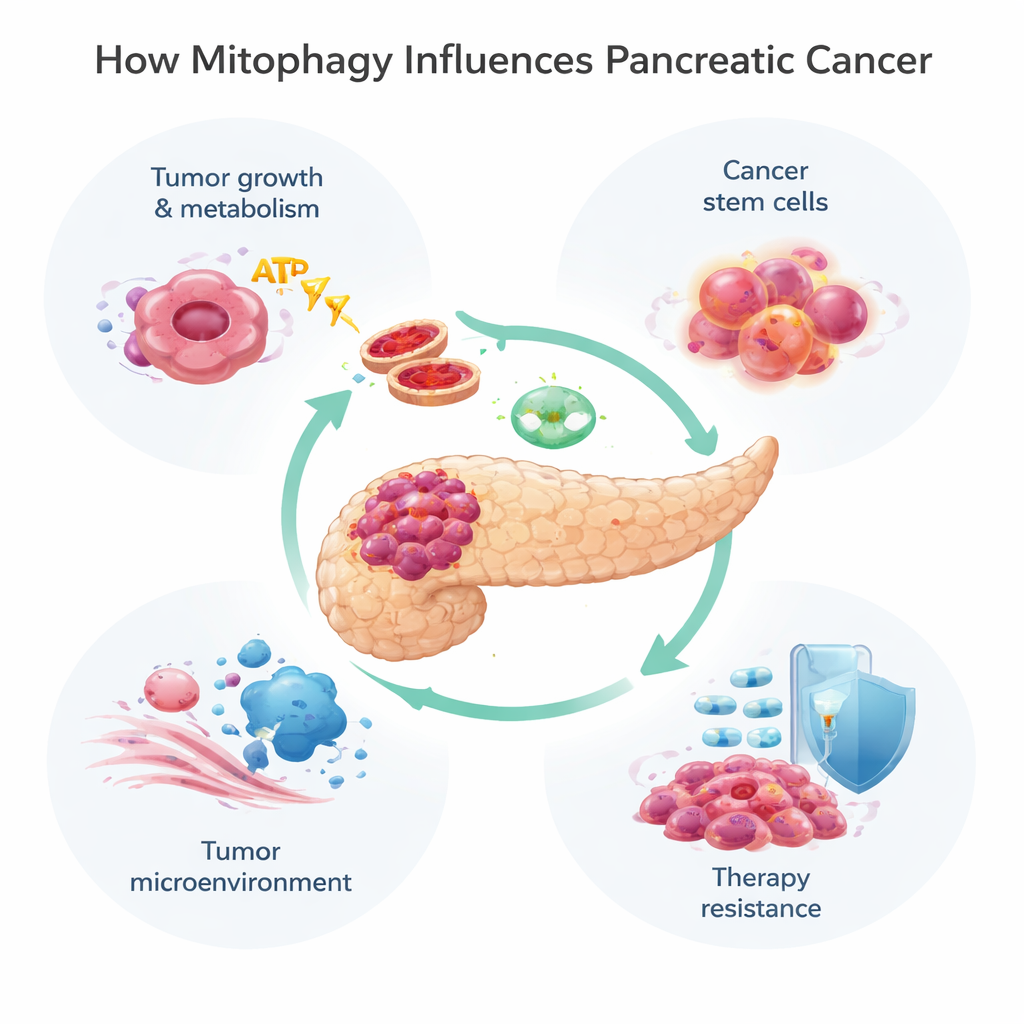
Jak guzy trzustki przekształcają swoje wykorzystanie energii
Guzy trzustki żyją w surowym otoczeniu: słabo unaczynione i natlenowane oraz otoczone gęstą tkanką bliznowatą. Aby przetrwać, komórki nowotworowe przełączają swoje systemy energetyczne, często oddech mitochondrialny na bazie tlenu na bardziej prymitywny proces spalania cukru znany jako glikoliza. Mitofagia pomaga dopracować to przełączenie. We wczesnym rozwoju guza utrata PINK1 lub Parkin przyspiesza rozwój nowotworu przez umożliwienie gromadzenia żelaza, nadmiaru reaktywnych form tlenu i przesunięcia w kierunku glikolizy. Równocześnie inne białko mitofagii, NIX, może pomagać usuwać nadal funkcjonalne mitochondria, skłaniając komórki jeszcze bardziej ku metabolizmowi glikolitycznemu i szybszemu wzrostowi. Natomiast BNIP3 wykazuje bardziej złożony obraz: pojawia się we wczesnych etapach, później bywa wyciszany w wielu zaawansowanych guzach, a jego przywrócenie może spowalniać wzrost komórek nowotworowych, co sugeruje, że niektóre drogi mitofagii hamują raka, podczas gdy inne go napędzają.
Komórki macierzyste raka i mikrośrodowisko guza
Nie wszystkie komórki nowotworowe są równe. Niewielka podgrupa, często nazywana komórkami macierzystymi nowotworu, potrafi samoodnawiać się, zasiewać nowe guzy i szczególnie dobrze znosić chemioterapię. W raku trzustki te komórki polegają na mitofagii, by pozostać metabolicznie elastycznymi. Białko modyfikujące o nazwie ISG15 wspiera ten proces i pomaga utrzymać cechy przypominające komórki macierzyste, łącząc mitofagię bezpośrednio z nawrotem choroby i niepowodzeniem terapii. Poza samymi komórkami nowotworowymi mitofagia kształtuje także mikrośrodowisko guza — mieszaninę komórek wspierających, komórek układu odpornościowego i tkanki łącznej wokół guza. Fibroblasty związane z nowotworem na przykład mogą zostać skierowane w stronę „odwrotnego efektu Warburga”, w którym nasilają własną mitofagię i glikolizę, a następnie dostarczają guzowi bogate w energię produkty uboczne. Mitofagia wpływa także na to, jak komórki odpornościowe rozpoznają i atakują nowotwór, poprzez modyfikację ekspresji znaczników immunologicznych, takich jak MHC‑I, oraz hamulców, jak PD‑L1, których guzy używają do ukrycia się.
Dlaczego blokowanie lub wzmacnianie porządków może zmienić odpowiedź na leki
Wiele standardowych i eksperymentalnych terapii raku trzustki, w tym lek chemioterapeutyczny gemcytabina i nowy lek ukierunkowany na powszechną mutację KRAS‑G12D, uszkadza mitochondria. Komórki guza często reagują włączeniem mitofagii, usuwając uszkodzenia i unikając śmierci. Badania pokazują, że mitofagia napędzana przez PINK1 może osłabiać działanie zabójcze chemioterapii i niektórych związków naturalnych, pomagając komórkom przeżyć. Z drugiej strony, w określonych warunkach nadmierne pobudzenie mitofagii — zwłaszcza przez BNIP3 i NIX — może pozbawić komórki zbyt wielu funkcjonujących mitochondriów, doprowadzając je do kryzysu energetycznego i promując śmierć komórkową. Ta dwuznaczna natura oznacza, że mitofagia może albo chronić guzy przed leczeniem, albo, jeśli zostanie odpowiednio pobudzona, uczynić je bardziej podatnymi. 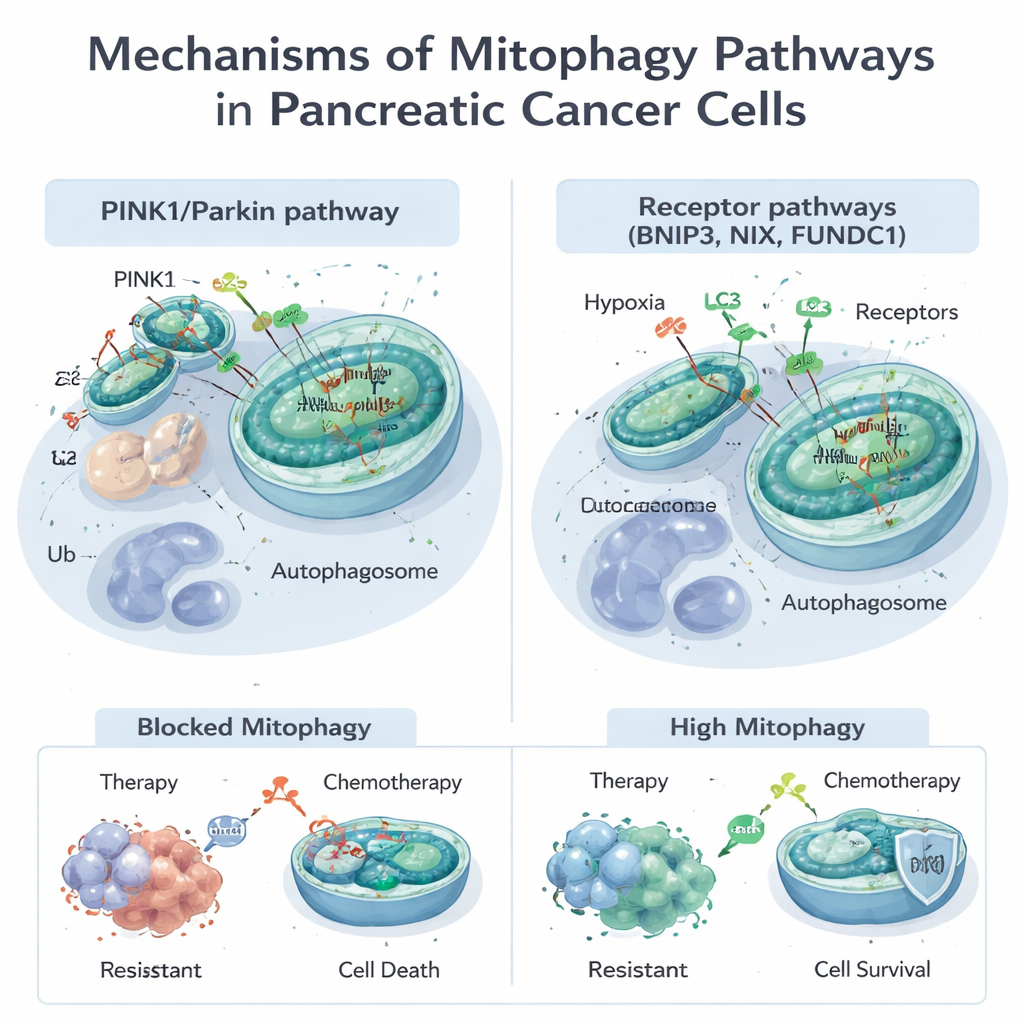
Nowe pomysły terapeutyczne i potrzeba mądrego dopasowania pacjentów
Ponieważ mitofagia leży na skrzyżowaniu metabolizmu, odpowiedzi na stres i śmierci komórkowej, jest atrakcyjnym celem dla terapii skojarzonych. Obecne strategie lekowe działają w większości pośrednio: niektóre związki zakłócają rozszczepianie i łączenie mitochondriów; inne, jak chlorochina i hydroksychlorochina, blokują końcowe etapy procesu recyklingu przez uniemożliwienie fuzji autofagosomów z kwaśnymi komorami degradacyjnymi. Kilka badań klinicznych testuje te leki razem ze standardową chemioterapią w raku trzustki. Jednak dotychczasowe wyniki są mieszane — niektórzy pacjenci odnoszą korzyść, inni nie. Część problemu wynika z tego, że guzy bardzo różnią się pod względem podstawowej aktywności mitofagii i profili metabolicznych: jedne polegają silnie na oddychaniu mitochondrialnym, inne na glikolizie. Autorzy podkreślają, że przyszłe sukcesy zależą od lepszych biomarkerów i sygnatur genowych pozwalających grupować pacjentów według aktywności mitofagii i sposobu wykorzystania energii oraz od rozwoju precyzyjniejszych leków, które selektywnie modulują konkretne ścieżki mitofagii zamiast brutalnie włączać lub wyłączać autofagię. Dla czytelników niebędących specjalistami kluczowe przesłanie jest takie, że nauczenie się odczytywać i starannie modyfikować ten mitochondrialny system porządkowania może pomóc przekształcić raka trzustki z opornego przeciwnika w chorobę łatwiejszą do opanowania.
Cytowanie: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Słowa kluczowe: rak trzustki, mitofagia, mitochondria, oporność na chemioterapię, metabolizm guza