Clear Sky Science · pl
SUMOylacja skazana na związek z dysfunkcją odporności związaną z komórkami regulatorowymi T
Utrzymywanie pokoju immunologicznego
Nasz układ odpornościowy balansuje na linie: musi atakować groźnych najeźdźców, nie zwracając się przeciw własnym tkankom. Mała grupa białych krwinek zwana komórkami regulatorowymi T, czyli Tregami, pełni w tym rolę strażników pokoju. Ten tekst wyjaśnia, jak maleńki, odwracalny znacznik chemiczny — zwany SUMO — pomaga Tregom wyczuwać stres, dostosowywać swoje zachowanie i, gdy coś idzie nie tak, przyczyniać się albo do chorób autoimmunologicznych, albo do zdolności nowotworów do ukrywania się przed układem odpornościowym.
Molekularne rzepy do kontroli komórek
SUMOylacja to proces przyłączania małych białek o nazwie SUMO do innych białek, jak zapinanie i odpianie molekularnych odznak. W przeciwieństwie do pokrewnych znaczników, które oznaczają białka do zniszczenia, znaczniki SUMO głównie zmieniają, jak białka się ze sobą łączą, gdzie się znajdują w komórce i jak aktywne są. Ponieważ te znaczniki można szybko dodawać i usuwać, działają bardziej jak molekularny ściemniacz niż wyłącznik on–off. W Tregach SUMOylacja koncentruje się zwłaszcza w jądrze komórkowym, gdzie przechowywane jest DNA. Tam kształtuje kluczowe procesy, takie jak naprawa DNA, podział komórki i odczyt genów. Znaczniki SUMO wchodzą też w interakcje z innymi modyfikacjami — jak fosforylacja, acetylacja, metylacja czy ubikwitynacja — tworząc bogaty informacyjnie kod, który pozwala Tregom jednocześnie integrować wiele sygnałów.
Budowanie i ochrona komórek regulatorowych T
Już od najwcześniejszych etapów w grasicy przyszłe limfocyty T polegają na SUMOylacji, by rozwijać się bezpiecznie. Gdy segmenty genów odpornościowych są cięte i składane, aby wytworzyć różnorodne receptory TCR, znaczniki SUMO pomagają prowadzić dokładną naprawę DNA i zapobiegać pozostawaniu niebezpiecznych przerw. Później, podczas selekcji komórek mającej na celu uniknięcie atakowania własnego organizmu, czynniki transkrypcyjne i szlaki sygnałowe regulowane przez SUMO precyzują, które komórki przetrwają jako Tregy. W dojrzałych Tregach SUMO utrzymuje stabilność chromosomów podczas podziału, wspiera tworzenie struktur takich jak jąderko niezbędne do produkcji białek i pomaga chronić integralność genomu w warunkach stresu oksydacyjnego i metabolicznego występującego w tkankach zapalnych i nowotworach. W ten sposób SUMO działa jako cichy architekt różnicowania i przeżycia Tregów.
Włączanie i wyłączanie genów
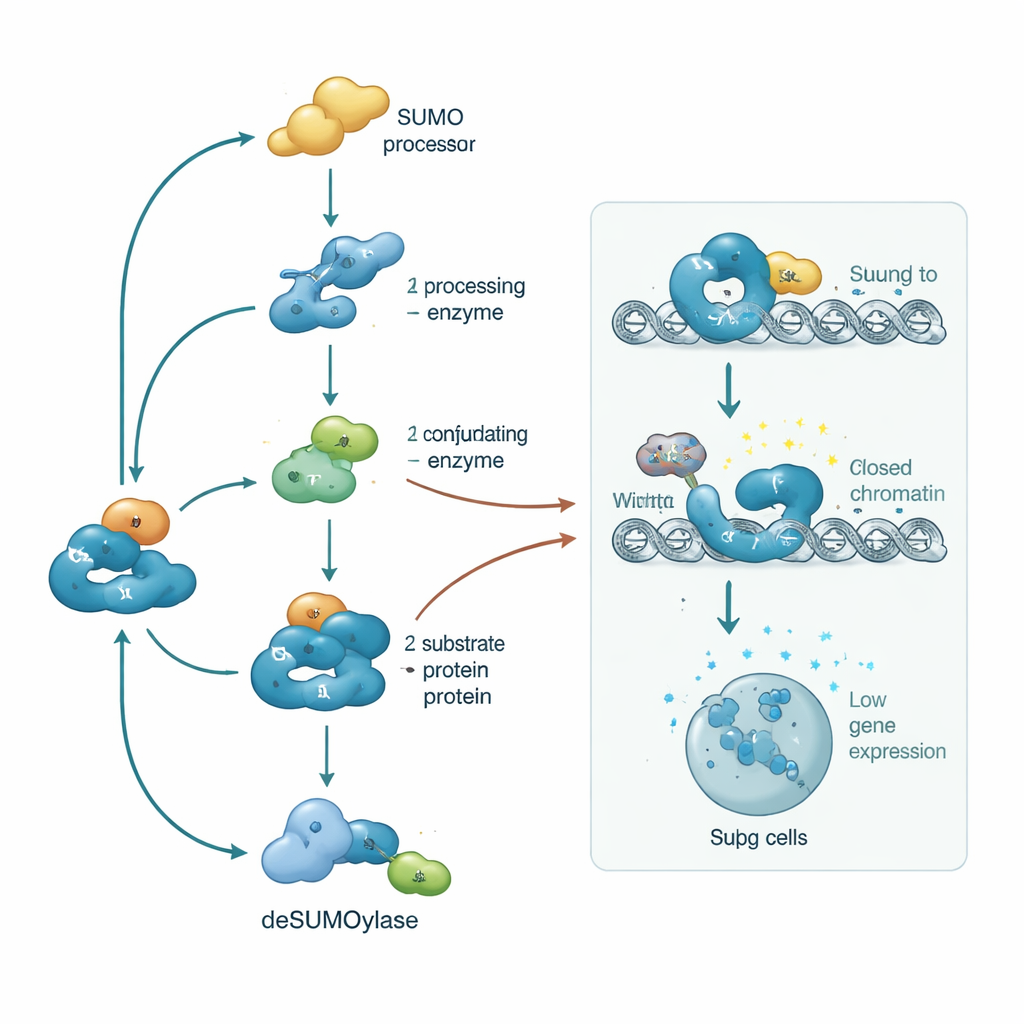
Tregy definiuje odrębny program genowy: muszą stale ekspresjonować „geny tożsamości” takie jak FOXP3, BACH2, IKAROS i IRF4, jednocześnie utrzymując wyciszenie genów zapalnych. SUMOylacja kształtuje obie strony tego równania. Wspiera stabilny, specyficzny dla Tregów wzorzec hipometylacji DNA i aktywujących znaków histonów wokół kluczowych regionów regulacyjnych, pomagając FOXP3 i jego partnerom utrzymać ekspresję przez długi czas. Równocześnie znaczniki SUMO na czynnikach transkrypcyjnych takich jak NF-κB, STATy, NFAT i AP-1 rekrutują korepresory i kompleksy modyfikujące chromatynę, które upakowują DNA w heterochromatynę, utrudniając dostęp do genów zapalnych. Jeśli równowaga SUMO zostanie zaburzona, Tregy mogą utracić FOXP3, nabyć cechy prozapalne, a nawet przekształcić się w szkodliwe efektorowe komórki — zmiana powiązana z autoimmunizacją i utratą tolerancji immunologicznej.
Wybór paliwa i przetrwanie w trudnych warunkach
Tregy są metabolicznie elastyczne: mogą korzystać z glikolizy spalającej cukry, ale szczególnie polegają na szlakach mitochondrialnych spalających tłuszcze i inne paliwa. SUMOylacja wpływa na wiele głównych przełączników kontrolujących te wybory, w tym AMPK, mTOR, LKB1, HIF‑1α, PPARy i SREBPy. Poprzez dostrajanie tych czynników SUMO może przesunąć Tregi z nadmiernej glikolizy w stronę utleniania kwasów tłuszczowych i fosforylacji oksydacyjnej — strategii, która pomaga im przetrwać w niszach o niskiej zawartości glukozy, wysokim stężeniu mleczanu i ubogich w tlen, jak guzy. SUMO reguluje też systemy antyoksydacyjne i enzymy kontroli jakości mitochondriów, co czyni Tregi wyjątkowo odpornymi na stres oksydacyjny, który uszkadza inne limfocyty T. W nowotworach te same mechanizmy mogą zostać zawłaszczone, by zasilać i chronić Tregi, pozwalając im tłumić odpowiedź przeciwnowotworową.
Gdy regulacja zawodzi — i jak można to naprawić
Podsumowując, przegląd argumentuje, że Tregy są w istocie „uzależnione” od SUMOylacji: zależą od tego odwracalnego systemu znakowania, by koordynować rozwój, regulację genów i metabolizm w odpowiedzi na stały stres. Gdy szlaki SUMO są nadmiernie aktywne lub skierowane niewłaściwie, mogą napędzać ucieczkę immunologiczną zależną od Tregów w guzie, a gdy są osłabione — przyczyniać się do chorób autoimmunologicznych i zapalnych. Dla laika kluczowym przekazem jest to, że pozornie drobny znacznik białkowy ma ogromny wpływ na to, czy komórki odpornościowe uciszają stan zapalny, czy pozwalają chorobie rozkwitnąć. Ponieważ enzymów SUMO jest niewiele, a jednocześnie kontrolują wiele celów, leki modulujące ten system mogą dać potężne nowe możliwości — albo wzmocnienia powściągliwości Tregów w autoimmunizacji, albo jej osłabienia w terapii przeciwnowotworowej.
Cytowanie: Qian, J., Yu, L., Tian, M. et al. SUMOylation is destined for regulatory T cell-related immune dysregulation. Cell Death Discov. 12, 90 (2026). https://doi.org/10.1038/s41420-026-02946-x
Słowa kluczowe: komórki regulatorowe T, SUMOylacja, tolerancja immunologiczna, autoimmunizacja, mikrośrodowisko nowotworu