Clear Sky Science · pl
Osteopontyna pochodząca z raka jelita grubego przeprogramowuje makrofagi w kierunku pro-przerzutowego stanu M2 poprzez oś PI3K/AKT/CSF1-CSF1R
Dlaczego to ma znaczenie dla osób z rakiem jelita
Większość zgonów z powodu raka jelita grubego (okrężnicy i odbytnicy) nie wynika z pierwotnego guza, lecz z jego rozsiewu do innych narządów. Badanie to analizuje, jak komórki nowotworowe „komunikują się" z pobliskimi komórkami układu odpornościowego, by ułatwić rozwój przerzutów. Odkrycie kluczowego sygnału wysyłanego przez komórki nowotworowe, który przeprogramowuje komórki odpornościowe na ich wspólników zamiast przeciwników, wskazuje nowe strategie terapeutyczne, które mogą spowolnić lub zatrzymać powstawanie przerzutów w zaawansowanym raku jelita grubego.
Lepka cząsteczka z ciemną stroną
Naukowcy skupili się na białku zwanym osteopontyną (OPN), które wytwarzane jest zarówno przez komórki nowotworowe, jak i przez niektóre komórki odpornościowe obecne w guzach. OPN od dawna wiązana jest z gorszym przebiegiem wielu nowotworów, lecz mechanizm, w jaki sprzyja rozsiewowi w raku jelita grubego, pozostawał niejasny. Analiza dużych baz danych pacjentów i próbek tkankowych wykazała, że poziomy OPN są znacznie wyższe w tkance raka jelita grubego niż w zdrowej śluzówce, szczególnie u chorych z zaawansowaną chorobą i odległymi przerzutami. Pacjenci, których guzy miały wyższe stężenia OPN, zazwyczaj mieli gorsze przeżycie, co sugeruje silny związek OPN z agresywnym, trudnym do leczenia nowotworem.
To nie tylko kwestia samych komórek nowotworowych
Zaskakująco, gdy naukowcy zmuszali w warunkach laboratoryjnych komórki raka jelita grubego do wytwarzania większej lub mniejszej ilości OPN, same komórki nie stawały się istotnie bardziej inwazyjne ani ruchliwe. Ich wzrost, migracja i zdolność do przenikania przez sztuczne membrany zmieniały się bardzo nieznacznie. To podważyło powszechne przekonanie, że OPN działa przede wszystkim poprzez bezpośrednie wzmacnianie właściwości samych komórek nowotworowych. Zamiast tego zespół zwrócił uwagę na mikrośrodowisko guza — a szczególnie na grupę komórek odpornościowych zwanych makrofagami, które mogą albo atakować guzy (stan „M1”), albo je wspierać (stan „M2").
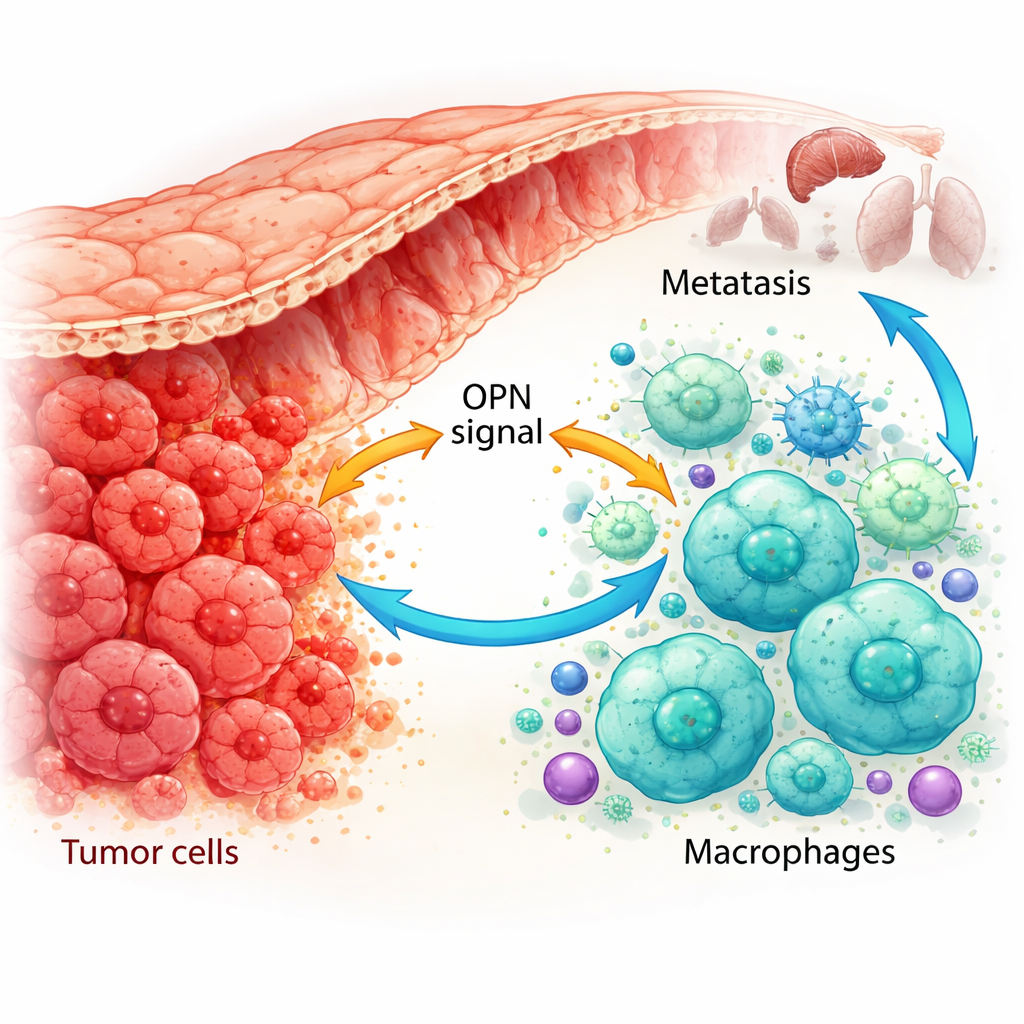
Jak komórki odpornościowe zostają przeprogramowane na pomocników guza
Wykorzystując mapowanie genów pojedynczych komórek i zaawansowane barwienia tkanek pacjentów, badacze pokazali, że OPN jest produkowana nie tylko przez komórki nowotworowe, lecz także przez makrofagi związane z guzem. W nowotworach, które już dały przerzuty, zarówno komórki nowotworowe, jak i określony podtyp makrofagów wykazywały wysokie poziomy OPN. Te makrofagi miały skłonność do stanu przypominającego M2, wspierającego guz, i były liczniejsze tam, gdzie poziom OPN w guzie był wysoki. W modelach mysich guzy zaprojektowane do produkcji większej ilości OPN przyciągały więcej makrofagów o fenotypie M2 i rosły szybciej, podczas gdy guzy z obniżonym OPN miały mniej makrofagów M2 i wolniejszy wzrost. Sugeruje to, że OPN jest silnym czynnikiem przyciągającym i przeprogramowującym makrofagi w mikrośrodowisku guza.
Ukryty łańcuch sygnałowy: od OPN do powstawania przerzutów
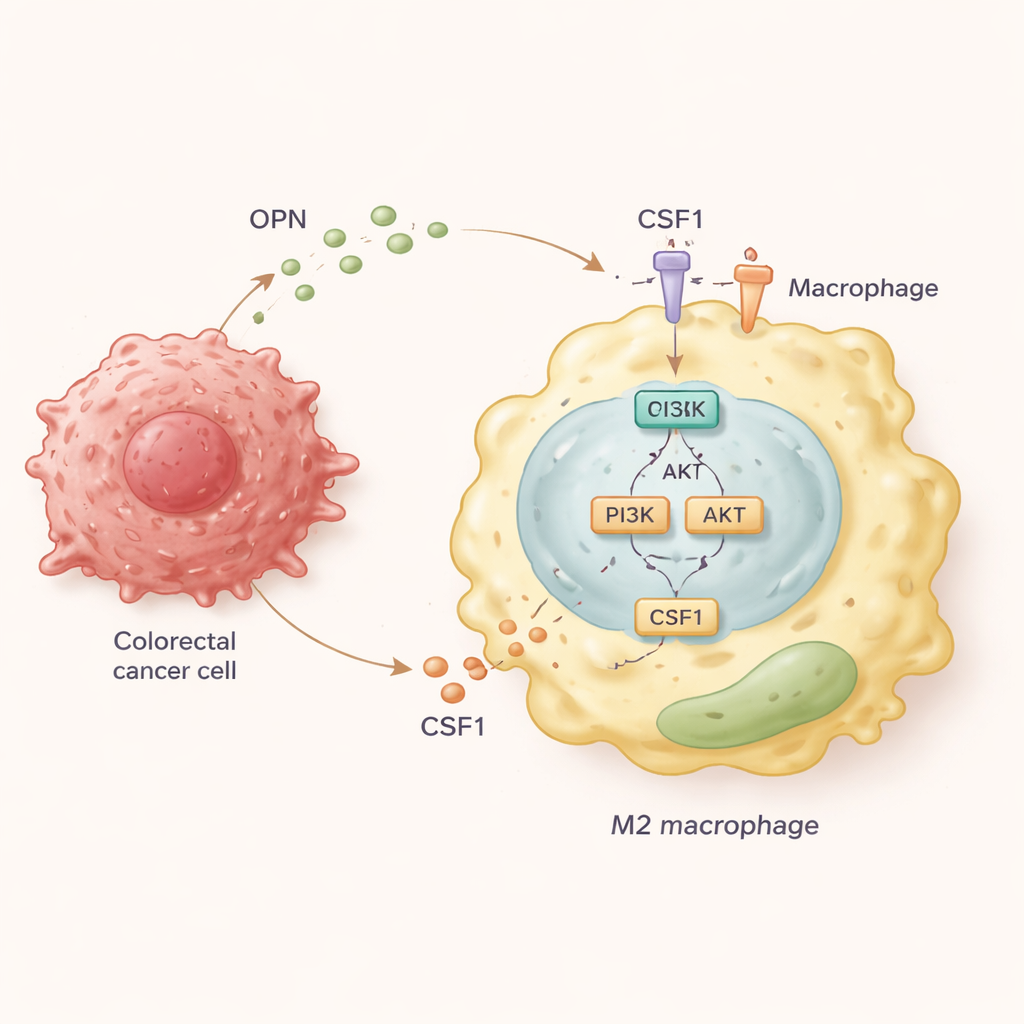
Aby ustalić molekularny łańcuch zdarzeń, zespół hodował ludzkie makrofagi razem z komórkami raka jelita grubego wytwarzającymi różne ilości OPN. Stwierdzili, że komórki z wysokim poziomem OPN przesuwały makrofagi w kierunku stanu M2 i wspierały dwukierunkową mobilność: makrofagi migrowały w stronę guza, a komórki nowotworowe stawały się bardziej inwazyjne w odpowiedzi na sygnały od tych makrofagów. Pogłębiając badania, naukowcy odkryli, że OPN aktywuje w makrofagach szlak sygnałowy PI3K/AKT. Ta aktywacja powoduje, że makrofagi uwalniają duże ilości innej cząsteczki — CSF1 — oraz zwiększają ekspresję jej receptora CSF1R na swojej powierzchni. CSF1 działa w pętli pozytywnego sprzężenia zwrotnego, umacniając stan M2 sprzyjający przerzutom i dalsze przyciąganie makrofagów do guza.
Przerwanie pętli, by spowolnić rozsiew
W modelach mysich raka jelita grubego z rozsiewem do jamy brzusznej badacze przetestowali lek blokujący CSF1R o nazwie PLX3397. Myszy z nowotworami o wysokim poziomie OPN rozwijały liczne guzki przerzutowe, ale leczenie inhibitorem CSF1R znacząco zmniejszyło zarówno liczbę przerzutów, jak i obecność makrofagów o fenotypie M2 w guzach. Komórki nowotworowe wykazywały mniejszy wzrost i więcej oznak zaprogramowanej śmierci komórkowej. Co istotne, lek głównie eliminował makrofagi promujące guz, nie wpływając znacząco na bardziej zapalne typy, co sugeruje stosunkowo ukierunkowany sposób osłabienia systemu wsparcia guza.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą główny wniosek jest taki, że niektóre raki jelita grubego odnoszą sukces w rozsiewie nie tylko dlatego, że same komórki są agresywne, lecz dlatego, że przechwytują pobliskie komórki odpornościowe i przekształcają je w współwinnych. W tym badaniu OPN pochodząca z komórek nowotworowych działa jak główny przełącznik, przeprogramowując makrofagi poprzez szlak PI3K/AKT oraz CSF1/CSF1R, tworząc sprzyjające przerzutom środowisko. Przerwanie tego łańcucha — szczególnie na etapie CSF1R — zmniejszyło rozsiew w modelach mysich. To sugeruje, że pomiar poziomów OPN mógłby pomóc zidentyfikować pacjentów, którzy mogliby skorzystać z terapii ukierunkowanych na makrofagi, a łączenie takich leków z istniejącymi terapiami czy immunoterapiami może dawać nowe możliwości dla osób z zaawansowanym rakiem jelita grubego.
Cytowanie: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Słowa kluczowe: rak jelita grubego, osteopontyna, makrofagi związane z guzem, przerzuty, hamowanie CSF1R