Clear Sky Science · pl
Celowanie w sygnalizację NXPH4/ALDH1L2 tłumi oporność na enzalutamid w raku prostaty
Dlaczego to ma znaczenie dla pacjentów z rakiem prostaty
Wielu mężczyzn z zaawansowanym rakiem prostaty polega na silnym leku blokującym hormony, zwanym enzalutamidem. Początkowo często działa on dobrze, zmniejszając guzy i hamując rozwój choroby. Jednak u większości pacjentów nowotwór w końcu znajduje sposób, by ominąć lek i zaczyna rosnąć ponownie. To badanie zagłębia się w mechanizmy tego uciekania i wskazuje nowy słaby punkt w guzach opornych na leki — oferując potencjalną drogę do wydłużenia i poprawy skuteczności istniejących terapii.
Powszechne leczenie napotyka uparte schorzenie
Wzrost raka prostaty jest ściśle związany z męskimi hormonami, czyli androgenami, które działają przez białko zwane receptorem androgenowym. Enzalutamid ma na celu zablokowanie tego receptora i jest standardową terapią, gdy guzy przestają reagować na tradycyjne leczenie obniżające poziom hormonów. Niestety wiele guzów adaptuje się, stając się tym, co lekarze nazywają rakiem prostaty opornym na kastrację. Autorzy tej pracy postanowili odkryć, które geny pomagają komórkom nowotworowym przetrwać działanie enzalutamidu, mając nadzieję, że zablokowanie tych pomocników może przywrócić skuteczność leku.
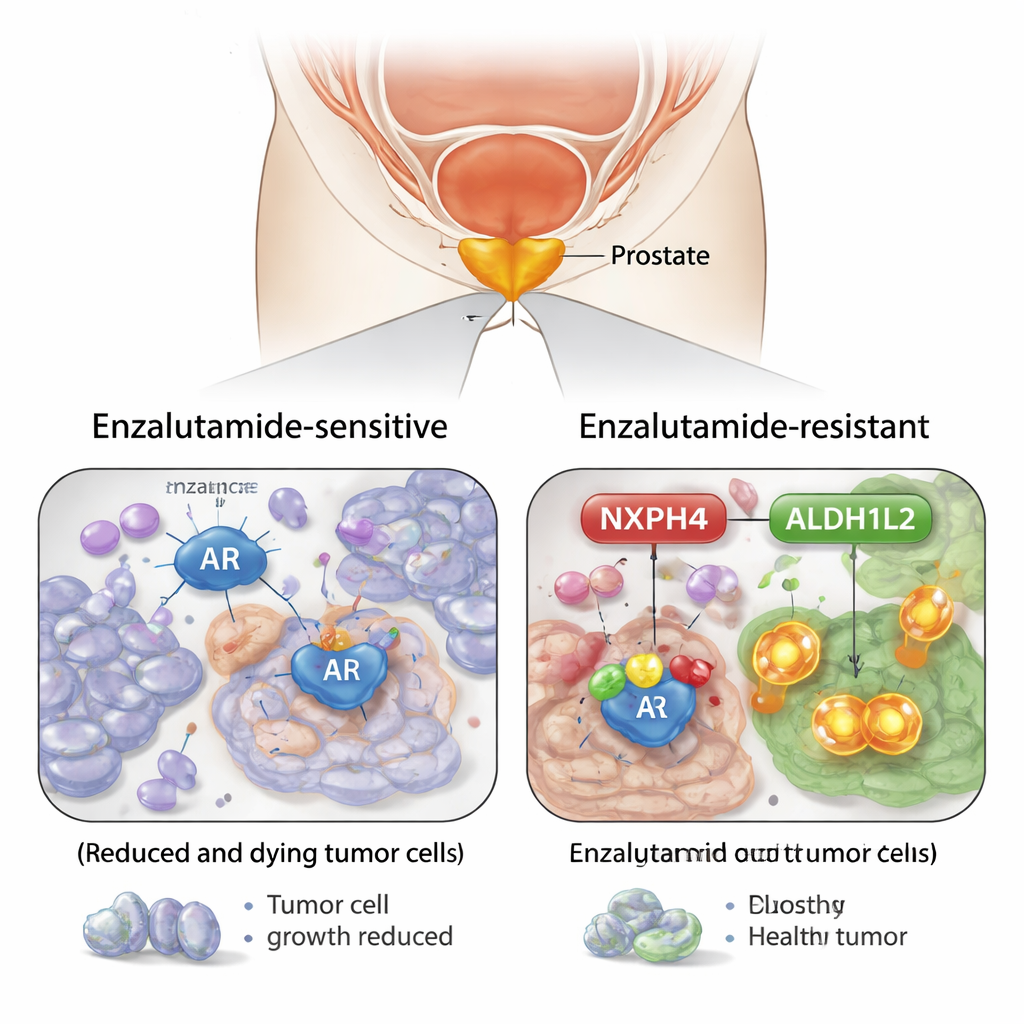
Wyróżnienie zaskakującej cząsteczki pomocniczej
Porównując komórki raka prostaty wrażliwe na enzalutamid z komórkami, które stały się oporne, zespół zidentyfikował białko o nazwie NXPH4 jako kluczowego gracza. Komórki oporne produkowały znacznie więcej NXPH4, a jego poziomy rosły stopniowo, gdy komórki były długotrwale eksponowane na enzalutamid. Próbki tkankowe od pacjentów wykazały ten sam wzorzec: wyższe stężenia NXPH4 w bardziej agresywnych guzach i w nowotworach, które przestały reagować na lek. Gdy badacze zmniejszyli poziom NXPH4 w komórkach opornych, komórki stały się łatwiejsze do zabicia enzalutamidem i tworzyły mniej kolonii, zarówno na szalkach, jak i w modelach mysich. W przeciwieństwie do tego, wymuszone zwiększenie produkcji NXPH4 uczyniło komórki trudniejszymi do leczenia.
Jak hormony uruchamiają NXPH4
Badanie zastanawiało się także, dlaczego NXPH4 jest tak obfity w tych guzach. Odpowiedź ponownie wskazała na receptor androgenowy. Naukowcy pokazali, że gdy komórki były traktowane hormonem dihydrotestosteronem, poziomy NXPH4 rosły. Dodanie dodatkowego receptora androgenowego zwiększało NXPH4; zablokowanie receptora powodowało spadek NXPH4. Szczegółowe eksperymenty z DNA potwierdziły, że receptor androgenowy fizycznie wiąże się z regionem kontrolnym genu NXPH4, włączając jego ekspresję. Oznacza to, że ten sam system napędzany hormonami, który pobudza wzrost raka prostaty, także przygotowuje komórki przez zwiększenie NXPH4, co sprzyja późniejszej oporności na lek.
Wzmacnianie „elektrowni” komórki
Dalsze badania wykazały, że NXPH4 zmienia sposób, w jaki komórki nowotworowe zarządzają energią i stresem w mitochondriach — malutkich elektrowniach komórkowych. W warunkach blokowania hormonów część NXPH4 przemieszcza się do mitochondriów i wiąże z innym białkiem, ALDH1L2, które jest kluczowe dla wytwarzania NADPH, ważnej cząsteczki kontrolującej reaktywne formy tlenu (ROS). W komórkach opornych NXPH4 i ALDH1L2 tworzą kompleks, który wzmacnia oddychanie mitochondrialne, utrzymuje potencjał błony mitochondrialnej, zwiększa poziomy NADPH i obniża poziom ROS. To połączenie utrzymuje mitochondria w dobrej kondycji i pozwala komórkom nowotworowym przetrwać stres wywołany enzalutamidem, zamiast umierać tak, jak zwykle by to miało miejsce.
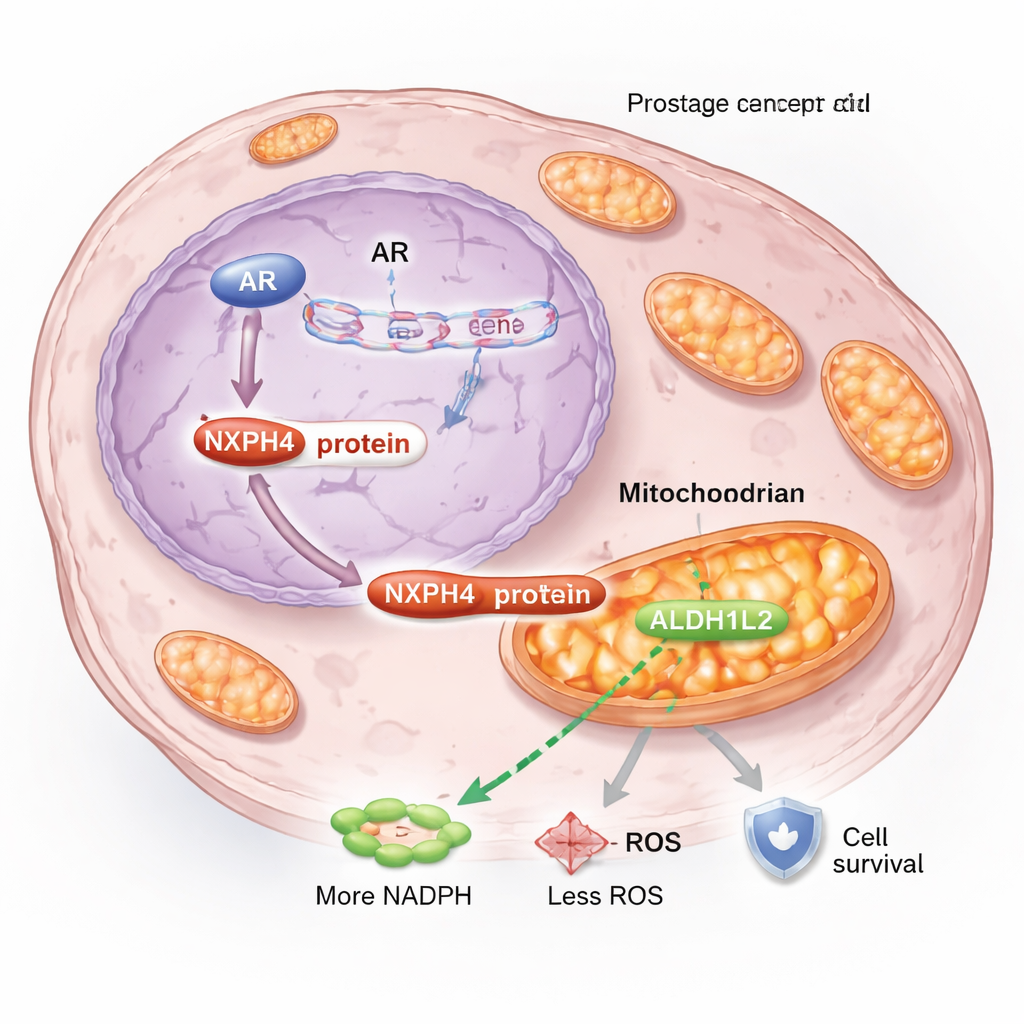
Przerwanie obwodu oporności
Gdy badacze zakłócili ten system wsparcia mitochondrialnego, efekty były uderzające. Zmniejszenie ekspresji NXPH4 w komórkach opornych obniżyło aktywność mitochondrialną, zwiększyło stres oksydacyjny, spowolniło wzrost i uczyniło komórki znacznie bardziej wrażliwymi na enzalutamid. Wyciszenie ALDH1L2 dało podobny efekt i zniwelowało ochronne korzyści wynikające z nadmiaru NXPH4, potwierdzając, że te dwa białka działają razem. W modelach mysich guzy pozbawione NXPH4 rosły wolniej, a połączenie utraty NXPH4 z leczeniem enzalutamidem zmniejszało guzy jeszcze bardziej niż każdy z tych zabiegów osobno. Wyniki sugerują, że partnerstwo NXPH4–ALDH1L2 nie jest jedynie ubocznym skutkiem oporności, lecz siłą napędową stojącą za nią.
Co to może znaczyć dla przyszłego leczenia
Mówiąc prosto, praca ta pokazuje, że niektóre raki prostaty przetrwają enzalutamid, przeorganizowując swoje źródła energii. NXPH4, uruchamiany przez receptor androgenowy, współpracuje z ALDH1L2 w mitochondriach, by utrzymać je w aktywności, chronić przed uszkodzeniami oksydacyjnymi i pomagać komórkom guza przetrwać terapię blokującą hormony. Celowanie w NXPH4 lub w jego interakcję z ALDH1L2 mogłoby osłabić ten obwód przetrwania. Choć leki bezpośrednio przeciwko NXPH4 nie istnieją jeszcze, badanie wskazuje tę parę molekuł jako obiecujący nowy cel. W przyszłości łączenie enzalutamidu z lekami zakłócającymi sygnalizację NXPH4‑ALDH1L2 może pomóc pacjentom dłużej wyprzedzać oporny rak prostaty.
Cytowanie: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
Słowa kluczowe: rak prostaty, oporność na enzalutamid, metabolizm mitochondrialny, NXPH4, ALDH1L2