Clear Sky Science · pl
Trim15 stabilizuje VDAC3 poprzez ubikwitynację, tłumiąc autofagię i zwiększając chemiowrażliwość w płaskonabłonkowym raku nagłośni
Dlaczego to badanie nad rakiem ma znaczenie
Płaskonabłonkowy rak nagłośni to trudny do leczenia nowotwór gardła o niskich wskaźnikach przeżywalności i ograniczonych opcjach terapeutycznych, gdy rozsiewa się albo przestaje reagować na leki. To badanie ujawnia ukrytą ścieżkę komórkową, która decyduje, czy komórki nowotworowe giną podczas terapii, czy też cicho adaptują się i przetrwają. Wyjaśniając, w jaki sposób dwa białka, Trim15 i VDAC3, kontrolują procesy samoczyszczenia komórki i odpowiedzi na stres, praca wskazuje nowe sposoby poprawienia skuteczności istniejącej chemioterapii.
Śmiertelny rak gardła ukryty na widoku
Nagłośnia znajduje się głęboko w gardle, więc guzy tam rosnące często pozostają niezauważone aż do zaawansowanego stadium. Wówczas lekarze muszą wybierać między agresywną chirurgią, która może znacząco zaburzyć mowę i połykanie, a terapiami oszczędzającymi narząd, takimi jak chemioterapia i radioterapia, które nie zawsze prowadzą do wyleczenia. Ponieważ przeżywalność nie poprawiła się znacząco w ciągu ostatnich dekad, badacze analizują biologiczne mechanizmy leżące u podstaw wzrostu, rozsiewu i oporności tych guzów. Obecne badanie koncentruje się na tym, jak komórki nowotworowe radzą sobie z uszkodzonymi mitochondriami — ich „elektrowniami” — i jak to kształtuje reakcję na stres i terapię.
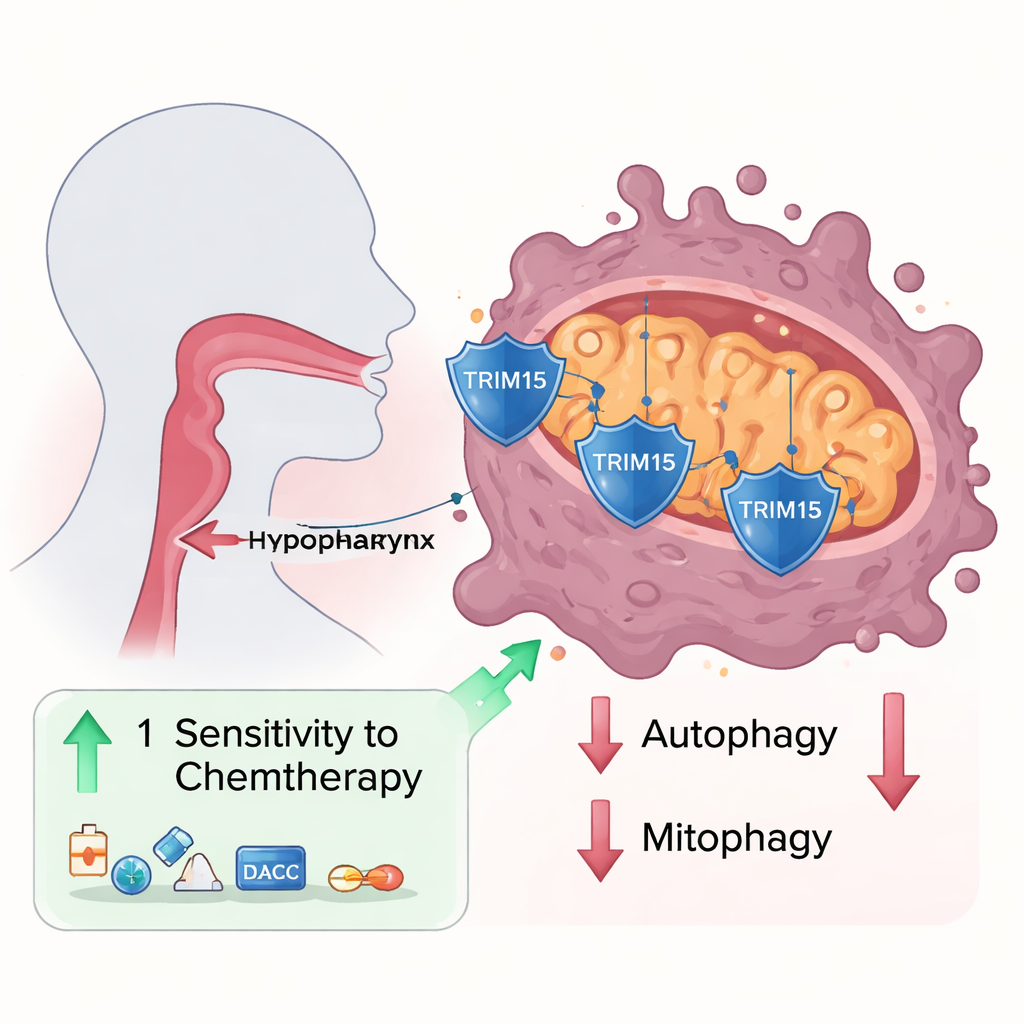
Znikające białko‑strażnik
Naukowcy przebadali próbki nowotworowe i linie komórkowe z raka nagłośni i stwierdzili, że białko o nazwie Trim15 było konsekwentnie zmniejszone w porównaniu z sąsiednią tkanką prawidłową. Kiedy wymuszono w komórkach nowotworowych większą ekspresję Trim15, komórki rosły i migrowały wolniej; gdy je usunięto, stały się bardziej agresywne. Za pomocą biochemicznych eksperymentów typu pull‑down odkryto, że Trim15 fizycznie oddziałuje z innym białkiem, VDAC3, które lokalizuje się w zewnętrznej błonie mitochondriów i pełni rolę bramki dla cząsteczek przemieszczających się do i z mitochondrium. Zamiast znakować VDAC3 do zniszczenia, Trim15 dodaje specyficzny rodzaj modyfikacji molekularnej, który w rzeczywistości stabilizuje VDAC3, utrzymując jego wysokie poziomy.
Jak komórki nowotworowe recyklingują swoje elektrownie
Mitochondria są ciągle monitorowane i, gdy są uszkodzone, mogą być usuwane poprzez wyspecjalizowany proces recyklingu zwany mitofagią. Zespół wykazał, że VDAC3 normalnie działa jak hamulec tego recyklingu. Gdy VDAC3 było obfite, markery ogólnej autolizy (autofagii) i mitofagii obniżały się; gdy VDAC3 było zmniejszone, te procesy przyspieszały, a więcej mitochondriów było otaczanych i rozkładanych. Ta zmiana wpływała też na równowagę reaktywnych form tlenu (ROS) — chemicznie reaktywnych cząsteczek często opisywanych jako „spaliny” komórkowe. Wysokie VDAC3 podnosiło poziomy ROS, zwiększając stres komórek, natomiast niskie VDAC3 pozwalało komórkom usuwać uszkodzone mitochondria, obniżać ROS i lepiej przetrwać w trudnych warunkach.
Alkohol, stres oksydacyjny i oporność na leki
Przewlekła ekspozycja na alkohol jest głównym czynnikiem ryzyka raka nagłośni, częściowo dlatego, że skoncentrowany etanol wielokrotnie obmywa wyściółkę gardła. Gdy badacze wystawili komórki nowotworowe na działanie alkoholu w laboratorium, zarówno poziomy Trim15, jak i VDAC3 spadły. Ten spadek wydawał się adaptacyjnym ruchem komórek nowotworowych: osłabiając oś Trim15–VDAC3, zwiększały mitofagię, utrzymywały ROS na bezpieczniejszych poziomach i tolerowały uszkodzenia wywołane alkoholem. Podobna odpowiedź wystąpiła po zastosowaniu standardowego leku chemioterapeutycznego 5‑fluorouracylu (5‑FU): leczenie obniżało Trim15 i VDAC3, co prawdopodobnie pomaga komórkom nowotworowym unikać śmiertelnego stresu oksydacyjnego i przyczynia się do oporności na chemioterapię.
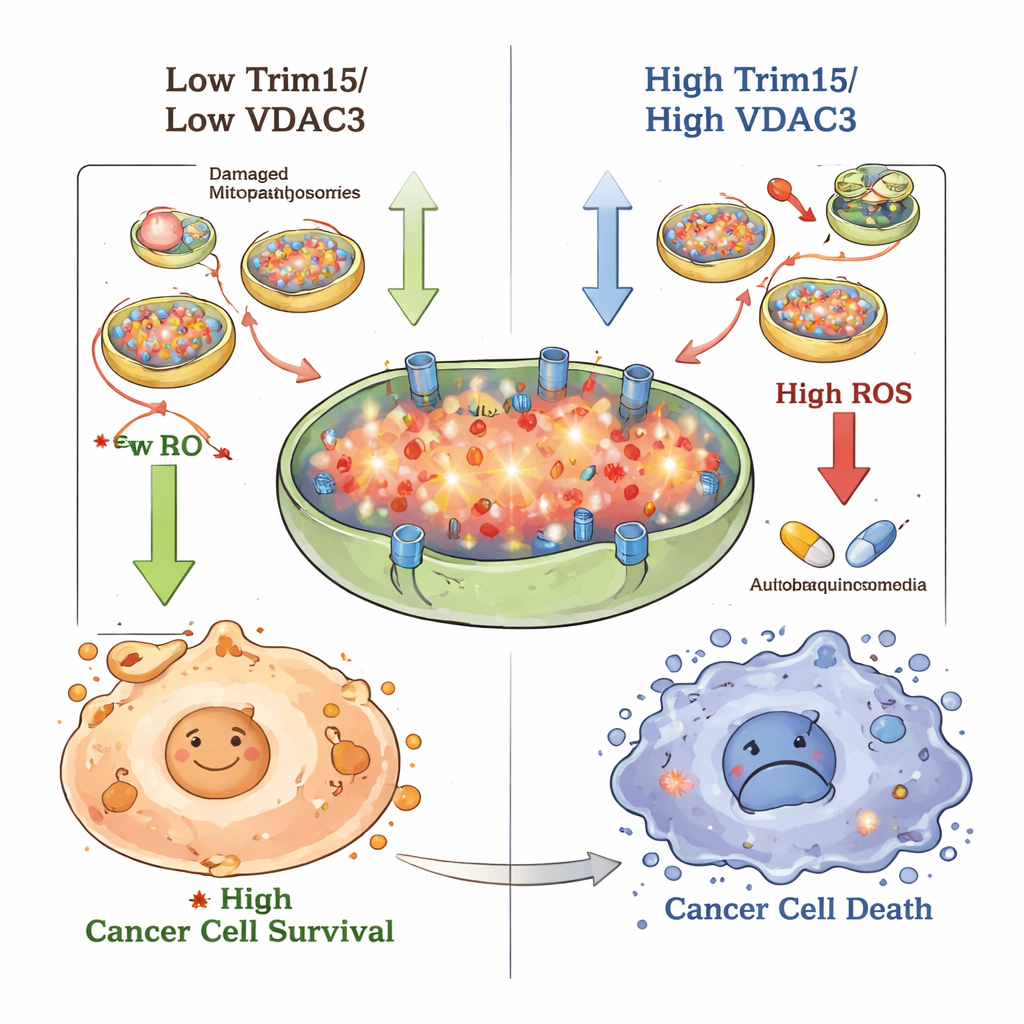
Wyłączenie mechanizmu samoochrony, by wzmocnić chemioterapię
Zespół zapytał następnie, czy zablokowanie autofagii może pozbawić komórki tej ochrony. Użyli chlorochiny, znanego od dawna leku przeciwmalarycznego, który zaburza końcowe etapy komórkowego samopożerania. W hodowlach komórek chlorochina sama w sobie spowalniała wzrost i migrację komórek raka nagłośni oraz niwelowała przewagę wzrostu wynikającą z utraty VDAC3. U myszy z wszczepionymi ludzkimi guzami chlorochina i 5‑FU każdy z osobna zmniejszały guzy, ale ich połączenie działało najlepiej, redukując objętość i masę guza bardziej niż którykolwiek lek oddzielnie, bez widocznie nasilonej toksyczności. Co istotne, wymuszenie nadprodukcji Trim15 lub VDAC3 uczyniło komórki bardziej wrażliwymi na 5‑FU, częściowo poprzez podniesienie poziomu ROS do wartości, które komórki nie były już w stanie kontrolować.
Co to oznacza dla przyszłych terapii
Dla osoby nietechnicznej badanie pokazuje, że część komórek raka nagłośni przeżywa chemioterapię, stając się sprawniejszymi „recyklerami”: szybko usuwają uszkodzone mitochondria i utrzymują stres oksydacyjny wystarczająco niski, by uniknąć śmierci. Trim15 i VDAC3 współdziałają jako przeciwwaga tej strategii — gdy są obecne, ograniczają recykling i zwiększają stres, co ułatwia zabijanie komórek nowotworowych. Celowanie w tę oś Trim15–VDAC3–mitofagia, na przykład za pomocą leków takich jak chlorochina dodanych do standardowej chemioterapii, może w przyszłości uczynić oporne guzy gardła bardziej podatnymi na leczenie i poprawić wyniki pacjentów.
Cytowanie: Wang, G., Shen, Y., Wang, L. et al. Trim15 stabilizes VDAC3 via ubiquitination to suppress autophagy and enhance chemosensitivity in hypopharyngeal squamous cell carcinoma. Cell Death Discov. 12, 88 (2026). https://doi.org/10.1038/s41420-026-02943-0
Słowa kluczowe: rak nagłośni, autofagia, mitochondria, oporność na chemioterapię, chlorochina