Clear Sky Science · pl
Rottlerin wywołuje podwójną degradację SLC7A11 i GPX4, prowadząc do ferroptozy i zwiększenia wrażliwości na chemioterapię w raku wątrobowokomórkowym
Dlaczego ten naturalny związek ma znaczenie dla raka wątroby
Rak wątrobowokomórkowy, najczęstsza postać pierwotnego raka wątroby, jest często rozpoznawany późno i wciąż trudny do leczenia. W badaniu sprawdzono, czy pochodna roślinna zwana rottleriną, od dawna znana z szerokiego spektrum właściwości przeciwnowotworowych, może zostać wykorzystana do wywołania nowszego typu śmierci komórkowej, zwanego ferroptozą, w komórkach raka wątroby. Poprzez zrozumienie działania rottlerinu na poziomie molekularnym, badacze liczą na otwarcie nowych dróg do skuteczniejszych terapii, na które trudniej będzie nabrać oporności.
Nowy sposób na zabijanie komórek nowotworowych
Tradycyjne leki przeciwnowotworowe zazwyczaj wymuszają w komórkach nowotworowych dobrze poznane programy śmierci, takie jak apoptoza. Ferroptoza różni się tym, że jest procesem zależnym od żelaza, napędzanym przez nagromadzenie toksycznych tłuszczów w błonach komórkowych. Komórki raka wątroby są szczególnie podatne na tego typu uszkodzenia, ponieważ silnie polegają na systemach antyoksydacyjnych, które utrzymują te lipidowe toksyny w ryzach. Zespół postawił pytanie, czy rottlerin może sabotować te mechanizmy obronne i w ten sposób wymusić ferroptozę w komórkach raka wątroby.
Jak rottlerin hamuje wzrost guza
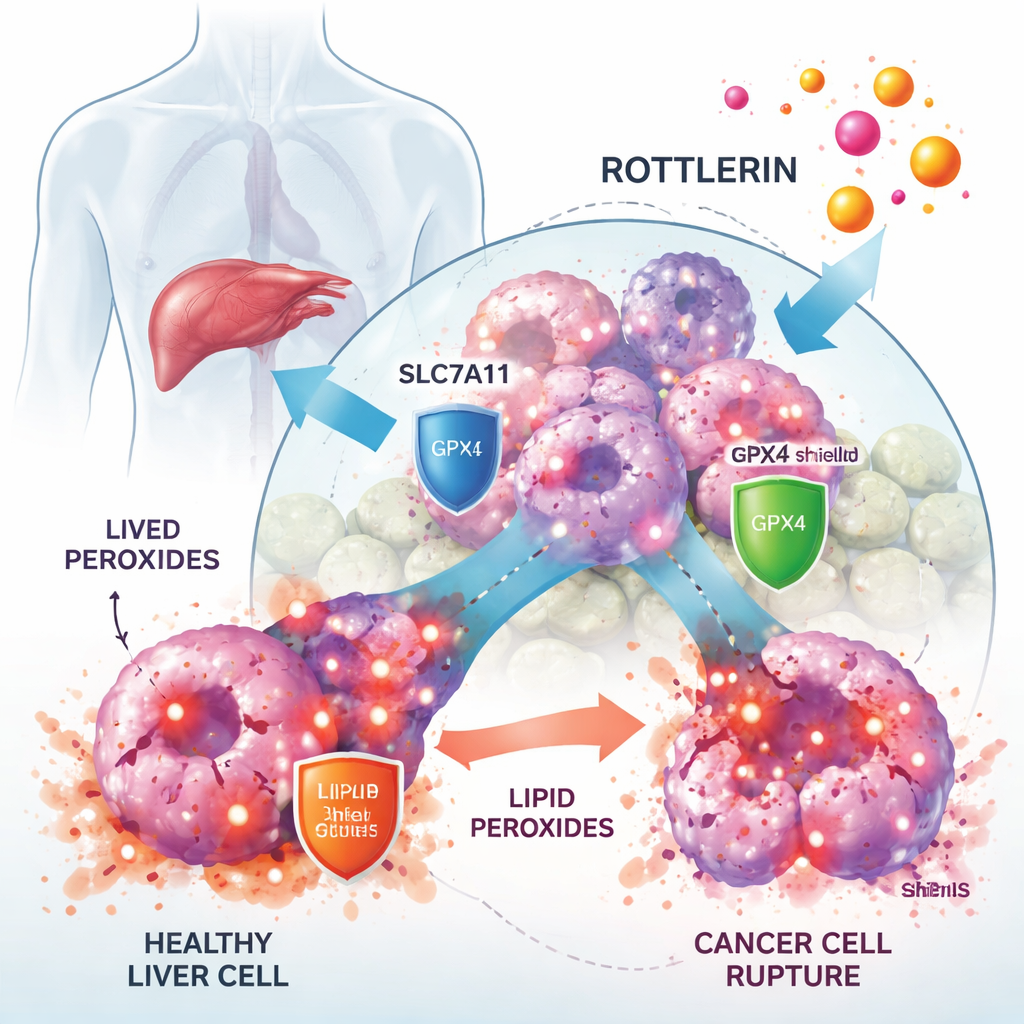
Pracując na ludzkich liniach komórek raka wątroby, badacze wykazali, że rottlerin silnie zmniejszał wzrost komórek nowotworowych przy niskich stężeniach rzędu mikromoli, podczas gdy normalne komórki związane z wątrobą były mniej dotknięte. Gdy dodano specyficzny bloker ferroptozy, Ferrostatyn‑1, znaczną część śmierci komórek wywołanej przez rottlerin udało się odwrócić, co silnie sugeruje, że głównym mechanizmem zabijania była ferroptoza. Mikroskopia i testy biochemiczne potwierdziły to: komórki traktowane rottleriną gromadziły wysokie poziomy nadtlenków lipidów, wykazywały zmiany w mitochondriach oraz obniżone ilości glutationu — wszystko to charakterystyczne cechy ferroptozy.
Rozbrajanie tarcz antyoksydacyjnych komórek
Komórki raka wątroby przetrwają dzięki krytycznej osi obronnej zbudowanej z transportera SLC7A11 i enzymu GPX4. SLC7A11 importuje cystynę, składnik budulcowy glutationu, natomiast GPX4 wykorzystuje glutation do neutralizacji nadtlenków lipidów zanim uszkodzą błony. Badanie wykazało, że rottlerin prowadził do spadku poziomu białek SLC7A11 i GPX4 w czasie. Nie wynikało to z zaprzestania ich syntezy, lecz z faktu, że białka te były oznaczane małymi „etykietami do zniszczenia” (ubikwityną) i kierowane do komórkowej maszyny rozkładającej białka, proteasomu. Zablokowanie proteasomu odwróciło tę utratę, a sztuczne zwiększenie poziomu SLC7A11 lub GPX4 w komórkach częściowo je chroniło przed rottleriną. Razem te wyniki pokazują, że rottlerin działa jako podwójny degrader dwóch kluczowych obrońców przed ferroptozą.
Wzmacnianie istniejących leków na raka wątroby
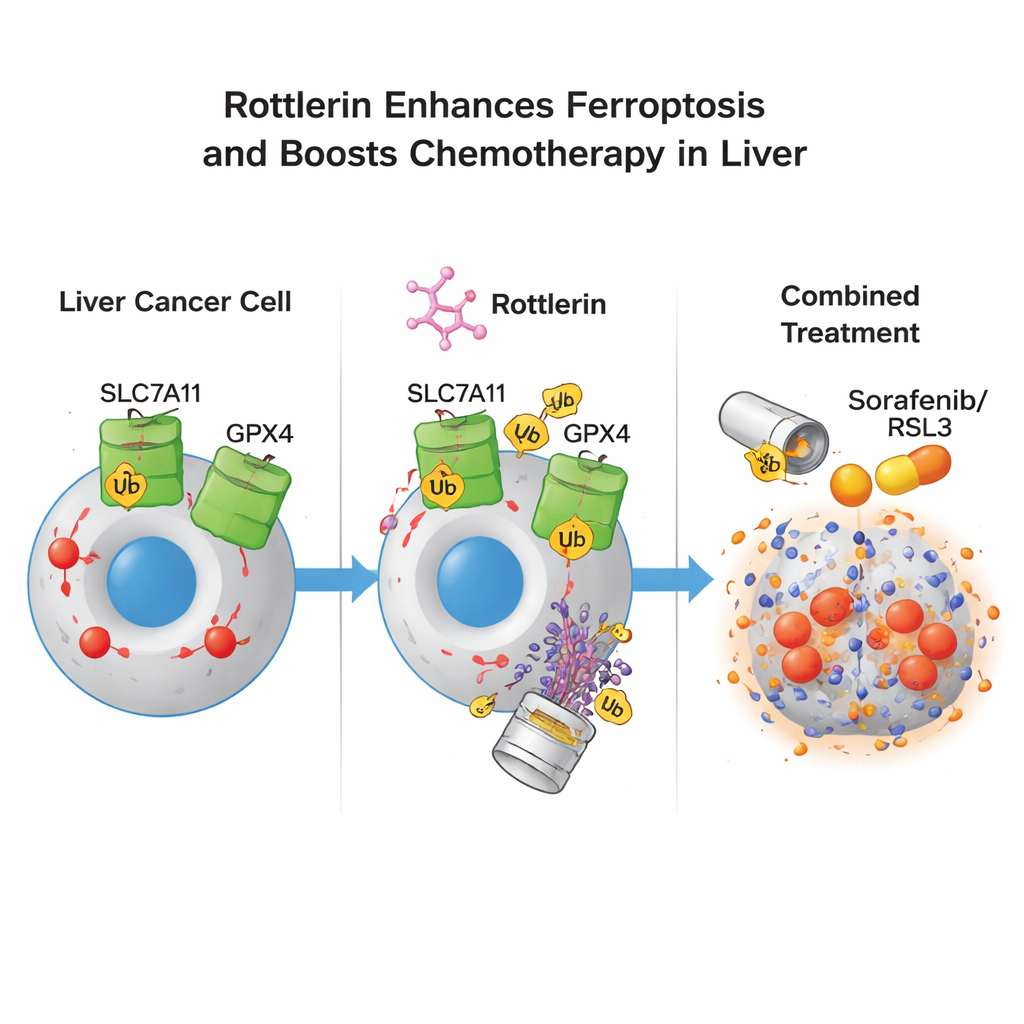
Wielu pacjentów z zaawansowanym rakiem wątroby otrzymuje sorafenib, standardowy lek pierwszego rzutu, który sam potrafi indukować ferroptozę, lecz oporność często ogranicza jego skuteczność. Autorzy sprawdzili, czy niskie, same w sobie słabe dawki rottlerinu mogą uczynić komórki nowotworowe bardziej wrażliwymi na leki indukujące ferroptozę, takie jak sorafenib i RSL3. W hodowlach komórkowych połączenie niskodawkowego rottlerinu z którymkolwiek z tych leków znacząco zwiększało śmierć komórek nowotworowych i przesuwało krzywe dawka‑odpowiedź, co wskazuje na większą skuteczność. Co ważne, efekt zwiększający wrażliwość utrzymywał się nawet po genetycznym obniżeniu klasycznego celu rottlerinu, kinazy PKCδ, co pokazuje, że kluczowe działanie nie przebiegało przez tę kinazę, lecz przez degradację SLC7A11 i GPX4. W modelach mysich z implantowanymi ludzkimi guzami wątroby leczenie łączone rottleriną i sorafenibem spowolniło wzrost guza bardziej niż sam sorafenib i dodatkowo obniżyło poziomy SLC7A11 i GPX4 w guzach.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami przesłanie jest takie: rottlerin działa jak „wytrych na dwa zamki” w komórkach raka wątroby — jednocześnie usuwa dwa kluczowe zamki — SLC7A11 i GPX4 — które normalnie chronią komórki przed śmiercionośną falą oksydacji tłuszczowej. Gdy te zamki znikają, komórki nowotworowe stają się znacznie bardziej podatne na ferroptozę, zwłaszcza w połączeniu z istniejącymi lekami, które popychają je w tym kierunku. Choć przed zastosowaniem rottlerinu lub powiązanych związków u pacjentów potrzebne są dalsze badania, strategia podwójnego degradowania oferuje obiecujący sposób obejścia adaptacyjnych mechanizmów obronnych, które często utrudniają leczenie guzów wątroby.
Cytowanie: Luo, H., Jin, X., Gao, C. et al. Rottlerin triggers dual degradation of SLC7A11 and GPX4 to drive ferroptosis and chemosensitization in hepatocellular carcinoma. Cell Death Discov. 12, 89 (2026). https://doi.org/10.1038/s41420-026-02942-1
Słowa kluczowe: rak wątroby, ferroptoza, rottlerin, SLC7A11, GPX4