Clear Sky Science · pl
Aktywacja GCN2, a następnie odpowiedzi na nieprawidłowo pofałdowane białka przez doustną małą cząsteczkę NXP800 opóźnia wzrost guza w mięsakach kości
Zmiana stresu nowotworu w jego słabość
Mięsak kości (osteosarcoma) to rzadki, ale agresywny nowotwór kości, który najczęściej dotyka dzieci i młodych dorosłych. Od dekad leczenie opiera się na intensywnej chemioterapii i operacji, jednak przeżywalność pacjentów z zaawansowaną chorobą uległa niewielkiej poprawie. W niniejszym badaniu zbadano nową tabletkę o nazwie NXP800, która ma wykorzystać ukrytą słabość komórek nowotworowych: ich stałą walkę z wewnętrznym stresem. Poprzez zwiększenie tego stresu ponad punkt krytyczny, NXP800 może zmusić komórki guza do samozniszczenia, oszczędzając przy tym większość zdrowych komórek.
Trudny nowotwór kości potrzebujący nowych opcji
Mięsak kości zwykle rozwija się w długich kościach ramion i nóg i może szybko dawać przerzuty do płuc. Standardowe leczenie łączy kilka silnych leków chemioterapeutycznych z operacją usunięcia guza. Choć podejście to leczy wielu pacjentów z chorobą miejscową, wyniki są złe u tych, których guzy nawracają lub już dają przerzuty przy rozpoznaniu. Ponieważ obecne leki osiągnęły swoje ograniczenia, badacze poszukują terapii atakujących mięsak kości w zupełnie nowy sposób, najlepiej celując w cechy odróżniające komórki nowotworowe od tkanki prawidłowej.
Wykorzystywanie stresu przeciwko komórkom guza
Komórki nowotworowe żyją w ciągłym napięciu. Dzielą się szybko, zużywają dużą ilość energii i tlenu oraz często doświadczają surowych warunków, takich jak niedotlenienie czy ekspozycja na chemioterapię. Aby sobie radzić, polegają na systemach awaryjnych, które pomagają prawidłowo składać i przetwarzać białka oraz dostosowywać metabolizm. Jednym z tych systemów jest tzw. odpowiedź na nieprawidłowo pofałdowane białka (unfolded protein response), uruchamiana gdy fabryka białek komórki — retikulum endoplazmatyczne — jest przeciążone. Innym jest zintegrowana odpowiedź na stres, która wykrywa różne rodzaje stresu i spowalnia produkcję białek. Zazwyczaj te szlaki pomagają komórkom nowotworowym przetrwać — ale jeśli są nadmiernie obciążone przez długi czas, mogą się przełączyć z ochrony na uruchamianie śmierci komórkowej.
NXP800 uderza w kluczowy sensor stresu
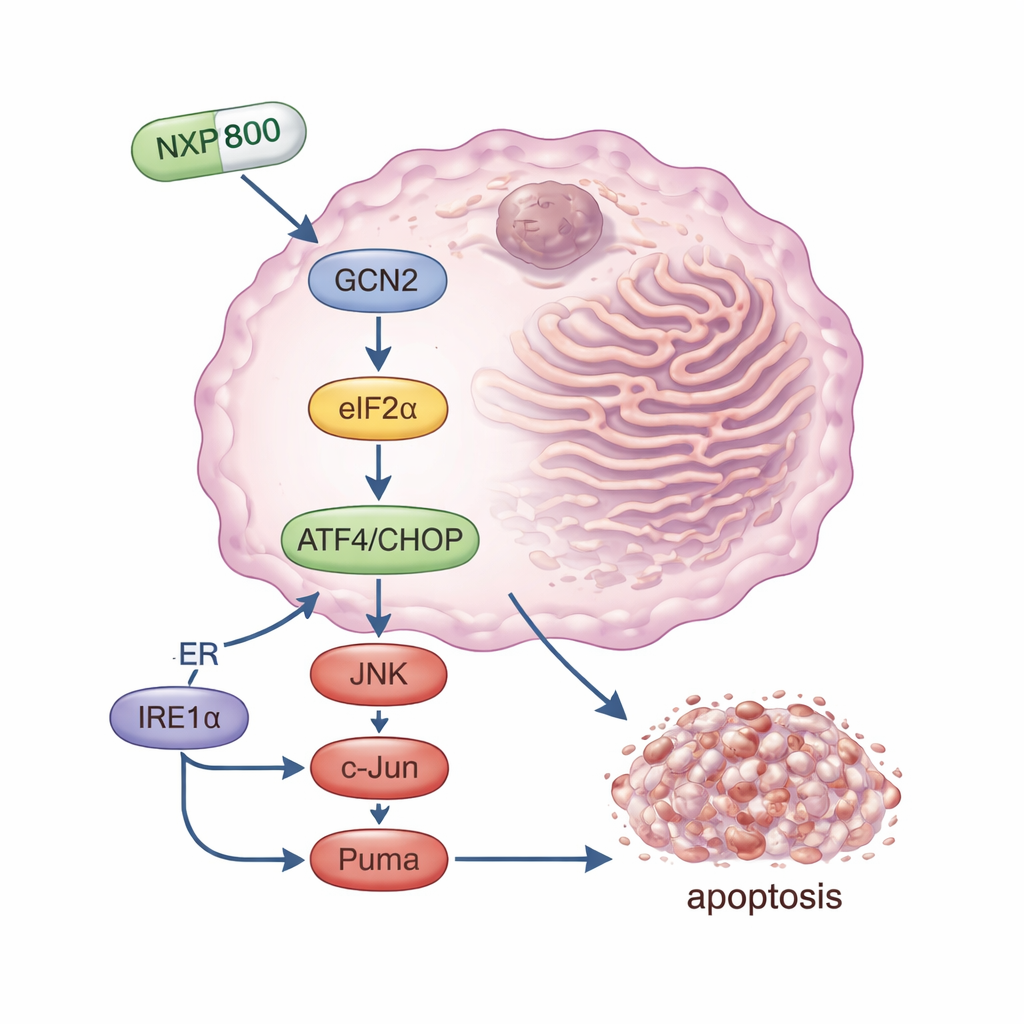
NXP800 to doustna mała cząsteczka, która pierwotnie rozwijana była jako inhibitor szlaku odpowiedzi na szok cieplny związanego z przetrwaniem nowotworu. W tym badaniu badacze odkryli, że w komórkach osteosarcoma jej główny efekt jest inny: silnie aktywuje białko-sensor stresu o nazwie GCN2. Po włączeniu GCN2 modyfikuje czynnik eIF2α, co szybko redukuje ogólną produkcję białek przy jednoczesnym zwiększeniu poziomów wybranych „głównych przełączników” stresu, w szczególności białka ATF4 i jego partnera CHOP. Te molekuły razem popychają komórkę w kierunku zaprogramowanej śmierci. Zespół wykazał, że gdy zablokowali GCN2 — albo poprzez wyciszenie genu, albo za pomocą oddzielnego inhibitora — NXP800 nie był już w stanie skutecznie wywołać tego łańcucha reakcji, a komórki nowotworowe stały się znacznie mniej wrażliwe na lek. To wskazuje GCN2 jako kluczowy cel działania NXP800 w osteosarcoma.
Zaangażowanie wielu szlaków śmierci w guzie
Poza gałęzią GCN2 w sieci stresowej, NXP800 uruchomił także inną drogę związaną ze śmiercią komórkową. Aktywował sensor IRE1α, który z kolei stymulował białka sygnałowe JNK i c-Jun. Ta gałąź jest znana z promowania produkcji Pumy, silnej pro-śmierci molekuły uszkadzającej wewnętrzne mechanizmy przetrwania komórki. W eksperymentach laboratoryjnych NXP800 spowalniał wzrost komórek osteosarcoma, zatrzymywał ich cykl komórkowy i aktywował enzymy oraz zmiany białkowe charakterystyczne dla apoptozy, czyli kontrolowanej śmierci komórkowej. Co ważne, normalne komórki macierzyste związane z kością były znacznie mniej dotknięte, co sugeruje pewien stopień selektywności wobec komórek nowotworowych już żyjących na granicy tolerowanego stresu.
Od stolika laboratoryjnego do modeli żywych
Aby sprawdzić, czy te komórkowe efekty przekładają się na kontrolę guza in vivo, badacze przetestowali NXP800 u myszy z implantowanymi ludzkimi komórkami osteosarcoma przy kości piszczelowej. Myszom podawano NXP800 doustnie; rozwijające się u nich guzy rosły znacząco wolniej i na koniec badania miały w przybliżeniu połowę objętości guzów u myszy nieleczonych. Próbki guzów z leczonych zwierząt wykazywały wyraźne ślady mechanizmu działania leku: wyższe poziomy markerów stresu eIF2α i ATF4, mniej komórek aktywnie dzielących się i więcej komórek poddających się apoptozie. Osobne eksperymenty bezpieczeństwa na zdrowych myszach nie wykazały istotnych uszkodzeń narządów, a testy czynności wątroby nie pogorszyły się, co wspiera możliwy do zaakceptowania profil bezpieczeństwa przy zastosowanych dawkach.
Co to może znaczyć dla pacjentów
Podsumowując, praca ta pokazuje, że NXP800 może opóźniać wzrost osteosarcoma poprzez celowe nadaktywowanie własnych mechanizmów obronnych komórki nowotworowej aż do momentu uruchomienia samozniszczenia. Poprzez celowanie w sensor stresu GCN2 i powiązane szlaki, lek oferuje całkowicie nowy sposób osłabienia guzów, które oporne są na tradycyjną chemioterapię. Ponieważ NXP800 jest już badany we wczesnych próbach klinicznych w innych nowotworach, wyniki te sugerują możliwość repozycjonowania leku dla osteosarcoma, samodzielnie lub w połączeniu z istniejącymi terapiami. Choć konieczne będą badania u ludzi, aby potwierdzić korzyści i bezpieczeństwo, to badanie dostarcza przekonującego dowodu koncepcji, że obrócenie stresu komórkowego przeciwko guzowi może otworzyć nowy rozdział terapeutyczny dla pacjentów z tym trudnym nowotworem kości.
Cytowanie: Racineau, E., Lallier, M., Postec, A. et al. Activating GCN2 and subsequently the Unfolded Protein Response with the small oral molecule NXP800 delays tumor growth in osteosarcoma. Cell Death Discov. 12, 94 (2026). https://doi.org/10.1038/s41420-026-02941-2
Słowa kluczowe: mięsak kości (osteosarcoma), NXP800, odpowiedź na stres, szlak GCN2, apoptoza