Clear Sky Science · pl
Egzosomalne pęcherzyki pochodzące od BMSC nasilają proliferację i przerzuty osteosarcoma poprzez szlak circRNA-0010220/β-katenina
Dlaczego ta historia o raku kości ma znaczenie
Osteosarcoma to najczęstszy nowotwór kości u dzieci i młodych dorosłych, który często daje przerzuty do płuc. Nawet przy współczesnej chemioterapii i zabiegach chirurgicznych wielu pacjentów wciąż doświadcza nawrotów i zagrażających życiu przerzutów. Badanie to zagląda w ukryte „rozmowy” między komórkami nowotworu a pobliskimi komórkami macierzystymi szpiku kostnego, odsłaniając maleńki cząsteczkowy posłaniec, który pomaga guzom rosnąć i się rozsiewać — i który mógłby stać się nowym celem terapeutycznym.
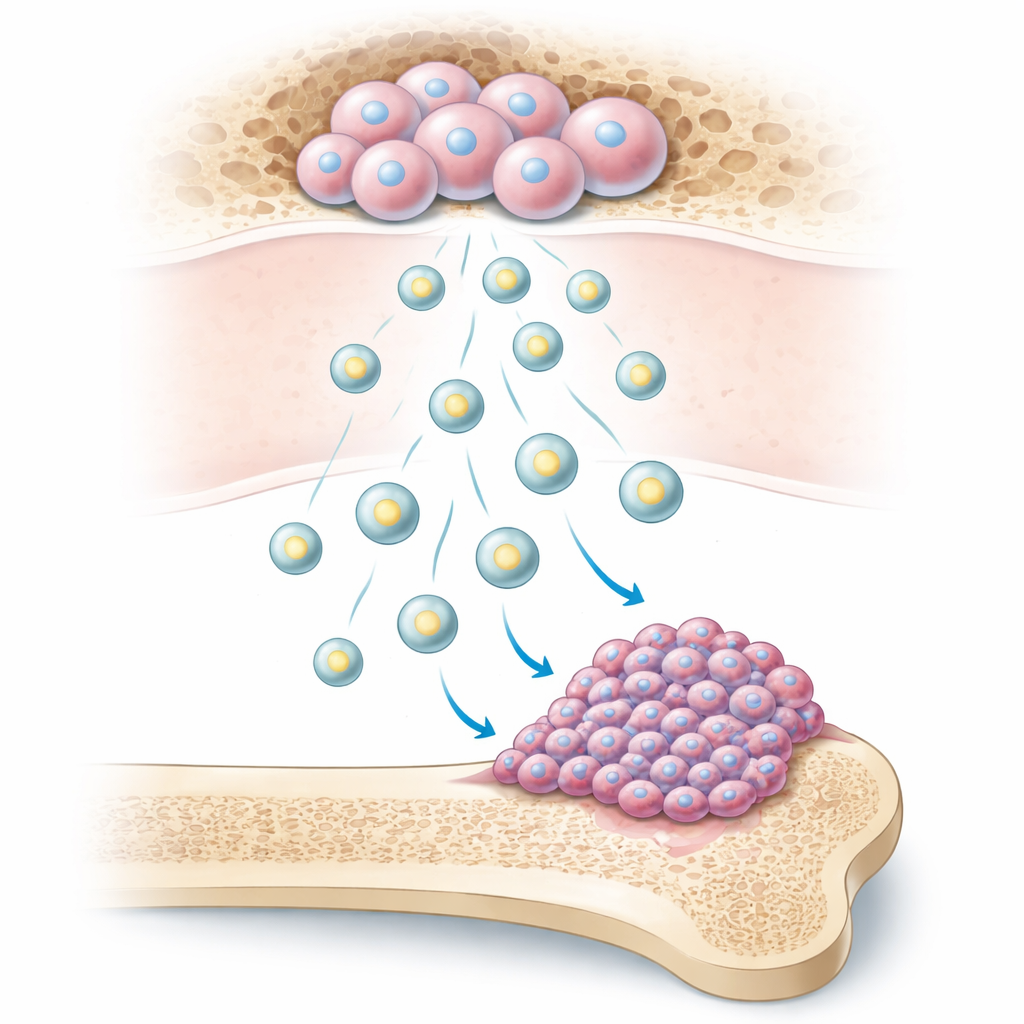
Małe pakunki o dużym wpływie
W naszych kościach znajdują się mezenchymalne komórki macierzyste szpiku kostnego, wszechstronne komórki biorące udział w utrzymaniu i naprawie kości. Te komórki uwalniają mikroskopijne, otoczone błoną pęcherzyki zwane pęcherzykami zewnątrzkomórkowymi. Badacze wykazali, że komórki osteosarcoma chętnie wchłaniają te pęcherzyki. Wówczas komórki nowotworowe zaczynają dzielić się szybciej, tworzyć więcej kolonii, poruszać się szybciej po powierzchniach i penetrować bariery w testach laboratoryjnych. U myszy guzy narażone na te pęcherzyki rosły większe i dawały więcej przerzutów do płuc, co wskazuje, że te mikroskopijne pakunki znacznie zwiększają agresywność nowotworu.
Okrągły przekaz, który wzmacnia raka
Zespół następnie zbadał, które genetyczne komunikaty wewnątrz pęcherzyków najbardziej zmieniają komórki osteosarcoma. Skoncentrowano się na RNA kolistych, niedawno odkrytej klasie cząsteczek RNA, które tworzą zamknięte pętle i są wyjątkowo stabilne. Sekwencjonowanie ujawniło jedną wyróżniającą się cząsteczkę, nazwaną circRNA‑0010220, która była silnie podwyższona w komórkach osteosarcoma traktowanych pęcherzykami komórek macierzystych oraz w próbkach guzów od pacjentów. Kiedy naukowcy obniżyli poziomy circRNA‑0010220 w komórkach macierzystych, ich pęcherzyki straciły dużą część zdolności do stymulowania wzrostu, migracji i inwazji komórek nowotworowych — zarówno in vitro, jak i w modelach mysich. To wskazało circRNA‑0010220 jako kluczowy czynnik odpowiedzialny za szkodliwe efekty.
Wyłączony hamulec epigenetyczny
Idąc dalej, badacze odwzorowali, jak to RNA koliste przebudowuje zachowanie komórek nowotworowych. W komórkach osteosarcoma circRNA‑0010220 przemieszcza się do jądra komórkowego, centrum kontroli komórki. Tam wiąże się z białkiem zwanym EZH2, enzymem dodającym chemiczne znaczki do histonów — białek pełniących rolę szpulek, wokół których owinięte jest DNA. Działając razem, circRNA‑0010220 i EZH2 zwiększają specyficzny znacznik znany jako H3K27me3 w rejonie kontrolnym genu CTNNBIP1. Ta modyfikacja silnie upakuje chromatynę w tym obszarze, skutecznie wyłączając gen. Ponieważ CTNNBIP1 normalnie działa jako hamulec dla silnego szlaku promującego wzrost, jego wyciszenie usuwa ważne zabezpieczenie przeciwko niekontrolowanemu zachowaniu nowotworu.
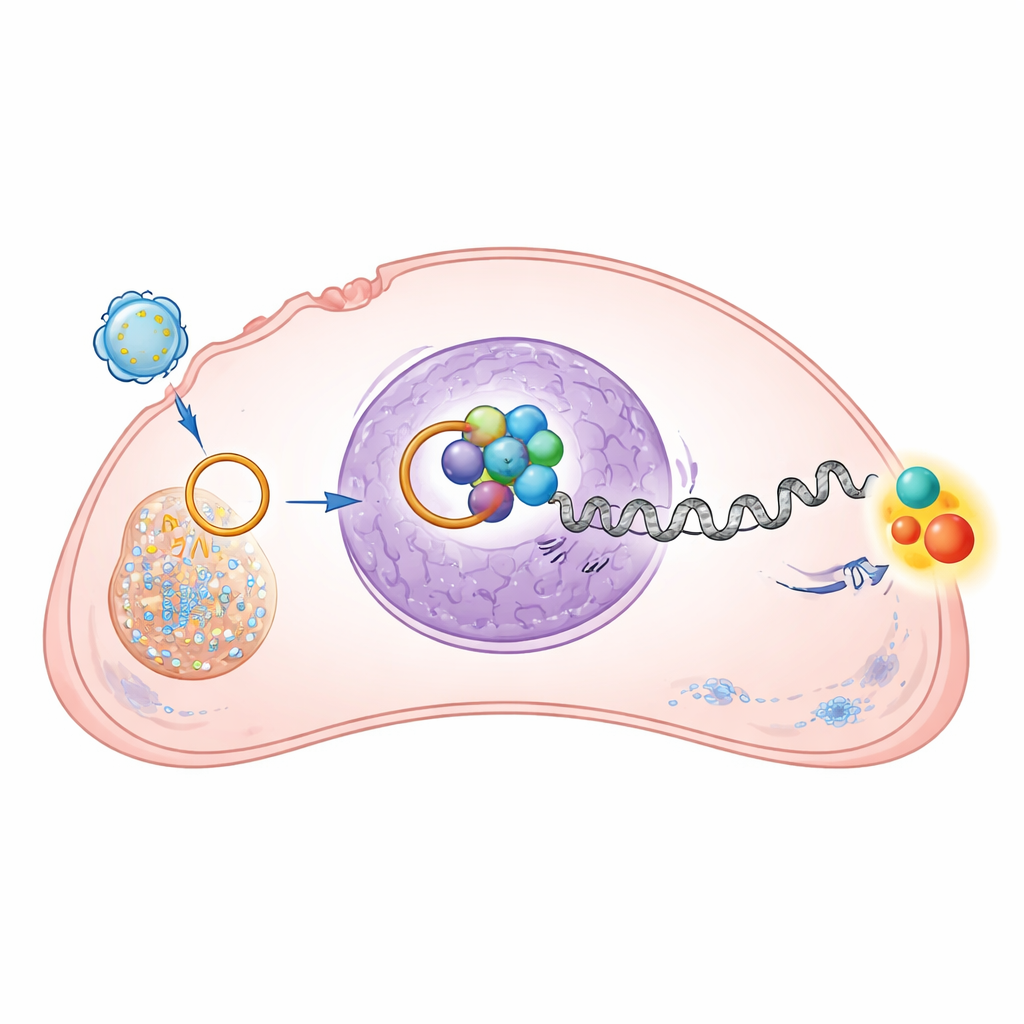
Włączenie potężnego szlaku wzrostu
CTNNBIP1 ogranicza szlak Wnt/β‑katenina, dobrze poznany system sygnalizacyjny, który, gdy jest nadmiernie aktywny, sprzyja dzieleniu się, migracji i przeżywaniu komórek. Poprzez wyłączenie CTNNBIP1, circRNA‑0010220 pośrednio zwiększa poziomy i aktywność jądrową β‑kateniny w komórkach osteosarcoma. Badanie wykazało, że geny kontrolowane przez ten szlak — związane z progresją cyklu komórkowego, cechami podobnymi do komórek macierzystych i inwazją — stały się bardziej aktywne, gdy obecne było pęcherzykowe circRNA‑0010220. Gdy badacze zastosowali lek blokujący specyficznie β‑kateninę, pro‑wzrostowe i pro‑migracyjne efekty circRNA‑0010220 zostały w dużej mierze odwrócone. Potwierdza to, że RNA koliste działa poprzez ten szlak wzrostu, napędzając progresję guza.
Co to oznacza dla przyszłego leczenia
Podsumowując, praca przedstawia pełny łańcuch zdarzeń: komórki macierzyste szpiku kostnego wysyłają pęcherzyki załadowane circRNA‑0010220 do komórek osteosarcoma; RNA koliste współdziała z EZH2 w jądrze, chemicznie uciszając CTNNBIP1; to uwalnia hamulec na szlaku Wnt/β‑katenina, co ostatecznie napędza szybszy wzrost i rozsiew guza. Dla pacjentów sugeruje to kilka nowych strategii terapeutycznych. Przerwanie transferu pęcherzyków, zablokowanie circRNA‑0010220, zakłócenie jego partnerstwa z EZH2 lub stłumienie sygnalizacji β‑kateniny mogłoby pomóc spowolnić progresję osteosarcoma. Choć pomysły te muszą jeszcze zostać zweryfikowane klinicznie, badanie ujawnia wcześniej ukrytą komunikację w mikrośrodowisku guza kostnego i wskazuje konkretne cele molekularne dla przyszłych leków.
Cytowanie: Pan, R., Pan, Y., Ruan, W. et al. BMSC-derived extracellular vesicles enhance osteosarcoma proliferation and metastasis via the circRNA-0010220/β-catenin pathway. Cell Death Dis 17, 376 (2026). https://doi.org/10.1038/s41419-026-08655-8
Słowa kluczowe: osteosarcoma, pęcherzyki zewnątrzkomórkowe, RNA koliste, Wnt beta-katenina, regulacja epigenetyczna