Clear Sky Science · pl
Utrata DIAPH3 przyspiesza powstawanie glejaka u myszy
Dlaczego to badanie mózgu ma znaczenie
Glejnik (glioblastoma) jest jednym z najbardziej śmiertelnych nowotworów mózgu; mimo operacji, radioterapii i chemioterapii większość pacjentów przeżywa niewiele ponad rok. To badanie stawia podstawowe, lecz kluczowe pytanie: jakie wczesne zmiany wewnątrz komórek mózgu popychają je w kierunku tak agresywnych guzów i dlaczego te nowotwory tak trudno zniszczyć promieniowaniem? Śledząc pojedyncze białko strukturalne w komórkach mózgu myszy, badacze ujawniają, jak jego utrata destabilizuje chromosomy, przyspiesza pojawianie się nowotworów i pomaga komórkom przypominającym komórki macierzyste raka przetrwać promieniowanie, które powinno je zniszczyć.
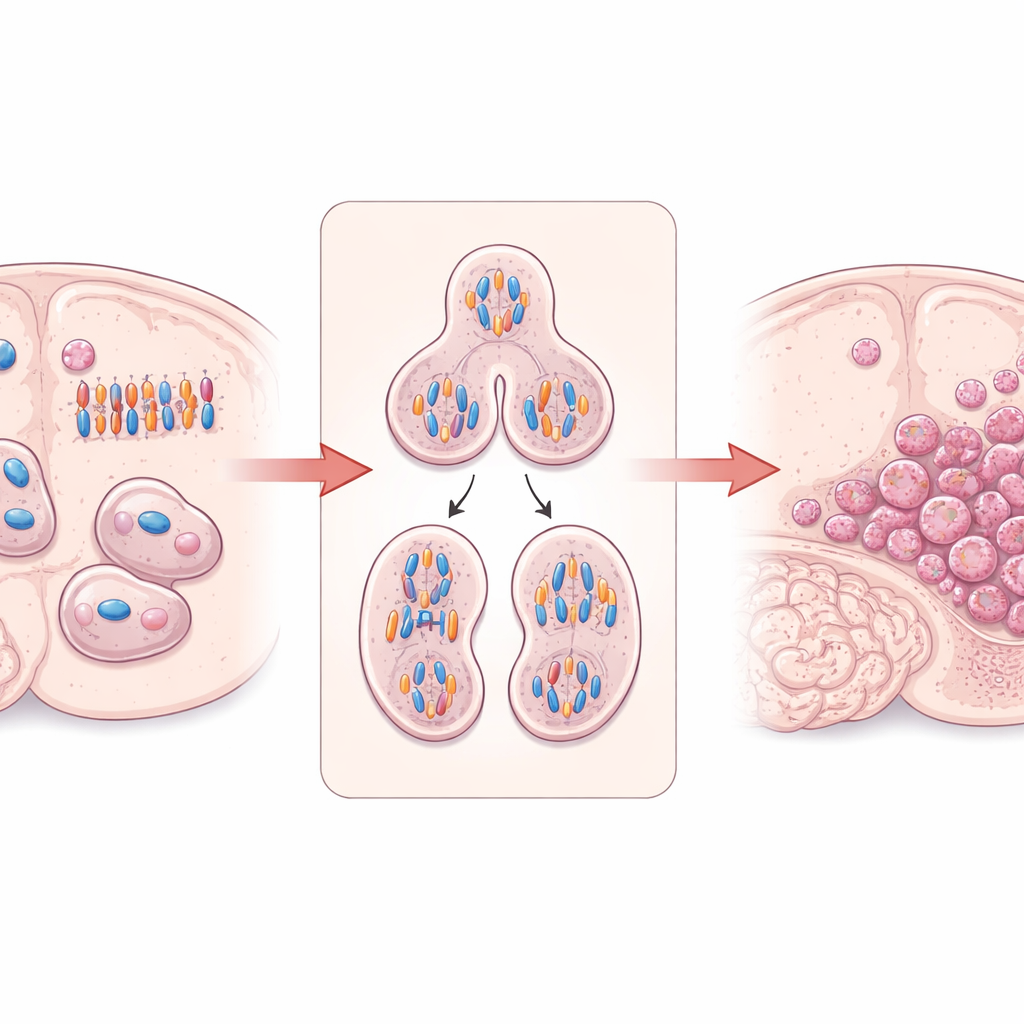
„Budowniczy” komórkowy, który pilnuje prawidłowego podziału
Praca koncentruje się na DIAPH3, białku pomagającym budować i organizować wewnętrzne rusztowanie komórki — włókna aktynowe i mikrotubule. W dzielących się komórkach macierzystych mózgu DIAPH3 jest niezbędny do utworzenia właściwego wrzeciona — struktury rozdzielającej zduplikowane chromosomy — oraz do rozdzielenia jednej komórki na dwie. Wcześniejsze badania wykazały, że gdy DIAPH3 jest nieobecny w rozwijających się mózgach myszy, komórki dzielące się często źle obsługują chromosomy, co prowadzi do nieprawidłowej liczby chromosomów (aneuploidii), zatrzymania cyklu komórkowego i śmierci komórki. Co ciekawe, mały region ludzkiego chromosomu 13 zawierający gen DIAPH3 jest często usuwany w glejaku, a wyższy poziom DIAPH3 wiązano z lepszym przeżyciem u niektórych pacjentów, co sugeruje, że to białko może pełnić rolę supresora guza w mózgu.
Inżynieria mózgów myszy do wzrostu guzów
Aby sprawdzić, czy utrata DIAPH3 rzeczywiście sprzyja nowotworowi mózgu, zespół stworzył myszy, u których dwa geny można było selektywnie usunąć w komórkach macierzystych tworzących korę: Diaph3 i Trp53, z którego pochodzi powszechnie znany strażnik genomu, p53. Myszy pozbawione jedynie Diaph3 w tym obszarze nie rozwijały guzów nawet po dwóch latach, co sugeruje, że p53 nadal może eliminować silnie nieprawidłowe komórki. W przeciwieństwie do tego, myszy pozbawione samego Trp53, albo zarówno Trp53, jak i Diaph3, ostatecznie tworzyły wysokozłośliwe, rozlane glejaki, które pod mikroskopem bardzo przypominały ludzką chorobę. Dzięki wielokrotnym skanom MRI o bardzo wysokim polu magnetycznym badacze wykazali, że zwierzęta pozbawione obu genów rozwijały wykrywalne guzy wcześniej, a w połowie życia częściej miały duże glejaki, szczególnie w opuszce węchowej, niż myszy pozbawione tylko Trp53. Szybkość wzrostu guza, gdy już się zaczęła, była podobna w obu grupach — zmieniało się to, jak szybko guzy się pojawiały.
Chaos chromosomalny i przebudowana aktywność genów
Dzięki analizie, dlaczego utrata DIAPH3 przyspiesza pojawienie się guza, zespół zbadał aktywność genów w opuszce węchowej młodych myszy, zanim pojawiły się jakiekolwiek widoczne guzy. U zwierząt pozbawionych zarówno Diaph3, jak i Trp53 126 genów było wyrażonych na innych poziomach w porównaniu z mutantami tylko Trp53, a niemal połowa z nich miała wcześniej powiązania z rakiem. Wiele zmian skupiało się w ścieżkach napędzających wzrost komórek, migrację i tworzenie naczyń krwionośnych, w tym sygnalizacji VEGF, MAPK, RAS, Rap1 i cAMP oraz sieciach związanych z receptorami sprzężonymi z białkami G. Ten zmieniony krajobraz molekularny sugerował, że komórki są wcześniej kierowane ku stanowi przypominającemu nowotwór. Analiza całogenomowych zmian liczby kopii w w pełni uformowanych guzach wykazała, że niedobór DIAPH3 nie zwiększał znacząco małych, ogniskowych zmian DNA, lecz raczej potęgował duże zyski i straty całych chromosomów — dokładnie tę aneuploidię, której należało się spodziewać po wadliwym segregowaniu chromosomów.
Wrodzone uszkodzenia DNA i bardziej wytrzymałe komórki macierzyste nowotworu
Komórki nowotworowe z aneuploidią nosiły więcej wewnętrznych uszkodzeń DNA, wykrytych przez podwyższone poziomy markera złamań DNA γ-H2AX rozproszonych po jądrach komórkowych. Mimo to guzy nadal rosły, co sugeruje, że nabyły mechanizmy tolerowania takiego stresu. Porównując ekspresję genów w ustalonych guzach, badacze znaleźli setki genów zmienionych przez utratę DIAPH3, w tym uderzającą amplifikację i nadprodukcję receptora czynnika wzrostu FGFR2 w wielu guzach o podwójnej mutacji. Wiadomo, że FGFR2 wzmacnia mechanizmy naprawy DNA w komórkach glejaka, a jego aktywacja wiązana jest z opornością na promieniowanie. Zespół wyizolował komórki przypominające komórki macierzyste glejaka z guzów myszy i sprawdził ich odpowiedź na klinicznie relewantną dawkę promieniowania jonizującego. Przed leczeniem częstość komórek macierzystych była podobna w obu genotypach, ale po naświetlaniu kultury z guzów pozbawionych DIAPH3 zachowały około dwa razy więcej aktywnych komórek przypominających komórki macierzyste niż te z guzów z samym Trp53, co wykazało większą oporność na promieniowanie.
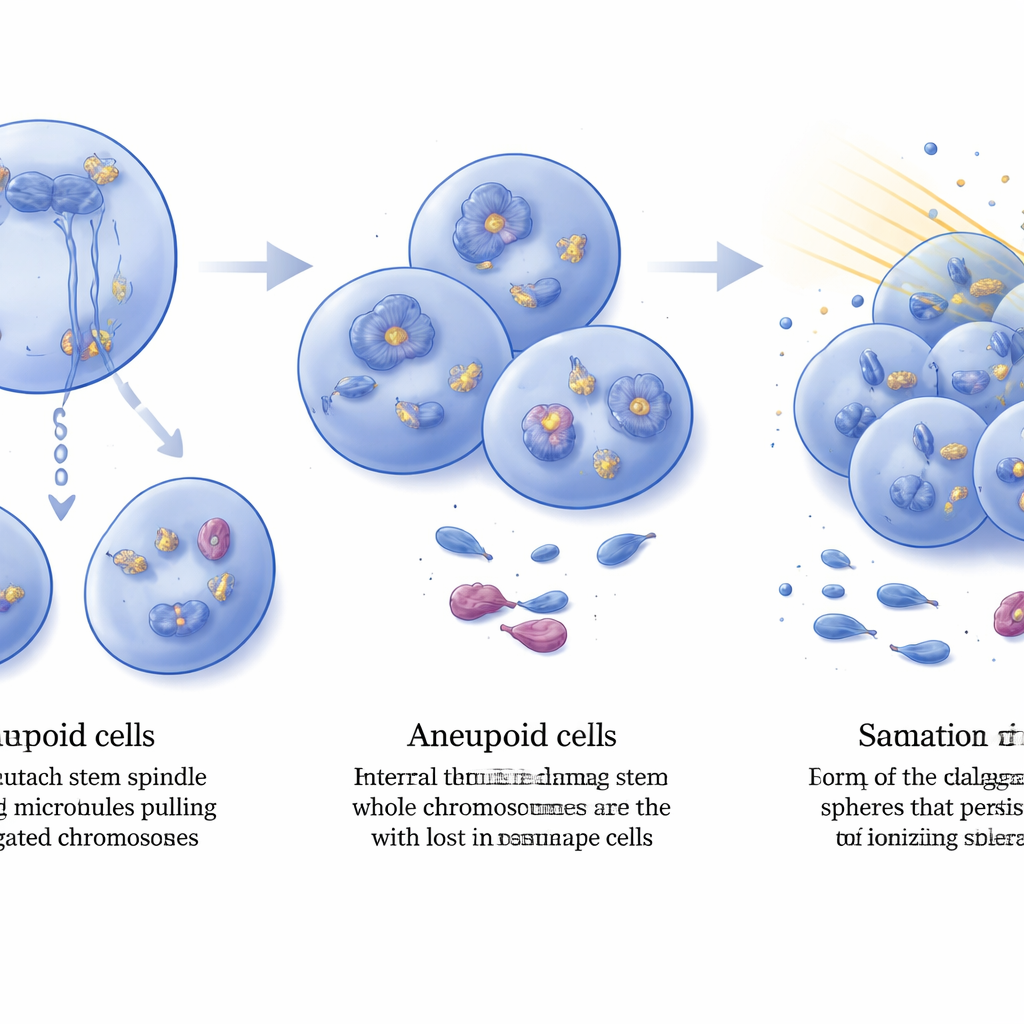
Co to oznacza dla raka mózgu
Podsumowując, badanie przedstawia DIAPH3 jako strażnika, który pomaga komórkom macierzystym mózgu dzielić się z właściwą liczbą chromosomów. Gdy zarówno DIAPH3, jak i p53 są nieobecne, podział komórki staje się podatny na błędy, całe chromosomy są tracone lub zyskiwane, a uszkodzenia DNA narastają. Zamiast ginąć, niektóre komórki adaptują się przez amplifikację czynników związanych z naprawą, takich jak FGFR2, przekształcając się w aneuploidalne, wysokozłośliwe glejaki, których komórki przypominające komórki macierzyste są wyjątkowo odporne na promieniowanie. Choć modele mysie nie odzwierciedlają każdego aspektu ludzkiego glejaka, wyniki te wskazują DIAPH3 jako potencjalny biomarker rokowania oraz jako węzeł w sieci procesów kontrolujących inicjację guza, stabilność genomu i odpowiedź na leczenie — otwierając nowe drogi do terapii, które mogą w przyszłości uczynić ten wyniszczający nowotwór mózgu bardziej podatnym na istniejące metody leczenia.
Cytowanie: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Słowa kluczowe: glejak, niestabilność chromosomalna, komórki macierzyste nowotworu mózgu, oporność na radioterapię, geny supresorowe guza